
题目列表(包括答案和解析)
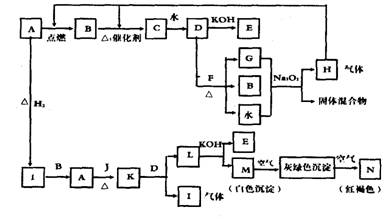
26.(7分)已知A-N为不同物质的代号,其中A、J为固体单质。F为焰色反应呈黄色的固体化合物,从A开始可发生以下一系列变化:
试回答:
(1)写出下列物质的化学式:
A____________B___________C___________D___________E___________
(2)写出有关反应的化学方程式:
D和F反应______________________ 由M生成N______________________
25.(4分)有A、B、C、D四瓶未知溶液,它们是Na2C03,K2S04,KHS04和Ba(N03)2,为了鉴别它们,进行如下实验:由此推断
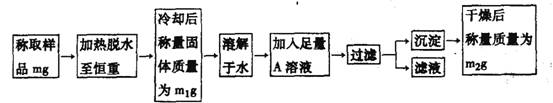
A_____________,B_____________。C_____________,D_____________。
24.(5分)已知:氢氧化钙在水中存在下列溶解平衡 Ca(OH)2(固) ?Ca2++20H-在火力发电厂燃烧煤的废气中往往含有S02、O2、N2、C02等。为了除去有害气体S02并变废为宝,常常用粉末状的碳酸钙或熟石灰悬浊液洗涤废气,反应产物为石膏。
(1)写出上述两个反应的化学方程式:__________________________
①S02与CaC03悬浊液反应:__________________________
②S02与Ca(OH)2悬浊液反应:__________________________
(2)试说明用熟石灰的悬浊液,而不用澄清石灰水洗涤废气的理由:
__________________________
(3)在英国进行的一个研究结果表明:高烟囱可以有效地降低地面S02浓度。在20世纪的60-70年代的10年间,由发电厂排放出的S02增加了35%,但由于建造高烟囱的结果,地面浓度降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?并简述其理由
23.(5分)过氧化氢(H202)俗称双氧水,它是一种液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上采用“醇析法”将H202转化成固态的过碳酸钠晶体(其化学式为2Na2C03·3H202)。该晶体具有Na2C03和H202的双重性质。“醇析法”的生产工艺过程如下:在0-5℃下,往饱和的Na2C03溶液中先后加H202、稳定剂(MgCl2和Na2Si03)和异丙醇,经充分反应,过滤分离,即得过碳酸钠晶体。
(1)固化H202采用Na2C03作载体的理由是__________________________
(2)反应控制在0-5℃下进行的原因是__________________________
(3)稳定剂能反应生成不溶物将过碳酸钠粒子包裹住,该反应的化学方程式为:__________________________
(4)下列物质不会使过碳酸钠失效的是_____________
A.Mn02 B.H2S
C.CH3COOH D.NaHC03
(5)加入异丙醇的作用是_____________。
22.(10分)要同时测定混有少量氯化钠杂质的芒硝(Na2SO4·nH20)的纯度和结晶水的含量,按下列流程进行实验:
(1)加热脱水时,若有固体飞溅出来造成损失,则会使测得的结晶水的含量偏______________。加热脱水后,若将样品露置于空气中冷却,则会使测得的结晶水的含量偏_____________
(2)现有硝酸银、氯化钡、氯化钙、硝酸钡、氢氧化钡五种溶液,从测定的准确性考虑,可作为A溶液的分别是_____________。若加入A溶液的量不足,会使测得的纯度偏_____________。判断A溶液是否足量的方法是_____________
(3)过滤时,应把滤纸上的沉淀洗涤干净,洗涤沉淀的方法是__________________________若不洗涤,会使测得的纯度偏_____________
(4)通过实验,测得芒硝化学式中n值为10,则芒硝的纯度为____________%
21.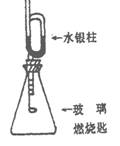 (4分)如图装配好装置,待内外空气压强不变时标注出水银液面的刻度(用红漆),取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢回到原标定的刻度。简要回答下列问题
(4分)如图装配好装置,待内外空气压强不变时标注出水银液面的刻度(用红漆),取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒精灯点燃迅速移入锥形瓶中并塞紧橡皮塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢回到原标定的刻度。简要回答下列问题
(1)水银柱推向左管说明什么?
(2)硫粉未燃尽时火焰就熄灭了,说明:
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?
(4)根据反应方程式S+O2?S02和上述结论又可推导出什么(或证明什么)?
20.密度为1.4g/cm3的稀硫酸溶液中,逐滴加入BaCl2溶液,直至沉淀完全为止,已知沉淀的质量与硫酸溶液质量恰好相等,则原硫酸的浓度为
A.29.6% B.42.1%
C.14.81m01·L-1 D.6.02mol·L-1
第Ⅱ卷(非选择题 共50分)
19.你认为减小酸雨产生的途径,可采取的措施是
①少用煤作燃料,②把工厂烟囱造高,③燃料脱硫,④在已酸化的土壤中加石灰,⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
18.有反应2FeS04=Fe203+S02↑+S03↑将生成的混合气体通入
BaCl2溶液中生成的沉淀是
A.Ba(HS03)2 B.BaS03
C.BaS04 D.BaS03和BaS04
17.下列各种气体,不能用浓H2S04干燥的是:①Cl2②H2③CO④HCl⑤02⑥H2S⑦NH3
A.②③⑥⑦ B.②③④⑥⑦
C.②⑥⑦ D.⑥⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com