
题目列表(包括答案和解析)
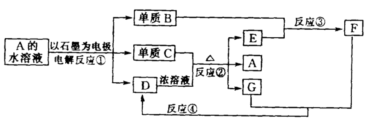
25、(12分)下图中每一方框内的字母代表一种反应物或生成物。
从A到F均为中学化学常见的物质,其中B跟E反应生成物质F,某温度下该反应起始和某时刻的反应混合物组成如右表所示。请写出下列反应的化学方程式:反应①_______ _____;反应②__ _____ _______;反应③(须注明反应条件)___ ___________;反应④_________ ___ ___。
24、(8分)A、B、C、D均为短周期元素,B、A可形成两种液态化合物,其原子个数比分别为1∶1和2∶1,且分子中电子总数分别为18和10;B与D能形成一种极易溶于水的碱性气体X, B与C能形成一种极易溶于水的酸性气体Y 。X分子与B2A分子中的电子数相同,Y分子中的电子数为18,A、B和D可形成离子化合物,其化学式为B4A3D2,其水溶液呈弱酸性。请回答:
(1)元素符号:C_________,D__________。
(2)B4A3D2的化学式___________,其水溶液呈现酸性的离子方程式________。
(3)写出化学方程式:C2和X(过量)反应__________。
(4)液态X能电离(可根据B2A电离推知),其阴离子电子式________。
|
|
B E
F |
|
起始组成n / mol |
2 4
0 |
|
某时刻组成
n / mol |
1 2
2 |
23、(12分)图2是实验室制取Cl2并以Cl2为原料进行特定反应的实验。
(1)A为氯气发生装置,写出反应的化学方程式:_________。
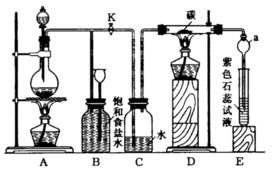
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C瓶后进入D。D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g)。试写出D装置中反应的化学方程式:__________;装置C的作用是_________。
(3)E处石蕊试液中的现象是________,其原因是________,干燥管a的作用是______。
(4)若将E处溶液改为石灰水,反应过程的现象是_________(填序号)。
A、有白色沉淀生成 B、无白色沉淀生成
C、先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是_________,B的作用是_________。
22、(6分)下面a~e 是中学化学实验中常见的几种定量仪器:
a、量筒 b、容量瓶 c、滴定管 d、托盘天平 e、温度计
(1)其中标出仪器使用温度的是___________(填写编号)。
(2)能够用以精确量取液体体积的是____________(填写编号)。
(3)由于错误操作,使得到数据比正确数据偏小的是_____(从下列A、B、C中选)。
A、用量筒最取一定量液体时,俯视液面读数
B、中和滴定达终点时俯视滴定管的液面读数
C、使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度
21、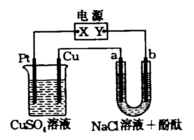 (8分)图1所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色。
(8分)图1所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色。
(1)Y为电源的_________极;
(2)写出U型管中的电极反应式:
a_______________________;
b_______________________;
(3)原烧杯中CuSO4溶液是不饱
和的,在通电过程中,CuSO4
溶液的pH_______(填“变大”、“不变”或“变小”)
20、(8分)电子表和电子计算器的电池常用微型银-锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应和总反应分别为:
Zn + 2OH――2e-= ZnO + H2O和Ag2O + Zn = 2Ag + ZnO
(1)该原电池工作时,负极区溶液的pH_______ (填“上升”、“下降”或“不变”)
(2)该原电池工作时,电子由__________(填“Zn”或“Ag2O”)极经外电路流向________(填“正”或“负”)极,正极上发生的电极反应式为__________________________。
19、(7分)(1)过氧化氢(H2O2)可作为采矿业废液消毒剂,如要消除采矿业废液中的氰化物(其中氮元素为-3价),化学反应式(已配平)为:KCN+H2O2+H2O== A + NH3↑
①生成物A 化学式为__________。
②反应中被氧化的元素为___________。
(2)人体内O2-离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生下列反应,请完成该反应的离子方程式: O2- + H2O == H2O2 + O2+ 。
18、锌粉、铝粉、镁粉的混合物ag,与质量分数为25%的稀硫酸恰好反应完全,蒸发水分后得固体X(不含结晶水)bg,则反应生成的氢气质量为:
A、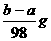 B、
B、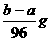
C、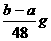 D、无法计算
D、无法计算
第II卷(非选择题,共78分)
17、 下列离子方程式正确的是:
下列离子方程式正确的是:
 A、纯碱与水反应:CO32-+2H2O H2CO3+2OH-
A、纯碱与水反应:CO32-+2H2O H2CO3+2OH-
B、用惰性电极电解氯化镁溶液: 2Cl- +2H2O Cl2↑+ H2↑+2OH-
C、硫酸亚铁溶液中加过氧化氢溶液:Fe2+ + 2H2O2 + 4H+ = Fe3+ + 4H2O
D、氨水与少量的二氧化硫反应:2NH3·H2O + SO2 = 2NH4+ + SO32-+H2O
16、无色X溶液与铝反应能放出氢气,下列离子组一定不能在原X溶液大量共存的是:
A、Mg2+、Na+、Cl-、NO3- B、Na+、K+、S2-、SO32-
C、NH4+、Mg2+、SO42-、Cl- D、NH4+、Na+、HSO3-、Br-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com