
题目列表(包括答案和解析)
22.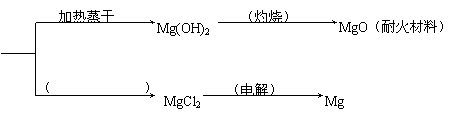 (8分)已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
(8分)已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
MgCl2·6H2O
请回答下列问题:
(1)在上图中的括号内填写适当的反应条件。
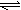 (2)Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固) Mg2++2OH-。向体系中加入(至少填出两种不同类别的物质)
,有利于Mg(OH)2溶解。
(2)Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固) Mg2++2OH-。向体系中加入(至少填出两种不同类别的物质)
,有利于Mg(OH)2溶解。
(3)NaF和MgO的核间距离分别为2.31×10-10m和2.10×10×10-10m,但两者的熔点分别为993℃和2852℃。试解释其可能的原因
。
(4)依据绿色化学的原子经济的概念(即化学反应的原料中每个原子都参与反应并全部转化为产物),203 kg MgCl2·6H2O原料可以获得29.8 kg MgO、 kg36.5%盐酸和 kg MgCl2。
21.(8分)如图所示:
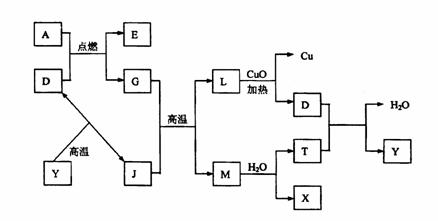
其中A、G是固体单质,其余是化合物。X是常用于切割和焊接金属的可燃性气体;Y
是一种难溶于水的白色固体,它的式量是100。
请填空:
(1)D的电子式是 。
(2)A跟D反应的化学方程式是 ;
该反应的反应热△H
0(填“<、=、>”  。
。
(3)在高温条件下,G跟J反应的化学方程式是 。
20. (11分) (1) 某无色透明的溶液,跟金属铝反应时放出H2,试判断下列离子: Mg2+、 Cu2+、 Ba2+、H+、Ag+、SO42一、HCO3一、OH一、NO3一在下述两种情况中,可能存在于此溶液中的是:
① 当与铝反应后生成Al3+时,原溶液可能存在的离子是____________________。
② 当与铝反应后生成AlO2一时,原溶液可能存在的离子是____________________。
(2)拉曼·光谱表明溶液中不存在AlO2-离子,实际存在[Al(OH)4]- 离子,在200mL0.2mol/L Na[Al(OH)4]溶液中逐滴加入0.2mol/L H2SO4溶液250mL,试回答:
①写出分两步反应的离子方程式____________________,_________________________。
②反应完全后,溶液中Al3+离子与SO42-离子的物质的量之比为___________。
19.(7分) 碳的稳定的氧化物除CO、CO2外,还有C3O2、C4O3、C5O2、C12O9等低氧化物,其中C3O2是一种在常温下有恶臭的气体,其分子中的每个原子都满足最外层8电子结构。假设在一定条件下 CH3COOH→CH2=C=O+H2O。
①C3O2分子的电子式为___________;
②在上述碳的低氧化物中,若有分子空间构型与 C3O2相同的,最可能是___________;
③不考虑反应条件,根据你现有的化学知识判断, O2、HCl能与 C3O2发生反应,请将能够反应的化学方程式写在下面。
_______________________________________,_____________________________________,
18.有四位学生设计了下列四个方案确证溶液中含SO42-,你认为合理的是
BaCl2溶液 足量盐酸

 A.方案甲:试液
白色沉淀
沉淀不溶解
A.方案甲:试液
白色沉淀
沉淀不溶解
BaCl2溶液 足量硝酸

 B.方案乙:试液
白色沉淀
沉淀不溶解
B.方案乙:试液
白色沉淀
沉淀不溶解
足量硝酸 Ba(NO3)2溶液

 C.方案丙:试液
无沉淀
白色沉淀
C.方案丙:试液
无沉淀
白色沉淀
足量盐酸 Ba(NO3)2溶液

 D.方案丁:试液
无沉淀
白色沉淀
D.方案丁:试液
无沉淀
白色沉淀
17.微量硒元素对人体有保健作用,已知硒与氧同主族,与钾同周期,下列有关硒元素的性质描述错误的是
A.硒既能溶于盐酸又能溶于烧碱溶液
B.硒的非金属性比溴弱,
C.硒的最高价氧化物的化学式为SeO3
D.硒的气态氢化物的化学式为 H2Se
16.下列根据实验现象的判断中,正确的是
A.能使湿润的碘化钾淀粉试纸变蓝的气体一定是氯气
B.在潮湿的空气中能形成白雾的气态氢化物一定是氯化氢
C.溶于水中能形成无色溶液的棕色气体一定是二氧化氮
D.能用于做喷泉实验的气体只能是氨气或氯化氢
15.将8gFe2O3投入150 mL某浓度的稀硫酸中,再投入7g铁粉,共收集到1.68LH2(标况),同时Fe和Fe2O3均无剩余。向溶液中滴入KSCN溶液,未见颜色变化。为了中和过量的H2SO4,且使Fe2+恰好完全转化为Fe(OH)2沉淀,共消耗4mol/L的NaOH溶液150mL。则原H2SO4的物质的量浓度为
A.1 mol/L B. 2 mol/L C.3 mol/L D. 4 mol/L
14.A、B、C、D、E分别是 Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:(1)A、C均能与稀 H2SO4反应放出气体;(2)B与D的硝酸盐反应,置换出单质D;(3)C与强碱反应放出气体;(4)C、E在冷浓H2SO4中发生钝化反应,由此可以推断A、 B、 C、 D、E依次为
A.Fe、Cu、Al、Ag、Mg B.Al、Cu、Mg、Ag、Fe
C.Mg、Cu、Al、Ag、Fe D.Mg、Ag、Al、Cu、Fe
13.下列各组溶液,不用其它试剂就可以将它们区别开的是
①KOH、K2CO3、MgSO4、KHSO4 ②NaNO3、HCl、NH4Cl、KOH
③BaCl2、CaCl2、Na2SO4、AgNO3 ④AlCl3、NaOH、NaHCO3、MgCl2
A.①④ B.①③ C.②④ D.②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com