
题目列表(包括答案和解析)
1.下列物质不属于“城市空气质量日报”报道的是
(A)二氧化硫 (B)氮氧化物 (C)二氧化碳 (D)悬浮颗粒
24.(10分)现有Na2O2和NaHCO3固体混合物0.06mol,在密闭容器中加热到250℃,让其充分反应后排出气体(包括水蒸气),冷却,称得残留固体质量为Ag。设混合物中Na2O2
为xmol(0<x<0.06),当x取不同数值时,气体的成分、残留固体成分会发生变化。请完
成下表(A值可以用包含x的式子表示):
|
x值 |
气体成分 |
残留固体成分 |
A值 |
|
0<x<0.02 |
|
Na2CO3 |
|
|
|
H2O 、O2 |
|
A=4.24 |
|
|
H2O 、O2 |
Na2CO3、NaOH |
A=3.96+14x |
|
x=0.03 |
O2 |
|
A=4.38 |
|
0.03<x<0.06 |
|
Na2CO3、NaOH 、Na2O2 |
|
23.(10分)实验室可通过多条途径得到氮气,常见的三种方法是:
方法一,将氨气通入灼热的氧化铜粉末,得到纯净氮气和铜。
方法二,将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末。
方法三,将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
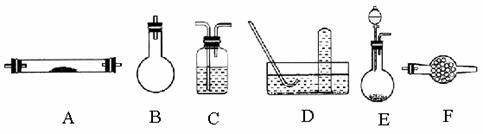 下列是进行实验进可选择的实验仪器(其它必要的仪器如:铁架台、铁夹、铁圈、石棉网、酒精灯等未列出):
下列是进行实验进可选择的实验仪器(其它必要的仪器如:铁架台、铁夹、铁圈、石棉网、酒精灯等未列出):
请回答下列问题:
(1)方法一制氮气;氨气是用浓氨水跟生石灰反应得到,此反应最好选用(填仪器的编号) 作发生装置,该反应的化学方程式
。要制取并收集纯净的氮气(可含有少量的水),还使用上述仪器中的(填仪器的编号,并按气流方向人左向右列出)
。
(2)在制取氮气的三种方法中,方法一和方法二越来越受到人们的关注,经常被联合使用。这两种方法与方法三相比,其优越性在于
。
22.(10分)从固体混合物A出发可以发生如下框图所示的一系列变化
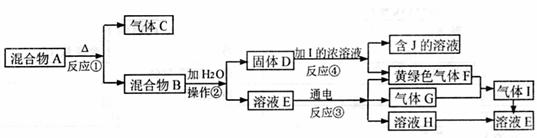
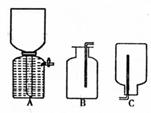
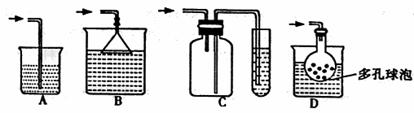
(1)在实验室中收集气体C,可选择右图装置中的 (填选项字母)
(2)操作②的名称是 ,在操作②中所使用的玻璃仪器的名称是 ,在得到固体D时必须进行洗涤、干燥等操作。洗涤固体D的操作方法
 是
。
是
。
(3)写出下列反应的化学方程式或离了方程式:
反应①
反应③
反应④
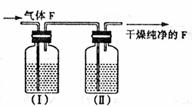 (4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如下示意图中的装置,其中瓶I中盛放的是
,瓶II中盛放的是:
。
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如下示意图中的装置,其中瓶I中盛放的是
,瓶II中盛放的是:
。
(5)实验中多余的气体F必须吸收,以免污染空气。下图是实验室用NaOH吸收气体F的装置,为防止产生倒吸现象,合理的装置是 。
21.(8分) 已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。从溶 液中将C u2+、Fe2+、Fe3+沉淀为氢氧化物所需pH值分别为6.4,6.4,3.7。 现有氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制取纯净的CuCl2·2H2O, 首先将其制成水溶液,然后按下图步骤进行提纯

现有可供选择的试剂组:
|
|
A |
B |
C |
D |
|
X |
H2O2 |
KMnO4 |
NaClO |
K2Cr2O7 |
|
Y |
CuO |
Cu(OH)2 |
CuO |
CuCO3 |
回答下列问题:
(1)最合适本实验的试剂组是 。
(2)加氧化剂的目的是 。
(3)本实验用加碱沉淀法直接除去FeCl2能达到目的吗?为什么?
。
(4)最后能否直接蒸发结晶,应如何操作?
。
20. (7分)硝酸工业中尾气中N的氧化物(NO、NO2)是主要的大气污染之一,其常用的治理方法中有以下两种(已简化)。
①NaOH吸收法,反应原理如下:
2NO2+2NaOH=NaNO3+NaNO2+H2O NO+NO2+2NaOH=NaNO2+NaNO2+H2O
②氨催化还原法,反应原理是:
NOx+NH3 N2+H2O(未配平)
N2+H2O(未配平)
现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体),若用过量的NaOH吸收后溶液中NaNO3和NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
x=__________________________________________。
(2)将1体积的该尾气用②的方法处理,至少消耗相同状况下的NH3的体积为____________。
(3)配平下列方程式:
______NOx+_____NH3=______N2+_____H2O
19.(9分)A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、X的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成C和E;
③工业上以A、空气和水为原料,通过催化氧化法制取E。
请回答以下问题:
(1)B的电子式为 ,A的结构式为 ,A分子的空间构型是
;
(2)写出②中涉及反应的化学方程式 ;
(3)由B反应生成1mol A放出的热量为46.2kJ,写出该反应的热化学方程式,并注明
反应条件 ;
(4)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出有关反应的化学方程式 。
18.汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的一种办法是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,并促使烃类充分燃烧及SO2的转化,下列说法中错误的是
A.CO与NO反应的化学方程式为2CO+2NO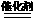 2CO2+N2
2CO2+N2
B.此方法的缺点是由于CO2的增多,会大大提高空气的酸度
C.为减少城市污染应开发新能源
D.汽车尾气中有两种气体会与血红蛋白结合而使人中毒
17.有三组物质:①NO2和Br2蒸气②C2H5CHO、C6H6、C6H5-NO2三种无色液体③CaC2、CuSO4(无水)、CaCO3、Na2SO4、干燥的碱石灰(含少量酚酞)五种固体,只用水就能区别开的是
A.① B.①② C.②③ D.①②③
16.空气和二氧化碳按体积5:1混合,将混合气体与足量的红热焦炭充分反应。设空气中氮气和氧气的体积比为4:1,不计其他成分,且体积都在同温、同压下测定的,则反应后的气体中一氧化碳的体积分数是
A.29% B.43% C.50% D.100%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com