
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
19ЃЎФГЙЄГЇгУC aSO4ЁЂH2OЁЂNH3ЁЂCO2жЦБИ(NH4)2SO4ЃЌЦфЙЄвеСїГЬШчЯТЃК
 ЁЁ
ЁЁ
ЁЁЁЁЁЁ ЯТСаЭЦЖЯВЛКЯРэЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎЭљМзжаЭЈCO2гаРћ(NH4)2SO4ЩњГЩ
ЁЁЁЁЁЁ BЃЎЩњдк1 mol(NH4)2SO4жСЩйЯћКФ2molNH3
ЁЁЁЁЁЁ CЃЎCO2ПЩБЛбЛЗЪЙгУ
ЁЁЁЁЁЁ DЃЎжБНгеєИЩТЫвКФмЕУЕНДПОЛ(NH4)2SO4
|
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
|
ЁЁЁЁЁЁ BЃЎЩњГЩЕФЧтЛЏЮяЗжзгМфОљПЩаЮГЩЧтМќ
ЁЁЁЁЁЁ CЃЎAгыCаЮГЩЕФвѕРызгПЩФмгаAC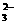 ЁЂA2C
ЁЂA2C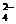
ЁЁЁЁЁЁ DЃЎAЁЂBЁЂCЁЂDЕФЕЅжЪГЃЮТЯТОљВЛЕМЕч
18ЃЎC8H18ОЖрВНСбЛЏЃЌзюКѓЭъШЋзЊЛЏЮЊC4H8ЁЂC3H6ЁЂC2H4ЁЂC2H6ЁЂCH4ЮхжжЦјЬхЛьКЯЮяЁЃИУЛьКЯЮяЕФЦНОљЯрЖдЗжзгжЪСППЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ30ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ28ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ40ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ38
17ЃЎЗжзгСПЮЊMЕФФГЮяжЪдкЪвЮТЯТЕФШмНтЖШЮЊSg/100gЫЎЃЌДЫЪБВтЕУБЅКЭШмвКЕФУмЖШЮЊdg/cm3ЁЃдђИУБЅКЭШмвКЕФЮяжЪЕФСПХЈЖШЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎ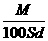 molЁЄL-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ
molЁЄL-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ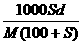 molЁЄL-1
molЁЄL-1
ЁЁЁЁЁЁ CЃЎ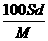 molЁЄL-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ
molЁЄL-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ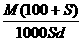 molЁЄL-1
molЁЄL-1
16ЃЎдкБъзМзДПіЯТЃЌНЋVLAЦјЬх(ФІЖћжЪСПЮЊMg/mol)Шмгк0.1LЫЎжаЃЌЫљЕУШмвКУмЖШЮЊdg/mLЃЌдђДЫШмвКЕФЮяжЪЕФСПХЈЖШЮЊ(ЁЁЁЁ )mol/LЁЃ
ЁЁЁЁЁЁ AЃЎ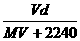 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ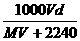 ЁЁЁЁЁЁ
ЁЁЁЁЁЁ
ЁЁЁЁЁЁ CЃЎ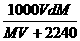 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ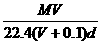
15ЃЎОнзюаТБЈЕРЃЌПЦбЇМвЗЂЯжСЫШчЯТЗДгІЃКO2+PtF6=O2(PtF6)ЃЌвбжЊO2(PtF6)ЮЊРызгЛЏКЯЮяЃЌЦфжаPtЮЊ+5МлЃЌЖдгкДЫЗДгІЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎдкДЫЗДгІжаЃЌO2ЪЧбѕЛЏМСЃЌPtF6ЪЧЛЙдМС
ЁЁЁЁЁЁ BЃЎO2(PtF6)жабѕдЊЫиЕФЛЏКЯМлЪЧ+1Мл
ЁЁЁЁЁЁ CЃЎO2(PtF6)жаВЛДцдкЙВМлМќ
ЁЁЁЁЁЁ DЃЎдкДЫЗДгІжаЃЌУПЩњГЩ1 mol O2(PtF6)ЃЌдђзЊвЦ1 molЕчзг
14ЃЎгУNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎГЃЮТГЃбЙЯТввШВЕФ1ЃЌ3-ЖЁЖўЯЉЛьКЯЦјagЃЌЦфжаC-HМќЕФЪ§ФПдМЮЊaNA/13
ЁЁЁЁЁЁ BЃЎЙЄвЕЩњВњСђЫсЪБЃЌдкНгДЅЪвФкУПГфШыNAИіSO2ПЩЭъШЋзЊЛЏЮЊ1 molSO3
ЁЁЁЁЁЁ CЃЎ1 molИЩБљОЇЬхжаКЌгаC=OМќЕФЪ§ФПЮЊ2NA
ЁЁЁЁЁЁ DЃЎ1 molCa(ClO)2жЛзїбѕЛЏМСЧвГфЗжЗДгІЪБЃЌзЊвЦЕФЕчзгЪ§вЛЖЈЮЊ2NA
13ЃЎЯТСаЫЕЗЈжаЃЌе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎдк100gЫЎРяЃЌзюЖрФмШмНт36gЪГбЮЃЌЫљвдЪГбЮЕФШмНтЖШЮЊ36g
ЁЁЁЁЁЁ BЃЎЫљгаЙЬЬхЮяжЪШмНтЖШЖМЫцзХЮТЖШЕФЩ§ИпЖјдіДѓ
ЁЁЁЁЁЁ CЃЎгаЙ§ЪЃШмжЪгыШмвКЙВДцЕФШмвКвЛЖЈЪЧИУЮТЖШЪБЕФБЅКЭШмвК
ЁЁЁЁЁЁ DЃЎ20ЁцЪБ100gЫЎРяШмНтСЫ30gЯѕЫсМиЃЌЫљвдЯѕЫсМиЕФШмНтЖШЪЧ30g
12ЃЎЯТСагаЙиЮяжЪЕФНсЙЙЛђаджЪЕФа№ЪіДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎгЩМЋадМќаЮГЩЕФЗжзгВЛвЛЖЈЪЧМЋадЗжзг
ЁЁЁЁЁЁ BЃЎЫЎЪЧвЛжжЗЧГЃЮШЖЈЕФЛЏКЯЮяЃЌетЪЧгЩгкЧтМќЫљжТ
ЁЁЁЁЁЁ CЃЎЪЏгЂЁЂЪГбЮЁЂН№ЪєФЦЁЂИЩБљЕФШлЕувРДЮНЕЕЭ
ЁЁЁЁЁЁ DЃЎЗжзгОЇЬхжавЛЖЈДцдкЗжзгМфзїгУСІЃЌПЩФмгаЙВМлМќ
11ЃЎНЋSO2ЭЈШыBaCl2ШмвКжСБЅКЭЃЌЮДМћГСЕэЩњГЩЃЌМЬајЭЈШыСэвЛжжЦјЬхЃЌШдЮоГСЕэЃЌдђЭЈШыЕФЦјЬхПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁЁЁ AЃЎCO2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎNH3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎNO2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎH2S
10ЃЎНЋМзЁЂввСНжжН№ЪєЕФаджЪЯрБШНЯЃЌвбжЊЂйМзИњH2OЗДгІБШввгыH2OЗДгІОчСвЃЛЂкМзЕЅжЪФмДгввЕФбЮШмвКжажУЛЛГіЕЅжЪввЃЛЂлМзЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяМюадБШввЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяМюадЧПЃЛЂмгыФГН№ЪєЗДгІЪБМздзгЕУЕчзгЪ§ФПБШввЕФЖрЃЛЂнМзЕЅжЪЕФШлЁЂЗаЕуБШввЕФЕЭЁЃФмЫЕУїМзЕФН№ЪєадБШввЧПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ ЁЁ)
ЁЁЁЁЁЁ AЃЎЂйЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлЂнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂйЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂйЂкЂлЂмЂн
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com