
题目列表(包括答案和解析)
14.某同学测定某一气体样品中CO的浓度:第一步,将2.00L气体样品通入盛有I2O5固体的反应管中,反应生成CO2和I2;第二步,用60.00mL 2.5×10-3mol·L-1的Na2S2O3吸收产生的I2(I2+2S2O32-==2I-+S4O62-);第三步,取上述反应后溶液体积的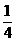 ,用标准溶液碘水(1.00×10-2mol·L-1)滴定过量的Na2S2O3,消耗碘水的体积为1.25mL,则样品中CO的浓度(mg·L-1)为( )
,用标准溶液碘水(1.00×10-2mol·L-1)滴定过量的Na2S2O3,消耗碘水的体积为1.25mL,则样品中CO的浓度(mg·L-1)为( )
A. 1.25×10-4 B. 3.5 C. 6.25×10-5 D. 1.75
13.某研究小组设计了如图所示的循环系统,来生产能解决能源危机的某种物质,其中所需的电能由太阳能光电池提供。有关叙述正确的是( )
A.该循环系统的目的是制I2
B.电解池A中离子反应方程式:H2+I2 2H++2I-
2H++2I-
C.光催化反应池中离子反应方程式为:2Fe2++I2 2Fe3++2I-
2Fe3++2I-
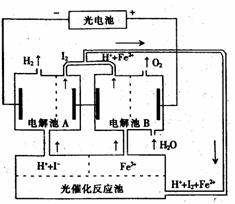 D.该系统中的Fe3+、O2、I-都是循环使用的物质
D.该系统中的Fe3+、O2、I-都是循环使用的物质
12.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
|
|
I |
II |
|
A |
少量CO2通和NaOH溶液中 |
过量CO2通入少量NaOH溶液中 |
|
B |
少量NaOH溶液滴入Al2(SO4)3溶液中 |
少量Al2(SO4)3溶液滴入浓氨水中 |
|
C |
0.1molCl2通入含0.2molFeBr2的溶液中 |
0.3mol Cl2通入含0.2mol FeBr2的溶液中 |
|
D |
过量BaCl2溶液与少量Na2SO4溶液相混合 |
少量Ba(NO3)2溶液与过量MgSO4溶液相混合 |
11.把NaHCO3和Na2O2的混合物放在密闭容器中加热,关于混合物加热前后与足量盐酸反应消耗盐酸的量,下列判断的是( )
A.加热前后一样多 B.加热前消耗的多
C.加热后消耗的多 D.当Na2O2适量时才会一样多
10.将0.2mol甲物质加入250mL 0.4mol·L-1的盐酸中,充分反应后,再加入0.1mol乙物质,在整个过程中,产生的H2在标准状况下的体积最多的是( )
|
|
A |
B |
C |
D |
|
甲 |
K |
K |
Na |
Al |
|
乙 |
Na |
Mg |
Al |
Mg |
9.粗碘中通常含有ICl和IBr,称为卤素互化物,其性质和卤素相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华。在粗碘中加入下列选项中的一种物质后,再进行升华可得到精碘,则应加入的物质的是( )
A.H2O B.Zn C.KI D.KCl
8.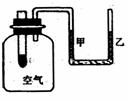 右图为某学生设计的一个实验装置,大试管中装有过氧化钠固体。现往大试管中加入水,下列说法中正确的是(
)
右图为某学生设计的一个实验装置,大试管中装有过氧化钠固体。现往大试管中加入水,下列说法中正确的是(
)
A.试管中发生了置换反应
B.一段时间后,看到“U”形管中的液面右边升高,左边下降
C.“贮存”在反应物中的总能量低于生成物的总能量
D.广口瓶中气体的分子在反应后增加
7.将标准状况下的某气体(摩尔质量为Mg·mol-1)溶于ag水中,所得到溶液的密度为bg·cm-3,物质的量浓度为c mol·L-1,则溶入水中的该气体的体积是( )
A.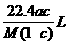 B.
B. 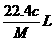 C.
C. 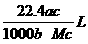 D.
D. 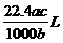
6.某同学用Na2CO3配制0.10mol·L-1Na2CO3(aq)的过程如下图所示:
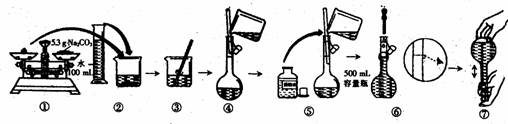
你认为该同学的错误有( )
A.1处 B.2处 C.3处 D.4处
5.某溶液中只含Na+、Al3+、Cl-、SO42-四种离子。已知Na+、Al3+、Cl-的个数比为3:2:1,则溶液中Al3+与SO42-的个数比为( )
A. 1:2 B. 1:4 C. 3:4 D. 3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com