
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
5£Æ“—÷™A°¢B°¢C°¢D°¢E «∫ÀµÁ∫…“¿¥Œ‘ˆ¥ÛµƒŒÂ÷÷∂Ã÷İ∆Ğ÷˜◊‘™Àÿ£¨‘≠◊”∞Îæ∂∞¥D°¢E°¢B°¢C°¢AµƒÀ≥–Ú“¿¥Œº–°£¨B°¢EÕ¨÷˜◊£¨A∫ÀƒĞŒŞ÷–◊”£¨œ¬¡–Õ∆∂œ’˝»∑µƒ «(°° )
A£ÆA°¢B°¢E“ª∂®≤ª‘ĞÕ¨“ª÷İ∆Ğ°°°°°°°°°°°° B£ÆDŒ™µĞ∂˛÷İ∆Ğ‘™Àÿ
C£ÆA°¢D≤ªø…ƒİ‘ĞÕ¨“ª÷˜◊°°°°°°°°°°°°°° D£Æ C°¢Dµƒµ•÷ ªØ∫œ“ª∂®–Œ≥…¿Î◊”ªØ∫œŒÔ
4£Æ. Ç(Sb)‘Ğ◊‘»ªΩÁ“ª∞„“‘¡ÚªØŒÔµƒ–Œ Ω¥Ê‘Ğ£¨Œ“π˙ǵƒ‘Ã≤ÿ¡ø’º ¿ΩÁµĞ“ª°£¥”¡ÚªØŒÔ÷–÷»°µ•÷ Ç“ª∞„ «œ»‘Ğ∏şŒ¬œ¬Ω´¡ÚªØŒÔ◊™ªØŒ™—ªØŒÔ£¨‘Ÿ”√úªπ‘≠£∫
°°°°°°°°°°°°°° 2Sb2S3+3O2+6Fe£ΩSb4O6+6FeS °°°≠°≠°≠°≠°≠°≠°≠°≠¢Ÿ
°°Sb4O6+6C£Ω4Sb+6CO°° °°°≠°≠°≠°≠°≠°≠°≠°≠°≠°≠°≠°≠¢Ğ
πÿ”Ğ∑¥”¶¢Ÿ°¢∑¥”¶¢ĞµƒÀµ∑®’˝»∑µƒ «(°° )
A£Æ°°∑¥”¶¢Ÿ¢Ğ÷–µƒ—ªØº¡∑÷± «Sb2S3°¢Sb4O6°°
B£Æ∑¥”¶¢Ÿ÷–√ø…˙≥…3 mol FeS ±£¨π≤◊™“∆6 molµÁ◊”
C£Æ∑¥”¶¢ĞÀµ√˜∏şŒ¬œ¬Sbµƒªπ‘≠–‘±»C«ø
D£Æ∑¥”¶¢Ÿ÷–FeS£¨º» «—ªØ≤˙ŒÔ”÷ «ªπ‘≠≤˙ŒÔ
3£Æ»œ ∂∑¥”¶Ãº˛∂‘ªØ—ß∑¥”¶µƒ”∞œÏ£¨∂‘—ß∫√ªØ—ßæş”–÷ÿ“™“‚“°£œ¬¡–Àµ∑®’˝»∑µƒ «(°° )
A£Æµ»Ãª˝µƒº◊ÕȔά»∆¯‘Ğπ‚’’Ãº˛œ¬£¨“ª∂®÷ª…˙≥…“ª¬»º◊ÕÈ∫Õ¬»ªØ«‚
B£Æƒ∆‘Ğ≥®øĞ»ı∆˜÷–≥§∆Ğ¥Ê∑≈ªÚ‘Ğø’∆¯÷–»º…’µƒ≤˙ŒÔ“ª∂® «Na2O2
C£Æ»İ“∫÷–—Œ”ΗŒµƒ∏¥∑÷Ω‚∑¥”¶£¨“ª∂®≤ªª·”–∆¯ÃÂ≤˙…˙
D£ÆœÚ±Ω∑”ƒ∆»İ“∫÷–Õ®»Î…Ÿ¡øCO2ªÚπ˝¡øCO2£¨≤˙ŒÔ“ª∂®∫¨”–NaHCO3
2£Æ∫∫¥˙∆˜ŒÔ…œµƒ—’¡œ°∞∫∫◊œ°±÷¡ΩÒ…–√ª”–∑¢œ÷∆‰◊‘»ª¥Ê‘еƒº«‘ÿ°£20 ¿ºÕ80ƒÍ¥˙ø∆—ߺ“Ω¯––≥¨µº≤ƒ¡œ—–æø ±£¨≈º»ª∑¢œ÷∆‰≥…∑÷Œ™◊œ…´µƒπËÀ·Õ≠±µ(ªØ—ß Ω£∫BaCuSi2Ox£¨CuŒ™+2ºğ)£¨œ¬¡–”–πÿ°∞∫∫◊œ°±µƒÀµ∑®÷–≤ª’˝»∑ «(°° )
A£Æ”√—Œµƒ–Œ Ω±Ì æ£∫BaSiO3°§CuSiO3°°°°°°°°°° °°°°°°B£Æ“◊»İ”Ğ«øÀ·°¢«øºÓ
C£Æ”√—ªØŒÔ–Œ Ω±Ì æ£∫BaO°§CuO°§2SiO2°°°°°°°°°°°° D£Æ–‘÷ Œ»∂®£¨≤ª“◊Õ …´
1£Æ«Â‘∂£¨…Ω«‡ÀÆ–„°¢æ∞…´“À»À°£œ¬¡–查Î≤ª¿˚”Ы‘∂ºÃ–¯±£≥÷¡º∫√ª∑æ≥µƒ «(°° )
A£ÆÕ∆π„ π”√ô—كݰ¢∑Áƒİµ»Ω‡æªƒİ‘¥£¨º…Ÿ√∫∆¯°¢“∫ªØ∆¯µƒ π”√¡ø
B£Æ∑÷¿‡ªÿ ’¿¨ª¯£¨≥‰∑÷¿˚”√‘Ÿ…˙◊ ‘¥
C£Æπƒ¿¯ –√Òπ∫÷√∫Õ π”√∆˚≥µ£¨º”øÏ≥« –ΩªÕ®œ÷¥˙ªØ
D£ÆÕ∆π„ π”√ø…ΩµΩ‚Àİ¡œ£¨œ˚≥˝∞◊…´Œğ»æ
113£Æ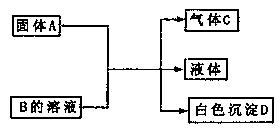 A°¢B°¢C°¢D°¢æ˘Œ™÷–—ߪؗß≥£º˚µƒŒÔ÷ £¨À¸√«º‰µƒ∑¥”¶πÿœµ»Áœ¬ÕºÀ˘ æ°£
A°¢B°¢C°¢D°¢æ˘Œ™÷–—ߪؗß≥£º˚µƒŒÔ÷ £¨À¸√«º‰µƒ∑¥”¶πÿœµ»Áœ¬ÕºÀ˘ æ°£
°° (1)»ÙA «ø…»İ–‘«øºÓ£¨B «’˝—Œ£¨D≤ª»İ”Ğœ°œÀ·£¨‘ÚBµƒªØ—ß Ω °°°°°°°°°°°°°£”–πÿ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
°° (2)»ÙB «’˝—Œ£¨Dº»ø…»İ”Ğ—ŒÀ·”÷ø…»İ”ĞNaOH»İ“∫°£
°°°°°°°° ¢ŸA «NaHCO3 ±£¨∏√∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫°°°°°°°°°°°°°°°°°°°°°°°° °°°£
°°°°°°°° ¢ĞA «“ª÷÷µ≠ª∆…´πÃ㨫“A”ÎB“‘ŒÔ÷ µƒ¡ø÷Ʊ»Œ™2£∫1œ‡ªÏ∫œ ±£¨Õ∆÷™BµƒªØ—ß ΩŒ™°°°°°°°° °°°£
°° (3)»ÙA «ÃºªØ∏∆(CaC2)£¨A”ÎBµƒ»İ“∫∑¥”¶ ±÷ª…˙≥…∆¯ÃÂC°¢CaCO3∫ÕÀÆ£ªCµƒ»º…’»»Œ™1300kJ°§mol£≠1£¨‘ÚBµƒªØ—ß ΩŒ™°°°°°°°° °°£ªC»º…’µƒ»»ªØ—ß∑Ω≥Ã ΩŒ™°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
112£ÆA°¢B°¢C°¢Dæ˘Œ™∂Ã÷İ∆Ğ÷˜◊‘™Àÿ£¨A°¢C°¢D‘Ğ≤ªÕ¨÷İ∆Ğ£¨A∫ÕCÕ¨÷˜◊£¨B°¢CÕ¨÷İ∆Ğ£¨A°¢B°¢C»˝÷÷‘™Àÿµƒ‘≠◊”–Ú ˝÷Æ∫ÕŒ™37£¨«“B‘™Àÿµƒ◊ÓÕ‚≤„µÁ◊” ˝”Î∆‰µÁ◊”≤„ ˝œ‡Õ¨£¨‘Ú£∫
°° (1)D‘™Àÿµƒ√˚≥∆Œ™°°°°°°°°°°°° °£
°° (2)–¥≥ˆ‘™ÀÿA°¢D–Œ≥…µƒªØ∫œŒÔD2AµƒµÁ◊” Ω°°°°°°°°°°°°°° £¨∆‰»ğµ„±»D2Cµƒ»ğµ„°°°°°° (”√°∞∏ş°±ªÚ°∞µÕ°±ÃÓ–¥)£¨¿Ì”… «°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (3)A°¢B°¢C»˝÷÷‘™ÀÿÀ˘–Œ≥…µƒ≥£º˚ªØ∫œŒÔ»İ”ĞÀÆ≥ À·–‘£¨”√¿Î◊”∑Ω≥Ã Ω±Ì æ∆‰‘≠“Ú°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
°° (4)A°¢B°¢C°¢DÀƒ÷÷‘™Àÿµƒ‘≠◊”∞Îæ∂¥”–°µΩ¥ÛµƒÀ≥–ÚŒ™(”√‘™Àÿ∑˚∫≈±Ì æ)°°°°°°
°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°
111£Æ A£ÆB£ÆC£ÆD£ÆE°¢F «÷–—ߪؗß÷–≥£º˚µƒ6÷÷ŒÔ÷ £¨À¸√«‘Ğ“ª∂®Ãº˛œ¬ø…∑¢…˙»Áœ¬∑¥”¶£∫ ¢ŸA+B C+D°° ¢ĞB+E
C+D°° ¢ĞB+E D+F°°°°
¢ğC+E
D+F°°°°
¢ğC+E A+F
A+F
°° (1)»ÙA°¢D°¢EŒ™¬±Àÿµ•÷ £¨∑¥”¶¢Ÿ°¢¢Ğ°¢¢ğæ˘Œ™‘ĞÀƻݓ∫÷–Ω¯––µƒ÷√ªª∑¥”¶£¨‘ÚA°¢D°¢E”Ϋ‚∆¯ªØ∫œ”…ƒ—µΩ“◊µƒÀ≥–ÚŒ™____________£¨A∏˙B∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «__________________________°£
°° (2)≥£Œ¬œ¬£¨»ÙD «“∫Ã¨Ω Ù£¨A «∫Ï…´πÃõ•÷ £¨∑¥”¶¢Ÿ°¢¢Ğ°¢¢ğ“≤∂º‘ĞÀƻݓ∫÷–Ω¯––£¨E «∂Ã÷İ∆Ğ‘™Àÿµƒµ•÷ £¨‘ÚEø…ƒİ «_______________£¨A∏˙B∑¥”¶¿Î◊”∑Ω≥Ã Ω «_____ __________________°£
°° (3)»ÙA°¢D°¢E «µ•÷ £¨C «”–¥≈–‘µƒπÃã¨F «ŒŞ…´°¢ŒŞŒ∂°¢”–∂浃∆¯Ã£¨‘ÚA‘Ğ÷İ∆бÌ÷–µƒŒª÷√ «_____________°°°° £¨A∫ÕB∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «_____°°°° ____£¨B∫ÕE∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «_°°°° ________________
110£Æ£Æ“‘œ¬∏˜µ•÷ ∫ÕªØ∫œŒÔ÷ƺ‰¥Ê‘Ğœ¬¡–◊™ªØπÿœµ(∏˜µ•÷ ∫ÕªØ∫œŒÔ÷–À˘∫¨‘™Àÿæ˘Œ™∂Ã÷İ∆Ğ‘™Àÿ)£∫
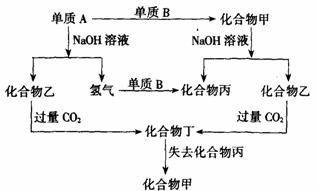
°° (1) ‘»∑∂®µ•÷ A∫ÕBµƒªØ—ß Ω£∫A________£¨B________°£
°° (2)–¥≥ˆªØ∫œŒÔº◊”ÎNaOH»İ“∫∑¥”¶µƒªØ—ß∑Ω≥à Ω________________________________°£
°° (3)–¥≥ˆªØ∫œŒÔ““◊™ªØŒ™ªØ∫œŒÔ∂°µƒ¿Î◊”∑Ω≥à Ω________________________________°£
109£Æ(12∑÷)∫£ÀÆ÷–∫¨”–∑·∏ªµƒªØ—ß‘™Àÿ£¨œ¬√Ê «ƒ≥ªØπ§≥ߥ”∫£ÀÆ÷–÷»°NaCl°¢Mg(“‘MgCl2–Œ Ω¥Ê‘Ğ)∫ÕBr2(“‘NaBrµƒ–Œ Ω¥Ê‘Ğ)º∞◊ğ∫œ¿˚”√µƒ…˙≤˙¡˜≥úÚÕº£∫
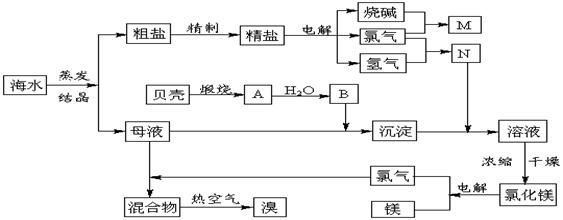
«Îªÿ¥£∫
(1)‘Ğ¥÷—Œ÷–∫¨”–Ca2+°¢Mg2+°¢SO42£≠µ»‘”÷ £¨æ´÷∆ ±À˘”√µƒ ‘º¡Œ™£∫
A£Æ—ŒÀ·°°°° B£Æ¬»ªØ±µ»İ“∫°°°°°° C£Æ«‚—ªØƒ∆»İ“∫°°°°°° D£ÆúÀ·ƒ∆»İ“∫°£
‘Úº”»Î ‘º¡µƒÀ≥–Ú «(ÃÓ±‡∫≈)_____°°°°°°°°°° _°£
(2)Mg(OH)2÷–º”»Î—ŒÀ·∫Û£¨“™ªÒµ√MgCl2°§6H2Oæß㨖˓™Ω¯––µƒ µ—È≤Ÿ◊˜“¿¥ŒŒ™____°£
A£Æ’Ù¡Û°°°°°° B£Æ◊∆…’°°°° C£Æπ˝¬À°°°°°° D£Æ’Ù∑¢°°°°°° E£Æ¿‰»¥Ω·æß
(3)¿˚”√MgCl2°§6H2Oø…÷∆µ√ŒŞÀƬ»ªØ√棨”¶≤…»°µƒ¥Î © «°°°°°°°°°°°°°°°°°°°°°° °£
(4)ƒø«∞𧓵…œ÷˜“™≤…”√¿Î◊”Ωªªªƒ§∑®µÁΩ‚±•∫Õ ≥—ŒÀÆ£¨œ¬¡–πÿ”Ğ¿Î◊”Ωªªªƒ§µÁΩ‚≤𵃖 ˆ¥ÌŒÛµƒ «°°°°°° °£
 A£Ææ´÷∆±•∫Õ ≥—ŒÀÆΩ¯»Î—Ùº´ “
A£Ææ´÷∆±•∫Õ ≥—ŒÀÆΩ¯»Î—Ùº´ “
B£Æ¥øÀÆ(º”…Ÿ¡øNaOH)Ω¯»Î“º´ “
C£Æ“º´≤˙ŒÔŒ™«‚—ªØƒ∆∫Õ«‚∆¯
D£ÆµÁΩ‚≤𵃗ٺ´”√Ω ÙÃ˙Õ¯÷∆≥…
(5)–¥≥ˆµÁΩ‚±•∫ÕNaCl»İ“∫µƒ¿Î◊”∑¥”¶∑Ω≥Ã Ω£∫
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
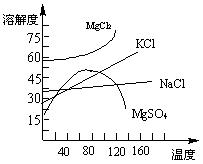
(6)ƒ∏“∫÷–≥£∫¨”–MgCl2°¢NaCl°¢MgSO4°¢KClµ»£¨ø…Ω¯“ª≤Ωº”π§÷∆µ√“ª–©÷ÿ“™µƒ≤˙∆∑°£»ÙΩ´ƒ∏“∫º”»»…˝Œ¬µΩ60°Ê“‘…œ£¨ÀÊ◊≈ÀÆ∑÷µƒ’Ù∑¢£¨ª·÷Ω•Œˆ≥ˆæß㨥Àæßõƒ÷˜“™≥…∑÷ «_______
___________£ªπ˝¬À…œ ˆæßÃÂ∫Û£¨Ω´¬À“∫ΩµŒ¬µΩ30°Ê“‘œ¬£¨”÷÷Ω•Œˆ≥ˆæß㨔√“ª∂®¡øµƒ¿‰ÀÆœ¥µ”∏√æßã¨◊Ó∫Ûø…µ√µΩ±»Ωœ¥ø檵ƒ________æßð£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒŞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com