
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
1£®¹ŲÓŚĒā¼ü£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””)
A£®·Ö×Ó¼äŠĪ³ÉµÄĒā¼üŹ¹ĪļÖŹµÄČŪµćŗĶ·ŠµćÉżøß”” B£®±łÖŠ“ęŌŚĒā¼ü£¬Ė®ÖŠ²»“ęŌŚĒā¼ü
C£®ĆæŅ»øöĖ®·Ö×ÓÄŚŗ¬ÓŠĮ½øöĒā¼ü”” ””””D£®H2OŹĒŅ»ÖÖ·Ē³£ĪČ¶ØµÄ»ÆŗĻĪļ£¬ÕāŹĒÓÉÓŚĒā¼üĖłÖĀ
11£®(10·Ö)¶ĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢D”£AŌŖĖŲµÄŌ×Ó×īĶā²ćµē×ÓÅŲ¼ĪŖns1£¬BŌŖĖŲµÄŌ×Ó¼Ūµē×ÓÅŲ¼ĪŖns2np2£¬CŌŖĖŲµÄ×īĶā²ćµē×ÓŹżŹĒĘäµē×Ó²ćŹżµÄ3±¶£¬DŌŖĖŲŌ×ÓµÄMµē×Ó²ćµÄPŃĒ²ćÖŠÓŠ3øöĪ“³É¶Ōµē×Ó”£
(1)CŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ”””””””””””””” £¬ČōAĪŖ·Ē½šŹōŌŖĖŲ£¬Ōņ°“Ō×Ó¹ģµĄµÄÖŲµü·½Ź½£¬AÓėCŠĪ³ÉµÄ»ÆŗĻĪļÖŠµÄ¹²¼Ū¼üŹōÓŚ”””””””””””””” ¼ü(Ģī”°¦Ņ”±»ņ”°¦Š”±)”£
(2)µ±n=2Ź±£¬BĪ»ÓŚŌŖĖŲÖÜĘŚ±ķµÄµŚ”””””” ÖÜĘŚ”””””” ×壬BC2ŹōÓŚ”””””””””” ·Ö×Ó(Ģī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±)”£µ±n=3Ź±£¬BÓėCŠĪ³ÉµÄ¾§ĢåŹōÓŚ”””””””””””” ¾§Ģ唣
(3)ČōAŌŖĖŲµÄŌ×Ó×īĶā²ćµē×ÓÅŲ¼ĪŖ2s1£¬BŌŖĖŲµÄŌ×Ó¼Ūµē×ÓÅŲ¼ĪŖ3s23p2£¬ A”¢B”¢C”¢DĖÄÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņŹĒ”””””””””””””””” (ÓĆŌŖĖŲ·ūŗűķŹ¾)”£
10£®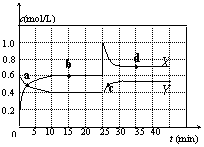
 (10·Ö)ŅŃÖŖNO2ŗĶN2O4æÉŅŌĻą»„×Ŗ»Æ£ŗ2NO2(g)””””
N2O4(g); ”÷H<0”£ĻÖ½«Ņ»¶ØĮæNO2ŗĶN2O4µÄ»ģŗĻĘųĢåĶØČėŅ»¶ØĢå»żĪŖ2LµÄŗćĪĀĆܱղ£Į§ČŻĘ÷ÖŠ£¬·“Ó¦ĪļÅضČĖꏱ¼ä±ä»Æ¹ŲĻµČēĶ¼”£
(10·Ö)ŅŃÖŖNO2ŗĶN2O4æÉŅŌĻą»„×Ŗ»Æ£ŗ2NO2(g)””””
N2O4(g); ”÷H<0”£ĻÖ½«Ņ»¶ØĮæNO2ŗĶN2O4µÄ»ģŗĻĘųĢåĶØČėŅ»¶ØĢå»żĪŖ2LµÄŗćĪĀĆܱղ£Į§ČŻĘ÷ÖŠ£¬·“Ó¦ĪļÅضČĖꏱ¼ä±ä»Æ¹ŲĻµČēĶ¼”£
(1)Ķ¼ÖŠ¹²ÓŠĮ½ĢõĒśĻßXŗĶY£¬ĘäÖŠĒśĻß”””” ±ķŹ¾NO2
ÅضČĖꏱ¼äµÄ±ä»Æ£»a”¢b”¢c”¢dĖÄøöµćÖŠ£¬±ķŹ¾»Æѧ
·“Ó¦“¦ÓŚĘ½ŗāדĢ¬µÄµćŹĒ”””””””””””””””””””””” ”£
(2)¢Ł Ē°10minÄŚÓĆNO2±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹ
v(NO2)=”””””””” mol/(L”¤min)
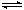 ¢Ś 15minŹ±£¬·“Ó¦2NO2(g)”””” N2O4(g)ŌŚbµćµÄÅØ¶Č”” Ę½ŗā³£ŹżK(b)=””””””””””””””
¢Ś 15minŹ±£¬·“Ó¦2NO2(g)”””” N2O4(g)ŌŚbµćµÄÅØ¶Č”” Ę½ŗā³£ŹżK(b)=””””””””””””””
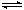 ¢Ū 35minŹ±£¬·“Ó¦2NO2(g)”””” N2O4(g)ŌŚdµćµÄÅضČĘ½ŗā³£ŹżK(d)”””””” K(b)
¢Ū 35minŹ±£¬·“Ó¦2NO2(g)”””” N2O4(g)ŌŚdµćµÄÅضČĘ½ŗā³£ŹżK(d)”””””” K(b)
”” (Ģī”°>”±”¢”°=”±»ņ”°<”±)
(3)¢Ł ČōŅŖ“ļµ½Ź¹NO2(s)µÄ°Ł·Öŗ¬ĮæÓėdµćĻąĶ¬µÄ»ÆŃ§Ę½ŗāדĢ¬£¬ŌŚ25minŹ±»¹æÉŅŌ²ÉČ”µÄ“ėŹ©ŹĒ”””””””””””””””””””””””””””””””””””””” ”£
A”¢¼ÓČė“߻ƼĮ”””” B”¢ĖõŠ”ČŻĘ÷Ģå»ż”””” C”¢ÉżøßĪĀ¶Č”””” D”¢¼ÓČėŅ»¶ØĮæµÄN2O4
”” ¢Ś ČōŌŚ35minŹ±£¬±£³ÖĪĀ¶Č²»±ä£¬æģĖŁĖõŠ”²£Į§ČŻĘ÷µÄĢå»żÖĮ1L£¬ĘųĢåµÄŃÕÉ«±ä»Æ¹ż³ĢŹĒ”””””””””””””””””””””””””””””””””””””” ”£
9£®(12·Ö)ÓĆŹ¾ŅāĶ¼ÖŠµÄ¼ņŅ××°ÖĆæÉŅŌ½ųŠŠĘųĢåµÄ·¢ÉśŗĶŹÕ¼Æ”£
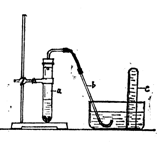 (1)ŹµŃéĒ°¼ģ²é×°ÖƵÄĘųĆÜŠŌµÄ·½·ØŹĒ£ŗ””””””””””””””””””””””””””””””””””””””””””
ӣ
(1)ŹµŃéĒ°¼ģ²é×°ÖƵÄĘųĆÜŠŌµÄ·½·ØŹĒ£ŗ””””””””””””””””””””””””””””””””””””””””””
ӣ
(2)°ĪæŖŹŌ¹ÜµÄĻšĘ¤Čū£¬¼ÓČė10 mL 6 mol/LĻ”ĻõĖįŗĶ 1 g ±”Ķʬ£¬
½«“ųÓŠµ¼¹ÜµÄĻšĘ¤ČūČū½ōŹŌ¹ÜæŚ”£·“Ó¦æŖŹ¼Ź±ĖŁ¶Č»ŗĀż£¬Ėę×Å·“Ó¦µÄ½ųŠŠÖš½„¼Óæģ£¬
ŌŚŹŌ¹ÜaÖŠĖł·¢ÉśµÄ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢Ł ””””””””””””””””””””””””””””””””””””””””””£¬
¢Ś”””””””””””””””””””””””””””””””””””””””” ”””£
(3)“Ó·“Ó¦æŖŹ¼µ½·“Ó¦½įŹų£¬Ō¤ĘŚŌŚŹŌ¹ÜaÖŠæɹŪ²ģµ½ĻóµÄĻÖĻóŹĒ
(ŅĄ“ĪŠ“³öÓĆŠņŗűźĆ÷)£ŗ””””””””””””””””””””””””””””””””””””””””””””””””””
”””””””””””””””””””””” ””””””””””””””””””””””””””””””””””””””””””””””””””
(4)ŌŚ·“Ó¦æŖŹ¼Ź±£¬æɹŪ²ģµ½µ¼¹ÜbÖŠµÄĖ®ĆęĻČŃŲµ¼¹ÜbĀżĀżÉĻÉżµ½Ņ»¶Øøß¶Č£¬“ĖŗóÓÖ»ŲĀä£¬Č»ŗóÓŠĘųÅŻ“Ó¹ÜæŚĆ°³ö”£·“Ó¦æŖŹ¼Ź±µ¼¹ÜÖŠĖ®ĆęÉĻÉżµÄŌŅņŹĒ£ŗ”””””””””””” ””””””””
”””””” ”””””””””””””””””””””””””””””””””””””””””””£
(5)ŹŌ¹ÜcŹÕ¼ÆĀśĘųĢåŗó£¬Ä³Ķ¬Ń§ÓĆĻšĘ¤Čū¶Ā×”¹ÜæŚ£¬Č”³öĖ®²Ū”£½«¹ÜæŚ³ÆÉĻ£¬°ĪæŖĻš½ŗČū£¬Ę¬æĢŗó£¬ŌŁ“Ī¶Ā×”¹ÜæŚ£¬½«ŹŌ¹ÜÓÖŌŁµ¹ÖĆÓŚĖ®²ŪÖŠ£¬°ĪæŖĻšĘ¤Čū”£“ĖŹ±¹Ū²ģµ½µÄĻÖĻóŹĒ£ŗ””””””””””””
”””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
8£®ŅŃÖŖ·“Ó¦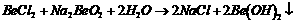 ÄÜĶźČ«½ųŠŠ£¬ŌņĻĀĮŠĶʶĻÖŠ£¬ÕżČ·µÄŹĒ””””””””””””””””””””””””””””””””””””””””””
ÄÜĶźČ«½ųŠŠ£¬ŌņĻĀĮŠĶʶĻÖŠ£¬ÕżČ·µÄŹĒ””””””””””””””””””””””””””””””””””””””””””
”””” A. 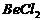 ČÜŅŗµÄpH£¼7£¬½«ĘäÕōøɲ¢×ĘÉÕŗó£¬µĆµ½µÄ²ŠĮōĪļæÉÄÜĪŖBeO
ČÜŅŗµÄpH£¼7£¬½«ĘäÕōøɲ¢×ĘÉÕŗó£¬µĆµ½µÄ²ŠĮōĪļæÉÄÜĪŖBeO
”””” B. 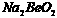 ČÜŅŗµÄpH£¾7£¬½«ĘäÕōøɲ¢×ĘÉÕŗó£¬µĆµ½µÄ²ŠĮōĪļæÉÄÜĪŖBeO
ČÜŅŗµÄpH£¾7£¬½«ĘäÕōøɲ¢×ĘÉÕŗó£¬µĆµ½µÄ²ŠĮōĪļæÉÄÜĪŖBeO
”””” C. 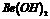 ¼ČÄÜČÜÓŚŃĪĖįÓÖÄÜČÜÓŚÉÕ¼īČÜŅŗ
¼ČÄÜČÜÓŚŃĪĖįÓÖÄÜČÜÓŚÉÕ¼īČÜŅŗ
”””” D. 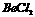 Ė®ČÜŅŗµÄµ¼µēŠŌĒ棬Ņņ“Ė
Ė®ČÜŅŗµÄµ¼µēŠŌĒ棬Ņņ“Ė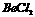 Ņ»¶ØŹĒĄė×Ó»ÆŗĻĪļ
Ņ»¶ØŹĒĄė×Ó»ÆŗĻĪļ
7£®ĪļÖŹµÄĮæÅضČø÷ĪŖ0.1mol”¤L£1µÄCH3COOHŗĶCH3COONaČÜŅŗµČĢå»ż»ģŗĻŗó£¬ČÜŅŗ³ŹĖįŠŌ”£ĻĀĮŠ¹ŲĻµŹ½ÕżČ·µÄŹĒ
A£®c(Na+)+c(H+)£½c(CH3COO£)+c(OH£)”” B£®c(CH3COO£)+c(CH3COOH)£½0.2mol”¤L£1
C£®c(CH3COO£)£¾c(Na+)£¾c(H+)£¾c(OH£)”” D£®c(Na+)£¾c(CH3COO£)£¾c(H+)£¾c(OH£)
6£®a mol FeSÓėb mol FeOĶ¶Čėµ½V L”¢C mol•L£1µÄĻõĖįČÜŅŗÖŠ³ä·Ö·“Ó¦£¬²śÉśNOĘųĢ壬ĖłµĆ³ĪĒåČÜŅŗµÄ³É·ÖæÉæ“×÷ŹĒFe(NO3)3”¢H2SO4µÄ»ģŗĻŅŗ£¬Ōņ·“Ó¦ÖŠĪ“±»»¹ŌµÄĻõĖįæÉÄÜĪŖA£®(a+b)”Į63g”””””” B£®(a+b)”Į189g”””””” C£®(a+b)mol””””””””
D£®(CV£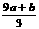 )mol
)mol
5£®ĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ””””””””””””””””””””””””””””
A£®ŌŚNaAlO2ČÜŅŗÖŠ£¬HSO3£(H2SO3µÄµēĄė³£ŹżK1£½1.5”Į10-2£»K2£½1.0”Į10-7)²»ÄÜ“óĮæ“ęŌŚ
B£®ŌŚ0.1mol”¤L-1µÄĒāäåĖįÖŠ¼ÓČėŹŹĮæµÄÕōĮóĖ®£¬ČÜŅŗµÄc(H+)¼õŠ”
C£®ŌŚÓÉĖ®µēĄė³öµÄc(OH-)£½1”Į10-12mol”¤L-1µÄČÜŅŗÖŠ£¬Al3+²»æÉÄÜ“óĮæ“ęŌŚ
D£®ŹŅĪĀĻĀpH£½6µÄĖįŠŌČÜŅŗÖŠ£¬æÉÄÜ“ęŌŚNH3”¤H2O·Ö×Ó
4£®Ä³ČÜŅŗæÉÄÜŗ¬ÓŠK+”¢Ag+”¢A13+”¢AlO2£”¢S2£”¢CO32£”¢SO32£”¢NO3£µČĄė×ÓÖŠµÄŹżÖÖ”£Ļņ“ĖČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖį£¬ÓŠĒ³»ĘÉ«³ĮµķŗĶĘųĢå³öĻÖ£¬“ĖČÜŅŗµÄŃęÉ«·“Ó¦ĪŖ×ĻÉ«(Ķø¹żĄ¶É«īܲ£Į§)”£øł¾ŻŅŌÉĻŹµŃéĻÖĻó£¬ĻĀĮŠ½įĀŪÖŠ“ķĪóµÄŹĒ
A£®“ĖČÜŅŗÖŠŅ»¶ØÓŠS2£”¢SO32£”¢K+”””””” B£®“ĖČÜŅŗÖŠæÉÄÜÓŠAlO2£”¢CO32£
C£®“ĖČÜŅŗÖŠŅ»¶ØƻӊAg+”¢A13+”””””””””” D£®“ĖČÜŅŗÖŠæÉÄÜÓŠS2£”¢NO3£
3£®ĻĀĮŠ±ķŹöÕżČ·µÄŹĒ””””””””””””””””””””””””””””””””””””””””””””””””””
A£®ČĖŌģøÕÓńČŪµćŗÜøߣ¬æÉÓĆ×÷øß¼¶ÄĶ»š²ÄĮĻ£¬Ö÷ŅŖ³É·ÖŹĒSiO2
B£®»Æѧ¼Ņ²ÉÓĆĀźč§ŃŠ²§Ä¦²Į¹ĢĢå·“Ó¦Īļ½ųŠŠĪŽČܼĮŗĻ³É£¬Āźč§µÄÖ÷ŅŖ³É·ÖŹĒAl2O3
C£®ĢįĒ°½Ø³ÉµÄČżĻæ“ó°ÓŹ¹ÓĆĮĖ“óĮæĖ®Äą£¬Ė®ÄąŹĒ¹čĖįŃĪ²ÄĮĻ
D£®ÓĆÓŚĻÖ“śĶØѶµÄ¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ³É·ÖŹĒøß“æ¶ČµÄ¹č
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com