
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
10.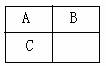 A°¢B°¢C∂Ã÷Ð∆⁄‘™Àÿ‘⁄÷Ð∆⁄±Ì÷–µƒŒª÷√»ÁÕºÀ˘ 棨“—÷™A°¢Cø…∑÷±”ÎB–Œ≥…ªØ∫œŒÔx∫Õy£¨A”ÎBµƒ÷ ◊” ˝÷Æ∫ÕŒ™Cµƒ÷ ◊” ˝£¨œ÷”–“‘œ¬Àµ∑®£¨∆‰÷–≈–∂œ’˝»∑µƒ◊È∫œ «( )°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
A°¢B°¢C∂Ã÷Ð∆⁄‘™Àÿ‘⁄÷Ð∆⁄±Ì÷–µƒŒª÷√»ÁÕºÀ˘ 棨“—÷™A°¢Cø…∑÷±”ÎB–Œ≥…ªØ∫œŒÔx∫Õy£¨A”ÎBµƒ÷ ◊” ˝÷Æ∫ÕŒ™Cµƒ÷ ◊” ˝£¨œ÷”–“‘œ¬Àµ∑®£¨∆‰÷–≈–∂œ’˝»∑µƒ◊È∫œ «( )°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
¢Ÿ°°°° B”ÎCæ˘¥Ê‘⁄Õ¨Àÿ“Ï–ŒÃ°° ¢⁄xµƒ÷÷¿ý±»yµƒ∂ý
°°¢€≥£Œ¬œ¬£¨B«‚ªØŒÔ÷–ŒÞH+
¢ÐCµƒ◊Ó∏þº€—ıªØŒÔ∂‘”¶Àƪ،ԃДÎAµƒ«‚ªØŒÔ–Œ≥…»˝÷÷—Œ
A.¢Ÿ¢⁄¢€¢Ð°°°°°° B.¢⁄¢€°°°° C.¢Ÿ¢⁄¢Ð°°°° D .¢Ÿ¢Ð
9.“—÷™ø…ƒÊ∑¥”¶2NO2(g)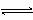 N2O4(g)£ª°˜H£º0£¨‘⁄“ª∂®Ãıº˛œ¬£¨∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨‘Ÿ≤…»°“‘œ¬∏ƒ±‰£¨‘Ÿ¥Œ¥ÔµΩ∆Ω∫‚∫Û£¨»ð∆˜÷–∆¯Ã—’…´º”…Óµƒ «(°° )
N2O4(g)£ª°˜H£º0£¨‘⁄“ª∂®Ãıº˛œ¬£¨∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨‘Ÿ≤…»°“‘œ¬∏ƒ±‰£¨‘Ÿ¥Œ¥ÔµΩ∆Ω∫‚∫Û£¨»ð∆˜÷–∆¯Ã—’…´º”…Óµƒ «(°° )
¢Ÿºı–°»ð∆˜Ãª˝°° ¢⁄…˝∏þŒ¬∂»°° ¢€∂®»ðœ¬≥‰»Î∆¯ÃÂN2O4°° ¢Ð∂®—πœ¬≥‰»ÎNO2∆¯ÃÂ
°° A.¢Ÿ¢⁄¢€¢Ð°°°° B.¢Ÿ¢⁄¢€°° C.¢Ÿ¢⁄°° D.¢Ÿ¢€
8.PH=3µƒ¡Ω÷÷À·»Ð“∫A°¢B£¨∑÷±”Î◊„¡øµƒ–ø∑¥”¶£¨À·A±»À·B≤˙…˙µƒ«‚∆¯µƒ¡ø∂ý£¨œ¬¡–πÿ”⁄A°¢BÀ·–‘«ø»ı≈–∂œ’˝»∑µƒ «(°° )
A.AµƒÀ·–‘£æBµƒÀ·–‘°°°°°°°°°°°° B. AµƒÀ·–‘£ºBµƒÀ·–‘
C. AµƒÀ·–‘”ÎBµƒÀ·–‘“ª—˘«ø°°°°°° D.ŒÞ∑®≈–∂œA°¢BÀ·–‘µƒœý∂‘«ø»ı
7.µ⁄»˝÷Ð∆⁄‘™ÀÿX£¨À¸µƒ‘≠◊”∫ÀÕ‚◊ÓÕ‚≤„ µœ÷8µÁ◊”Œ»∂®Ω·ππÀ˘–˵ƒµÁ◊” ˝–°”⁄¥ŒÕ‚≤„∫Õ◊Óƒ⁄≤„µƒµÁ◊” ˝÷Æ≤Ó£¨«“µ»”⁄◊Óƒ⁄≤„µÁ◊” ˝µƒ’˚ ˝±∂°£œ¬¡–Àµ∑®’˝»∑µƒ «
A£ÆX‘™Àÿ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،ԓª∂® ««øÀ·°°°°°°
B£ÆX‘™Àÿµƒ«‚ªØŒÔªØ—ß Ω“ª∂®Œ™H2X
C£ÆX‘™Àÿ‘⁄≥£Œ¬œ¬Œ»∂®¥Ê‘⁄µƒ—ıªØŒÔ“ª∂®ƒÐ”Î…’ºÓ∑¥”¶°°
D£ÆXµƒµ•÷ “ª∂® «¡º∫√µƒ∞εºÃÂ≤ƒ¡œ
6£Æœ¬¡–¿Î◊”∑Ω≥à Ω÷–’˝»∑µƒ «
°°°° A£Æπ˝¡øµƒNaHSO4”ÎBa(OH)2»Ð“∫∑¥”¶£∫Ba2++2OH-+2H++SO42-= BaSO4°˝+2H2O
B£ÆNH4HCO3 »Ð“∫”Îπ˝¡øNaOH»Ð“∫∑¥”¶£∫NH4++OH- = NH3°¸+H2O
C£Æ¥Œ¬»À·∏∆»Ð“∫÷–Õ®»Î…Ÿ¡ø∂˛—ıªØú£∫2ClO-+CO2+H2O = 2HClO+CO32-
°°D£Æ FeBr2 »Ð“∫÷–Õ®»Îπ˝¡øCl2£∫2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl-°°°°
5. µÁ∆ø≥µÀ˘”√µÁ≥ÿ“ª∞„Œ™«¶–ÓµÁ≥ÿ£¨’‚ «“ª÷÷µ‰–Õµƒø…≥‰µÁµÁ≥ÿ£¨µÁ≥ÿ◊Ð∑¥”¶Œ™£∫
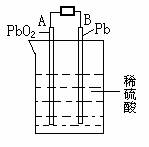 Pb+PbO2+4H++2SO42-
Pb+PbO2+4H++2SO42-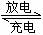 2PbSO4+2H2O
2PbSO4+2H2O
‘Úœ¬¡–Àµ∑®’˝»∑µƒ «£∫
A£Æ≥‰µÁ ±£∫—Ùº´∑¥”¶ «4OH-£≠4e-£ΩO2°¸+2H2O
B£Æ∑≈µÁ ±£∫’˝º´∑¥”¶ «Pb-2e-+SO42- PbSO4
PbSO4
C£Æ≥‰µÁ ±£∫«¶–ÓµÁ≥ÿµƒ∏∫º´”¶”Î≥‰µÁ∆˜µÁ‘¥µƒ’˝º´œý¡¨
D£Æ∑≈µÁ ±£∫µÁ◊”¡˜∂Ø∑ΩœÚ”…BµΩA
4.œ¬¡–ªÏ∫œ»Ð“∫÷–£¨∏˜¿Î◊”≈®∂»µƒ¥Û–°À≥–Ú’˝»∑µƒ «
°°°° A£Æ10mL0.1mol/L∞±ÀÆ”Î10mL0.1mol/L—ŒÀ·ªÏ∫œ£¨
c(Cl£≠)£æc(NH4+)£æc(OH£≠)£æc(H+)
°°°° B£Æ10mL0.1mol/L NH4Cl»Ð“∫”Î5mL0.2mol/LNaOH»Ð“∫ªÏ∫œ£¨
°°°°°°°° c(Na+)£Ωc(Cl£≠)£æc(OH£≠)£æc(H+)
°°°° C£Æ10mL0.1mol/LCH3COOH»Ð“∫”Î5mL0.2mol/LNaOH»Ð“∫ªÏ∫œ£¨
°°°°°° c(Na+)£Ωc(CH3COO£≠)£æc(OH£≠)£æc(H+)
°°°° D£Æ10mL0.5mol/LCH3COONa»Ð“∫”Î6mL1mol/L—ŒÀ·ªÏ∫œ£¨
°°°°°° c(Cl£≠)£æc(Na+)£æc(OH£≠)£æc(H+)
3°£NA±Ì æ∞¢∑¸º”µ¬¬Þ≥£ ˝£¨œ¬¡–Àµ∑®’˝»∑µƒ «
°°°° A£Æ6.4gÕ≠”Î◊„¡øµƒ¡Ú∑€≥‰∑÷∑¥”¶£¨◊™“∆µÁ◊” ˝Œ™0.2NA
°°°° B£Æ0.1molNa2O2”Î◊„¡øµƒÀÆ∑¥”¶◊™“∆µÁ◊” ˝Œ™0.2NA
°°°° C£Æ±Í◊º◊¥Ã¨œ¬£¨22.4LµƒNH3∫ÕCH4µƒªÏ∫œ∆¯ÃÂÀ˘∫¨µƒµÁ◊” ˝Œ™10NA D£Æ1molNH4+∫¨”–µƒπ≤º€º¸ ˝Œ™3NA
2£Æ≈–∂œœ¬¡–”–πÿªØ—ߪ˘±æ∏≈ƒÓµƒ“¿æð’˝»∑µƒ «
A£Æ—ıªØªπ‘≠∑¥”¶£∫‘™ÀÿªØ∫œº€ «∑Ò±‰ªØ
B£Æπ≤º€ªØ∫œŒÔ£∫ «∑Ò∫¨”–π≤º€º¸
C£Æ«ø»ıµÁΩ‚÷ £∫»Ð“∫µƒµºµÁƒÐ¡¶¥Û–°
D£ÆΩ Ùæßã∫æßà«∑ÒƒÐπªµºµÁ
1£Æª∑æ≥Œ€»æ“—≥…Œ™»À¿ý…Áª·√Ê¡Ÿµƒ÷ÿ¥ÛÕ˛–≤£¨œ¬¡–∂‘”¶πÿœµ≤ª’˝»∑µƒ «
|
°° |
ª∑æ≥Œ  |
‘Ï≥…ª∑æ≥Œ µƒ÷˜“™ŒÔ÷ |
|
A |
À·”Í |
∂˛—ıªØ¡Ú |
|
B |
Œ¬ “–ß”¶ |
∂˛—ıªØú |
|
C |
∞◊…´Œ€»æ |
∂˛—ıªØπË |
|
D |
π‚ªØ—ß—ÃŒÌ |
∂˛—ıªØµ™ |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com