
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
71.Α¥ΒΎ“ΜΒγάκΡήΒί‘ωΒΡΥ≥–ρ≈≈Ν–ΒΡ «
AΓΔLiΓΓ NaΓΓ KΓΓΓΓΓΓ BΓΔNaΓΓ AlΓΓ SΓΓΓΓΓΓ CΓΔPΓΓ SiΓΓ AlΓΓΓΓΓΓ DΓΔClΓΓ BrΓΓ I
70Θ°»ΥΟ«≥ΘΫΪ‘ΎΆ§“Μ‘≠Ή”ΙλΒά…œ‘ΥΕ·ΒΡΘ§Ή‘–ΐΖΫœρœύΖ¥ΒΡ2ΗωΒγΉ”Θ§≥ΤΈΣΓΑΒγΉ”Ε‘Γ±ΘΜΫΪ‘ΎΆ§“Μ‘≠Ή”ΙλΒά…œ‘ΥΕ·ΒΡΒΞΗωΒγΉ”Θ§≥ΤΈΣΓΑΈ¥≥…Ε‘ΒγΉ”Γ±ΓΘ“‘œ¬”–ΙΊ÷ςΉε‘ΣΥΊ‘≠Ή”ΓΑΈ¥≥…Ε‘ΒγΉ”Γ±ΒΡΥΒΖ®Θ§¥μΈσΒΡ «
AΘ°ΚΥΆβΒγΉ” ΐΈΣΤφ ΐΒΡΜυΧ§‘≠Ή”Θ§Τδ‘≠Ή”ΙλΒά÷–“ΜΕ®Κ§”–ΓΑΈ¥≥…Ε‘ΒγΉ”Γ±
BΘ°ΚΥΆβΒγΉ” ΐΈΣ≈Φ ΐΒΡΜυΧ§‘≠Ή”Θ§Τδ‘≠Ή”ΙλΒά÷–“ΜΕ®≤ΜΚ§ΓΑΈ¥≥…Ε‘ΒγΉ”Γ±
CΘ°ΚΥΆβΒγΉ” ΐΈΣ≈Φ ΐΒΡΜυΧ§‘≠Ή”Θ§Τδ‘≠Ή”ΙλΒά÷–Ω…ΡήΚ§”–ΓΑΈ¥≥…Ε‘ΒγΉ”Γ±
DΘ°ΚΥΆβΒγΉ” ΐΈΣΤφ ΐΒΡΜυΧ§‘≠Ή”Θ§Τδ‘≠Ή”ΙλΒά÷–Ω…Ρή≤ΜΚ§ΓΑΈ¥≥…Ε‘ΒγΉ”Γ±
69Θ°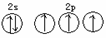 œ¬Ν–±μ¥ο Ϋ¥μΈσΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
œ¬Ν–±μ¥ο Ϋ¥μΈσΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
AΘ°ΦΉΆιΒΡΒγΉ” ΫΘΚ
BΘ°ΒΣ‘≠Ή”ΒΡL≤ψΒγΉ”ΙλΒά±μ Ψ ΫΘΚ
CΘ°ΝράκΉ”ΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΘΚ1s22s22p63s23p4
DΘ°ΧΦΘ≠12‘≠Ή”ΘΚ12ΓΓ 6C
68.œρpH=1ΒΡΡ≥Υα»ή“ΚΚΆpH=13ΒΡ«β―θΜ·ΡΤ»ή“Κ÷–Θ§Φ”»κΉψΝΩΒΡ¬ΝΤ§Θ§Ζ≈≥ωH2ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ3: 1Τδ‘≠“ρΩ…Ρή «
AΘ°ΝΫ»ή“ΚΒΡΧεΜΐœύΆ§Θ§Υα «Εύ‘Σ«ΩΥαΓΓ
BΘ°»τΥαΈΣ“Μ‘Σ«ΩΥαΘ§Υα»ή“ΚΒΡΧεΜΐ «Φν»ή“ΚΧεΜΐΒΡ3±Ε
CΘ°ΝΫ»ή“ΚΒΡΧεΜΐœύΆ§Θ§Υα «»θΥα
 DΘ°Υα ««ΩΥαΘ§«“Υα»ή“ΚΒΡ≈®Ε»±»NaOH»ή“Κ≈®Ε»¥σ
DΘ°Υα ««ΩΥαΘ§«“Υα»ή“ΚΒΡ≈®Ε»±»NaOH»ή“Κ≈®Ε»¥σ
67Θ°ΫΪ15.6g Na2O2ΚΆ5.4g AlΆ§ ±Ζ≈»κ“ΜΕ®ΝΩΒΡΥ°÷–Θ§≥δΖ÷Ζ¥”ΠΚσΒΟΒΫ200mL»ή“ΚΘ§‘ΌœρΗΟ»ή“Κ÷–ΜΚ¬ΐΆ®»κHClΤχΧε6.72L(±ξΉΦΉ¥Ωω)Θ§»τΚω¬‘Ζ¥”ΠΙΐ≥Χ÷–»ή“ΚΒΡΧεΜΐ±δΜ·Θ§‘ρœ¬Ν–≈–Εœ’ΐ»ΖΒΡ «ΓΓΓΓ
AΘ°Ζ¥”ΠΙΐ≥Χ÷–ΒΟΒΫ6.72L(±ξΉΦΉ¥Ωω)ΒΡΤχΧεΓΓΓΓΓΓ BΘ°Ήν÷’ΒΟΒΫ7.8gΒΡ≥ΝΒμ
ΓΓCΘ°Ήν÷’ΒΟΒΫΒΡ»ή“Κ÷–c(NaCl)=1.5mo/L ΓΓDΘ°Ήν÷’ΒΟΒΫΒΡ»ή“Κ÷–c(Na+)=c(Cl-)+c(OH-)
66Θ°1798ΡξΖ®ΙζΜ·―ßΦ“Ε‘¬Χ÷υ ·ΚΆΉφΡΗ¬ΧΫχ––Μ·―ßΖ÷ΈωΖΔœ÷ΝΥνκΓΘ“―÷Σ¬Χ÷υ · «“Μ÷÷≥ ¬Χ…ΪΒΡΙηΥα―ΈΘ§Ω…±μ ΨΈΣBexAly[SimOn](xΓΔyΓΔmΓΔnΨυΈΣΉ‘»Μ ΐ)Θ§Τδ÷–“θάκΉ”≤ΩΖ÷ΫαΙΙ»γœ¬ΆΦΥυ Ψ(“―÷ΣΓΓΓΓ ±μ ΨΙηΥαΗυάκΉ”SiO44-)Θ§œ¬Ν–ΥΒΖ®ΩœΕ®≤Μ’ΐ»ΖΒΡ «

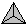 ΓΓ ΓΓA. “θάκΉ”Μ·―ß ΫΈΣΘΚSi6O1612-
ΓΓ ΓΓA. “θάκΉ”Μ·―ß ΫΈΣΘΚSi6O1612-
B. ¬Χ÷υ ·Ω…”Ο―θΜ·Έο–Έ Ϋ±μ ΨΈΣΘΚ3BeOΓΛAl2O3ΓΛ6SiO2
C. ¬Χ÷υ ·Ω…±μ ΨΈΣBe3Al2[Si3O12]
D. ¬Χ÷υ ·Ω…»ή”Ύ«ΩΦνΚΆ«βΖζΥα
65Θ° »γΆΦΘ§Δώ «Κψ―ΙΟή±’»ίΤςΘ§Δρ «Κψ»ίΟή±’»ίΤςΓΘΤδΥϋΧθΦΰœύΆ§ ±Θ§‘ΎΔώΓΔΔρ÷–Ζ÷±πΦ”»κ3mol ZΘ§Τπ Φ ±»ίΤςΧεΜΐΨυΈΣV LΘ§ΖΔ…ζ»γœ¬Ζ¥”Π≤Δ¥οΒΫΤΫΚβ(XΓΔYΉ¥Χ§Έ¥÷Σ)ΘΚaX(?)+2Y(?)
»γΆΦΘ§Δώ «Κψ―ΙΟή±’»ίΤςΘ§Δρ «Κψ»ίΟή±’»ίΤςΓΘΤδΥϋΧθΦΰœύΆ§ ±Θ§‘ΎΔώΓΔΔρ÷–Ζ÷±πΦ”»κ3mol ZΘ§Τπ Φ ±»ίΤςΧεΜΐΨυΈΣV LΘ§ΖΔ…ζ»γœ¬Ζ¥”Π≤Δ¥οΒΫΤΫΚβ(XΓΔYΉ¥Χ§Έ¥÷Σ)ΘΚaX(?)+2Y(?) 3Z(g)ΓΘ¥Υ ±Δρ÷–XΓΔYΓΔZΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ3:2:2Θ§‘ρœ¬Ν–ΥΒΖ®“ΜΕ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓ
3Z(g)ΓΘ¥Υ ±Δρ÷–XΓΔYΓΔZΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ3:2:2Θ§‘ρœ¬Ν–ΥΒΖ®“ΜΕ®’ΐ»ΖΒΡ «ΓΓΓΓΓΓ
AΘ°»τXΓΔYΨυΈΣΤχΧ§Θ§‘ρΤΫΚβ ±ΤχΧεΤΫΨυΡΠΕϊ÷ ΝΩΘΚΔώΘΨΔρ
BΘ°»τXΓΔY≤ΜΨυΈΣΤχΧ§Θ§‘ρΤΫΚβ ±XΒΡ≤ζ¬ ΘΚΔώΘΨΔρ
CΘ°»τXΓΔYΨυΈΣΤχΧ§Θ§‘ρ¥”Τπ ΦΒΫΤΫΚβΥυ–η ±ΦδΘΚΔώ>Δρ
DΘ°»τXΈΣΙΧΧ§Θ§YΈΣΤχΧ§Θ§ΒΫ¥οΤΫΚβΚσ»τ‘ΎΔρ÷–‘ΌΦ”»κ1molZΘ§‘ρ–¬ΤΫΚβ ±ZΒΡΧεΜΐΖ÷ ΐ±δ–Γ
64Θ°”–“ΜΕ®÷ ΝΩΒΡKNO3―υΤΖΘ§‘Ύ100Cœ¬Φ”’τΝσΥ° Ι÷°≥δΖ÷»ήΫβΘ§≤–ΝτΙΧΧεΒΡ÷ ΝΩΈΣ250gΓΘΗΟ Β―ι‘Ύ400Cœ¬Ϋχ–– ±Θ§≤–ΝτΙΧΧε÷ ΝΩΈΣ120gΘ§700C ±ΈΣ20gΓΘ“―÷ΣKNO3‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡ»ήΫβΕ»ΘΚ
|
Έ¬Ε» |
100C |
400C |
550C |
700C |
|
»ήΫβΕ» |
20g |
65g |
100g |
140g |
œ¬Ν–Ε‘ΗΟ―υΤΖΒΡΆΤΕœ’ΐ»ΖΒΡ «
AΓΔ―υΤΖΈΣ¥ΩΨΜΈοΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΓΔ―υΤΖ÷–Μλ”–≤Μ»ή”ΎΥ°ΒΡ‘”÷
CΓΔ―υΤΖ÷–Μλ”–»ήΫβΕ»Ϋœ¥σΒΡ‘”÷ ΓΓΓΓΓΓ DΓΔΒ±Έ¬Ε»‘Ύ550CΉσ”“ ±KNO3Άξ»Ϊ»ήΫβ
63Θ°Ζ÷ΈωΜ·―ß÷–≥Θ”ΟX…δœΏ―–ΨΩΨßΧεΫαΙΙΘ§”–“Μ÷÷άΕ…ΪΨßΧε[Ω…±μ ΨΈΣΘΚMxFey(CN)z]Θ§―–ΨΩ±μΟςΥϋΒΡΫαΙΙΧΊ–‘ «ΘΚFe2+ΚΆFe3+Ζ÷±π’ΦΨίΝΔΖΫΧεΒΡΕΞΒψΘ§Ή‘…μΜΞ≤ΜœύΝΎΘ§ΕχCNΘ≠ΈΜ”ΎΝΔΖΫΧεΒΡάβ…œΓΘΤδΨßΧε÷–ΒΡ“θάκΉ”ΨßΑϊΫαΙΙ»γΆΦ ΨΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
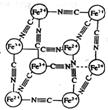 AΘ°ΗΟΨßΧε «άκΉ”ΨßΧεΓΓΓΓ
AΘ°ΗΟΨßΧε «άκΉ”ΨßΧεΓΓΓΓ
BΘ°MΒΡάκΉ”ΈΜ”Ύ…œ ωΨßΑϊΟφ–ΡΘ§≥ +2Φέ
CΘ°MΒΡάκΉ”ΈΜ”Ύ…œ ωΨßΑϊΧε–ΡΘ§≥ +1ΦέΘ§«“M+Ω’»±¬ ΈΣ50%(Χε–Ρ÷–ΟΜ”–M+’ΦΉήΧε–ΡΒΡΑΌΖ÷±»)
DΘ°ΨßΧεΒΡΜ·―ß ΫΩ…±μ ΨΈΣMFe2(CN)6Θ§«“MΈΣ+1Φέ
62Θ°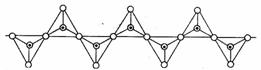 ΙηΥα―Έ”κΕΰ―θΜ·Ιη“Μ―υ,ΕΦ «“‘Ιη―θΥΡΟφΧεΉςΈΣΜυ±ΨΫαΙΙΒΞ‘ΣΓΘΙη―θΥΡΟφΧεΩ…“‘”ΟΆΕ”ΑΆΦ±μ Ψ≥…ΘΚ
ΙηΥα―Έ”κΕΰ―θΜ·Ιη“Μ―υ,ΕΦ «“‘Ιη―θΥΡΟφΧεΉςΈΣΜυ±ΨΫαΙΙΒΞ‘ΣΓΘΙη―θΥΡΟφΧεΩ…“‘”ΟΆΕ”ΑΆΦ±μ Ψ≥…ΘΚ
Τδ÷–Γπ±μ Ψ―θ‘≠Ή”Θ§÷––ΡΚΎΒψ±μ ΨΙη‘≠Ή”ΓΘΙη―θΥΡΟφΧεΆ®Ιΐ≤ΜΆ§ΖΫ ΫΒΡΝ§Ϋ”Ω…“‘Ήι≥…Ης÷÷≤ΜΆ§ΒΡΙηΥαΗυάκΉ”ΓΘ ‘»ΖΕ®‘ΎΈόœό≥ΛΒΡΒΞΝ¥“θάκΉ”÷–(ΦϊΆΦ)Θ§Ιη‘≠Ή””κ―θ‘≠Ή”ΒΡΗω ΐ÷°±»ΈΣ B
ΓΓΓΓ AΘ°1:2ΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°1:3ΓΓΓΓΓΓΓΓΓΓ ΓΓCΘ°2:5ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°2:7
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com