
题目列表(包括答案和解析)
25.( 9 分)
下图中 A 至 I 分别表示化学反应中的一种常见物质,工业上常用电解 A 的饱和溶液的方法制取 B 。其中 E 、 F 、 J 在通常情况下是气体单质, E 为有色气体, J 是空气中含量最多的气体, X 是一种常见的金属单质。部分产物和反应条件略去。
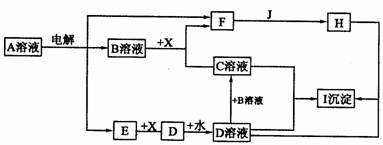
填写下列空白:
( l )写出 A 溶液电解的化学方程式:_______________________________________
( 2 )若将 a mol D 全部转化为 C ,则 B 的物质的量的取值范围为______________
( 3 ) C + D →I 的离子反应方程式为_______________________________________
(
4 )一定条件下, H 可进行如下转化: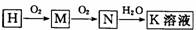 。将 K 溶液逐滴滴人 C 溶液至过量,可观察到的现象是_______________________________________
。将 K 溶液逐滴滴人 C 溶液至过量,可观察到的现象是_______________________________________
___________________________________________________________________________。
24.( 10 分)
某含有少量 FeCl2杂质的 FeCl3样品,现要测定其中铁元素的含量.实验步骤如下:
① 准确称量mg 样品;
② 向样品中加人 10 mL 5 mol · L一1的盐酸,再加人蒸馏水,配制成 250 mL 溶液; ③ 量取 25 mL 操作 ② 中配得的溶液,加人 3 mL 溴水,加热使之完全反应;
④ 趁热迅速加人质量分数为 10 %的氨水至过量,充分搅拌,使之完全沉淀;
⑤ 过滤,将沉淀洗涤后反复灼烧、冷却、称量至恒重。
请根据上面的叙述回答:
( l )溶解样品时要加人盐酸,其目的是_______________________________________
( 2 )配制 250 mL 溶液时,除需玻璃棒、烧杯外,还须用到的玻璃仪器是__________
________________________________________________
( 3 )加人溴水时发生反应的离子方程式是:
____________________________________________________
( 4 )若坩埚质量为 W1 g ,增锅与灼烧后固体的总质量是 W2 g ,则样品中铁元素的质量分数是_____________________________
22.某学生用 NaHCO3和 KHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)。下列分析推理不正确的是
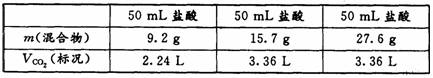
A.盐酸的物质的量浓度为 3.0 mol · L 一1
B.根据表中数据不能计算出混合物中 NaHCO3的质量分数
C.加人混合物 9.2g 时盐酸过量
D.15.7g 混合物未与盐酸完全反应
第 II 卷(非选择题,共 56 分)
已知 A 、 B 、 C 、 D 为原子序数依次增大的四种短周期元素,最外层电子数均小于 8 ,其中只有 B 是金属元素。 A 元素的原子最外层电子数是次外层的 3 倍,且 A 与 B 可形成原子个数比分别为 1:1 和 1:2 的两种化合物, A 与 D 的原子序数之和等于 B 与 C 的原子序数之和。请回答下列问题:
( 1 ) B 、 D 的元素符号分别是: B_________ , D________
( 2 ) A 与 C 形成的化合物属于_________晶体; C 与 D 形成的化合物的电子式是:
________________________
( 3 )写出 A 、 B 形成的化合物与 CO2发生氧化还原反应的化学方程式:
________________________________________________________________。
( 4 ) A 、 B 、 C 形成的化合物的水溶液的 pH_______7 (填“ > " , " =”或“ < ” ) ,原因是___________________________________________________________(用文字表述)。
21.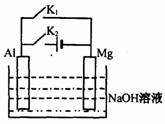 将
Mg 条、 Al 条平行插人一定浓度的 NaOH 溶液中,如图所示用导线连接起来。下列叙述符合事实的是
将
Mg 条、 Al 条平行插人一定浓度的 NaOH 溶液中,如图所示用导线连接起来。下列叙述符合事实的是
A.断开 K2,闭合 K1时, Al 电极反应为:
Al+ 4OH-一3e一===AlO2-+ 2H2O
B.断开 K2,闭合 Kl 时,由于 Mg 比 Al 活泼,故 Mg 失去电子被氧化成 Mg2+
C.断开 K1,闭合 K2时,电子由 Mg 向 Al 流动
D.断开 Kl ,闭合 K2时,溶液中立即会有白色沉淀析出
20.已知某溶液中存在 OH一、 H+、 NH4+和 Cl一四种离子,其浓度大小有如下关系。其中不可能的是
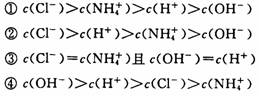
A.① ② B.② ③ C.③ D.④
19.14g 铜、银合金与足量的某浓度的硝酸反应,将生成的气体与 1.12L (标准状况下)氧气混合,通人水中恰好全部被吸收,则合金中铜的质量为
A.3.2g B.1.6g C.9.6 g D.6.4g
18. 霉变的大米、花生中含有黄曲霉素,黄曲霉素的结构如图所示。下列说法中不正确的是 A.霉变的大米、花生等绝对不能食用
霉变的大米、花生中含有黄曲霉素,黄曲霉素的结构如图所示。下列说法中不正确的是 A.霉变的大米、花生等绝对不能食用
B.l 个黄曲霉素分子中至少有 8 个碳原子共平面
C.1 mol 该化合物能与 7 molH2发生加成反应
D.1 mol 该化合物与 NaOH 溶液反应,最多消耗 2 mol NaOH
17.金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式
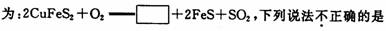
A.方框中的物质应为 Cu2S
B.O2只作氧化剂
C.SO2 既是氧化产物又是还原产物
D.若有 1 molSO2 生成,则反应中有 4 mol 电子转移
15.有如下几种制备气体的方案:
① 加热稀硫酸和乙醇制备乙烯,
② 用水与过氧化钠固体反应制氧气,
③ 用稀硫酸和大理石制备二氧化碳,
④ 氧化钙与浓氨水反应制氨气,
⑤ NaI固体和浓硫酸混合共热制碘化氢;
⑥ 电石与饱和食盐水制乙炔。不宜采用的方案有
A.仅 ① ③ ⑤ B.仅 ① ② ③
C.仅 ③ ④ D.全部
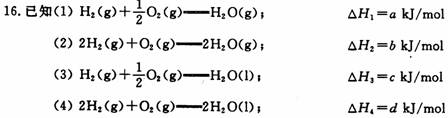
下列关系式中正确的是
A .2a = d < 0 B.b > d > 0 C.2a = b < 0 D.2c = d > 0
14.以 NA 表示阿伏加德罗常数,下列说法正确的是
A.如果 5.6 LN2含有 n 个氮分子,则阿伏加德罗常数一定为 4n
B.1 L 1 mol·L一1的 FeCl3溶液中含有铁离子的数目为 N A
C.1 mol 苯中含有 3NA 个 C=C 双键
D.46g NO2与 N2O4的混合物中含 3 NA 个原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com