
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
7.Ň»»ŻŃ§ĐËȤС×éÔÚĽŇÖĐ˝řĐĐ»ŻŃ§ĘµŃ飬°´ŐŐÍĽ1Á¬˝ÓşĂĎß··˘ĎÖµĆĹݲ»ÁÁŁ¬°´ŐŐÍĽ2Á¬˝ÓşĂĎß··˘ĎÖµĆĹÝÁÁŁ¬Óɴ˵óöµÄ˝áÂŰŐýČ·µÄĘÇ( C )
AŁ®NaClĘǷǵç˝âÖĘ
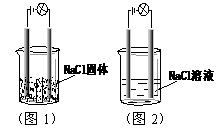 BŁ®NaClČÜŇşĘǵç˝âÖĘ
BŁ®NaClČÜŇşĘǵç˝âÖĘ
CŁ®NaClÔÚË®ČÜŇşÖеçŔëłöÁËżÉŇÔ×ÔÓÉŇƶŻµÄŔë×Ó
DŁ®NaClČÜŇşÖĐË®µçŔëłö´óÁżµÄŔë×Ó
6.łŁÎÂĎÂŁ¬ÄłČÜŇşÖĐÓÉË®µçŔë˛úÉúµÄH+µÄŨ¶ČÎŞ1ˇÁ10-5moL/LŁ¬Ôň¸ĂČÜŇşÖеÄČÜÖĘżÉÄÜĘÇĎÂÁĐÎďÖĘÖеÄ( C )
A.HClˇˇ ˇˇˇˇB.NaHSO4ˇˇ ˇˇˇˇC.Na2CO3ˇˇ ˇˇˇˇD.NaCl
5.łŁÎÂʱŁ¬˝«pH=3µÄŃÎËáşÍpH=11µÄ°±Ë®µČĚĺ»ý»ěşĎşóŁ¬ËůµĂČÜŇşµÄpH( B )
AŁ®µČÓÚ7ˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®´óÓÚ7ˇˇˇˇˇˇˇˇCŁ®ĐˇÓÚ7ˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®ÎŢ·¨Č·¶¨
4.ŇŃÖŞ0.1mol/LµÄ´×ËáČÜŇşÖĐ´ćÔÚµçŔëĆ˝şâŁşˇˇ CH3COOH CH3COOŁ+H+ ˇˇŇŞĘąČÜŇşÖĐc(H+)/c(CH3COOH)±ČÖµÔö´óŁ¬żÉŇÔ˛ÉȡµÄ´ëĘ©ĘÇ( D )
CH3COOŁ+H+ ˇˇŇŞĘąČÜŇşÖĐc(H+)/c(CH3COOH)±ČÖµÔö´óŁ¬żÉŇÔ˛ÉȡµÄ´ëĘ©ĘÇ( D )
AŁ®ĽÓÉŮÁżCH3COONH4ąĚĚ塡ˇˇBŁ®˝µµÍζȡˇˇˇCŁ®ĽÓÉŮÁżNaCląĚĚ塡ˇˇDŁ®Éý¸ßζČ
3.0.10 mol/LŃÎËáşÍ0.12 mol/L NaOHČÜŇşµČĚĺ»ý»ěşĎşóŁ¬ČÜŇşµÄpHµČÓÚ( D )
A. 2.0ˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇ B. 12.3ˇˇˇˇ ˇˇˇˇˇˇ C. 1.7ˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇ D. 12.0ˇˇ ˇˇ
2.ÓĂĐżşÍ1mol/LϡÁňËáČÜŇşÖĆȡÇâĆřŁ¬ÓűĚá¸ßÖĆȡÇâĆřµÄËŮÂĘŁ¬ĎÂÁĐ´ëĘ©˛»żÉĐеÄĘÇ( A )
AŁ®¸ÄÓĂ98%µÄŨÁňËᡡˇˇˇˇˇˇ BŁ®ĘąÓøüСżĹÁŁµÄĐżÁŁ
CŁ®µÎČëÉŮÁżCuSO4ČÜŇşˇˇˇˇˇˇˇˇDŁ®ĽÓČČ
1.ĎÂÁĐÎďÖĘŁ¬ĘôÓÚÇżµç˝âÖʵÄ( C )
AŁ®NH3.H2Oˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇBŁ®H2Oˇˇˇˇˇˇˇˇˇˇ ˇˇ
CŁ®CH3COONH4ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®CH3COOH
12.µŘÇň»ŻŃ§ÖĐŁ¬Í¨łŁÓĂČČÖŘ·ÖÎöŃĐľżżóÎďÔÚĘÜČČʱµÄÖĘÁż±ä»ŻŇÔČ·¶¨Ćä×éłÉˇŁČˇ66.6mgÓɸßÁëĘŻ[Al4Si4O10(OH)8]şÍ·˝˝âĘŻ(CaCO3)×éłÉµÄżóÎĽÓČČŁ¬ÔÚ673K-1123KÇřĽäÄÚ·Ö˝âÎŞŃő»ŻÎŃůĆ·×ÜʧÖŘ13.8mgˇŁ
(1)·˝˝âĘŻµÄʧÖŘ°Ů·Ö±ČÎŞˇˇˇˇˇˇˇˇ Ł»(2)ĽĆËăżóÎďÖиßÁëĘŻµÄÖĘÁż·ÖĘýˇŁ
11.ľ§ĚĺąčĘÇŇ»ÖÖÖŘŇŞµÄ·Ç˝đĘô˛ÄÁĎŁ¬ÖƱ¸´żąčµÄÖ÷ŇŞ˛˝ÖčČçĎÂŁş˘Ů¸ßÎÂĎÂÓĂĚĽ»ąÔ¶ţŃő»ŻąčÖƵôֹ衡 ˘Ú´ÖąčÓë¸ÉÔďHClĆřĚĺ·´Ó¦ÖƵĂSiHCl3ŁşSi+3HCl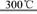 SiHCl3+H2ˇˇ ˘ŰSiHCl3ÓëąýÁżH2ÔÚ1000-1100ˇć·´Ó¦ÖƵôżąčˇŁŇŃÖŞSiHCl3Ł¬ÄÜÓëH2OÇżÁŇ·´Ó¦Ł¬ÔÚżŐĆřÖĐŇ××ÔČĽˇŁÇë»Ř´đĎÂÁĐÎĘĚ⣺
SiHCl3+H2ˇˇ ˘ŰSiHCl3ÓëąýÁżH2ÔÚ1000-1100ˇć·´Ó¦ÖƵôżąčˇŁŇŃÖŞSiHCl3Ł¬ÄÜÓëH2OÇżÁŇ·´Ó¦Ł¬ÔÚżŐĆřÖĐŇ××ÔČĽˇŁÇë»Ř´đĎÂÁĐÎĘĚ⣺
(1)Đ´łöąčµÄÔ×ӽṹʾŇâÍĽˇˇˇˇˇˇˇˇˇˇ ˇŁ
(2)´ÖąčÓëHCl·´Ó¦ÍęČ«şóŁ¬ľŔäÄýµĂµ˝µÄSiHCl3(·Đµă33.0ˇć)ÖĐş¬ÓĐÉŮÁżSiCl4(·Đµă57.6ˇć)şÍHCl(·ĐµăŁ84.7ˇć)Ł¬Ěá´żSiHCl3˛ÉÓõķ˝·¨ÎŞˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
(3)ÓĂSiHCl3ÓëąýÁżH2·´Ó¦ÖƱ¸´żąčµÄ×°ÖĂČçĎÂ(ČČÔ´Ľ°ĽĐłÖ×°ÖĂÂÔČĄ)Łş
|
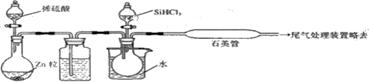
˘Ů×°ÖĂBÖеÄĘÔĽÁĘÇŨH2SO4Ł¬Ćä×÷ÓĂĘÇ________________Ł¬ÔÚÉĎĘö×°ÖĂÖĐĐčŇŞĽÓČȵÄĘǡˇˇˇˇˇ (ĚîĐňşĹ)ˇŁ
˘Ú·´Ó¦Ň»¶ÎʱĽäşóŁ¬×°ÖĂDÖй۲쵽µÄĎÖĎóĘǡˇˇˇˇˇˇˇˇˇˇˇ Ł¬ŇŃÖŞ·´Ó¦˘ÚĂżÉúłÉ1molH2ʱ·ĹČČ381kJŁ¬ÇëĐ´łö×°ÖĂDÖĐ·´Ó¦µÄČČ»ŻŃ§·˝łĚĘ˝______________________________ˇŁ
˘ŰÎŞ±ŁÖ¤ÖƱ¸´żąčʵŃéµÄłÉą¦Ł¬˛Ů×÷µÄąŘĽüĘÇĽě˛éʵŃé×°ÖõÄĆřĂÜĐÔŁ¬żŘÖƺ÷´Ó¦Î¶ČŇÔĽ°ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
˘ÜÎŞĽř¶¨˛úĆ·ąčÖĐĘÇ·ńş¬Î˘ÁżĚúµĄÖĘŁ¬˝«ĘÔŃůÓĂϡŃÎËáČܽ⣬ȡÉϲăÇĺŇşşóĐčÔŮĽÓČëµÄĘÔĽÁ(ĚîĐ´×Öĸ´úşĹ)Ęǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
a.µâË®ˇˇˇˇ b.ÂČË®ˇˇˇˇ c.NaOHČÜŇşˇˇˇˇ d.KSCNČÜŇşˇˇˇˇ e.Na2SO3ČÜŇş
10.ąčŃőËÄĂćĚĺżÉŇÔÓĂÍĽ30-1a±íĘľŁ¬ÍĽbˇ˘cĘÇąčŃőËÄĂćĚĺ˝áşĎłÉ»·×´˝áąąµÄÁ˝¸öŔý×ÓˇŁÇë»Ř´đĎÂÁĐÎĘĚ⣺
(1)ČôÔÚ»·×´˝áąąÖĐąčµÄÔÓÚĘýÎŞnŁ¬Đ´łö»·×´˝áąąÖĐąčËá¸ůŔë×ÓµÄͨʽˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
(2)ĽşÖŞÂĚÖůĘŻĘÇÓÉ»·×´ąčŃőËÄĂćĚĺąąłÉµÄąčËáŃΡŁËüĘÇş¬ÓĐî롢ÂÁÁ˝ÖÖÔŞËصĸ´ŃÎŁ¬Ëá¸ůÖĐş¬ÓĐ6¸öąčÔ×ÓŁ¬î롢ÂÁ˝áşĎµÄËá¸ůŔë×ÓĘýĎŕµČˇŁĐ´łöÂĚÖůĘŻµÄ»ŻŃ§Ę˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ Ł¬˛˘ÔÚ´Ë»ů´ˇÉϸÄĐ´łÉŃő»ŻÎďĎŕ˝áşĎµÄĐÎĘ˝ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com