
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
23Θ°”Ο»γΆΦΥυ ΨΉΑ÷Ο(Φ–≥÷“«Τς Γ¬‘)Ϋχ–– Β―ιΘ§ΫΪ“ΚΧεA÷πΒΈΦ”»κΒΫΙΧΧεB÷–Θ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΆΦ÷–DΉΑ÷Ο‘Ύ Β―ι÷–ΒΡΉς”Ο «ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΘ
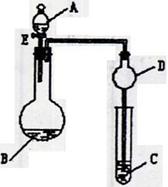 (2)»τ AΈΣ30%H2O2»ή“ΚΘ§BΈΣMnO2
Θ§C Δ”–«βΝρΥα(H2S)±ΞΚΆ»ή“ΚΘ§–ΐΩΣEΚσΘ§C÷–≥ωœ÷«≥ΜΤ…ΪΜκΉ«ΒΡœ÷œσΘ§–¥≥ωC÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΘ
(2)»τ AΈΣ30%H2O2»ή“ΚΘ§BΈΣMnO2
Θ§C Δ”–«βΝρΥα(H2S)±ΞΚΆ»ή“ΚΘ§–ΐΩΣEΚσΘ§C÷–≥ωœ÷«≥ΜΤ…ΪΜκΉ«ΒΡœ÷œσΘ§–¥≥ωC÷–ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓΓΓΓΘ
(3)»τAΈΣ≈®―ΈΥαΘ§BΈΣKMnO4Θ§C÷– Δ”–KIΒμΖέ»ή“ΚΘ§–ΐΩΣEΚσΘ§C÷–ΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΘΜΦΧ–χΆ®ΤχΧε”ΎC÷–Θ§ΉψΙΜ≥ΛΒΡ ±ΦδΚσΘ§ΖΔœ÷C÷–»ή“ΚΒΡ―’…Ϊœϊ ßΘ§’β «“ρΈΣ‘Ύ»ή“Κ÷–I2Ρή±ΜCl2―θΜ·ΈΣHIO3Θ§–¥≥ωΗΟΖ¥”ΠΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΘ
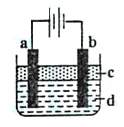
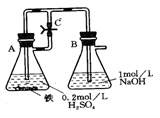 (4)»τAΈΣ≈®Α±Υ°Θ§BΈΣ…ζ ·Μ“Θ§C÷– Δ”–AlCl3»ή“ΚΘ§–ΐΩΣEΘ§ΉψΙΜ≥ΛΒΡ ±ΦδΚσΘ§C÷–ΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΘ§C÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΘ
(4)»τAΈΣ≈®Α±Υ°Θ§BΈΣ…ζ ·Μ“Θ§C÷– Δ”–AlCl3»ή“ΚΘ§–ΐΩΣEΘ§ΉψΙΜ≥ΛΒΡ ±ΦδΚσΘ§C÷–ΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΘ§C÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΘ
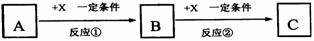
22Θ° AΓΔBΓΔCΓΔXΨυΈΣ÷–―ß≥ΘΦϊΒΡ¥ΩΨΜΈοΘ§ΥϋΟ«÷°Φδ”–»γœ¬ΉΣΜ·ΙΊœΒ(Η±≤ζΈο“―¬‘»Ξ)ΓΘ
 ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
ΓΓ
‘ΜΊ¥πΘΚ
(1)»τX ««Ω―θΜ·–‘ΒΞ÷ Θ§‘ρA≤ΜΩ…Ρή «ΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓΓΓΓΓ ΓΓaΘ°SΓΓΓΓΓΓ bΘ°N2ΓΓΓΓΓΓΓΓ cΘ°NaΓΓΓΓ dΘ°MgΓΓΓΓΓΓΓΓ eΘ°Al
(2)»τX «Ϋπ τΒΞ÷ Θ§œρCΒΡΥ°»ή“Κ÷–ΒΈΦ”AgNO3»ή“ΚΘ§≤ζ…ζ≤Μ»ή”ΎœΓHNO3ΒΡΑΉ…Ϊ≥ΝΒμΘ§‘ρBΒΡΜ·―ß ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜC»ή“Κ‘Ύ÷ϋ¥φ ±”ΠΦ”»κ…ΌΝΩXΘ§άμ”… «(”Ο±Ί“ΣΒΡΈΡΉ÷ΚΆάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)»τAΓΔBΓΔCΈΣΚ§Ϋπ τ‘ΣΥΊΒΡΈόΜζΜ·ΚœΈοΘ§XΈΣ«ΩΒγΫβ÷ Θ§A»ή“Κ”κC»ή“ΚΖ¥”Π…ζ≥…BΘ§‘ρBΒΡΜ·―ß ΫΈΣΓΓΓΓΓΓΓΓΓΓ Θ§XΒΡΜ·―ß ΫΩ…ΡήΈΣ(–¥≥ω≤ΜΆ§άύΈο÷ )ΓΓΓΓΓΓΓΓΓΓΓΓ ΜρΓΓΓΓΓΓ ΓΓΓΓΘ§Ζ¥”ΠΔΌΒΡάκΉ”ΖΫ≥Χ ΫΈΣ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΜρΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
21.Ρ≥Ζ¥”ΠΧεœΒΒΡΈο÷ ”–ΘΚNaOHΓΔAu2O3ΓΔNa2S4O6ΓΔNa2S2O3ΓΔAu2OΓΔH2OΓΘ
ΓΓ (1)«κΫΪAu2O3÷°ΆβΒΡΖ¥”ΠΈο”κ…ζ≥…ΈοΖ÷±πΧν»κ“‘œ¬Ω’ΗώΡΎΓΘ

ΓΓ (2)Ζ¥”Π÷–Θ§±ΜΜΙ‘≠ΒΡ‘ΣΥΊ «_______Θ§ΜΙ‘≠ΦΝ «____________ΓΘ
(3)ΫΪ―θΜ·ΦΝ”κΜΙ‘≠ΦΝΧν»κΩ’Ηώ÷–Θ§≤Δ±ξ≥ωΒγΉ”ΉΣ“ΤΒΡΖΫœρΚΆ ΐΡΩΓΘ

(4)ΖΡ÷·ΙΛ“Β÷–≥Θ”Ο¬»ΤχΉςΤ·ΑΉΦΝΘ§Na2S2O3Ω…ΉςΈΣΤ·ΑΉΚσ≤ΦΤΞΓΑΆ―¬»ΦΝΓ±Θ§Na2S2O3ΚΆCl2Ζ¥”ΠΒΡ≤ζΈο «H2SO4ΓΔNaClΚΆHClΘ§‘ρΜΙ‘≠ΦΝ”κ―θΜ·ΦΝΈο÷ ΒΡΝΩ÷°±»ΈΣ__________ΓΘ
20Θ°ΫϋΡξά¥Θ§Φ”ΓΑΒβΓ± ≥―ΈΫœΕύ Ι”ΟΝΥΒβΥαΦΊΘ§KIO3‘ΎΙΛ“Β…œΩ…”ΟΒγΫβΖ®÷Τ»ΓΘ§“‘ ·ΡΪΚΆΧζΈΣΒγΦΪΘ§“‘KI»ή“ΚΈΣΒγΫβ“Κ‘Ύ“ΜΕ®ΧθΦΰœ¬ΒγΫβΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣKI+3H2O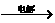 KIO3+3H2ΓϋΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «( )
KIO3+3H2ΓϋΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «( )
AΓΓ ΒγΫβ ±Θ§ ·ΡΪΉς“θΦΪΘ§ΧζΉς―τΦΪ ΓΘΓΓΓΓ
B ΓΓΒγΫβ ±Θ§‘Ύ“θΦΪΗΫΫϋΒΡpH÷Β±δ¥σΓΘ
CΓΓ ΒγΫβΚσΒΟΒΫKIO3≤ζΤΖΒΡ≤Ϋ÷η”–ΘΚΙΐ¬ΥΓζ≈®ΥθΓζΫαΨßΓζΉΤ…’
DΓΓ ΒγΫβ÷–ΟΩΉΣ“Τ0.6molΒγΉ”Θ§άμ¬έ…œΩ…ΒΟΒΫ0.1molΈόΥ°KIO3ΨßΧε
ΨμΔρ Ζ«―Γ‘ώΧβ
19Θ°2000Ρξ1‘¬ΒΉΘ§¬ό¬μΡα―«“ΜΫπΩσΈέΥ°¥Πάμ≥Ί“ρΫΒ±©”ξΕχΖΔ…ζΝ―ΩΎΘ§10Άρ…ΐΚ§«ηΜ·ΈοΚΆ«ΠΓΔΙ·Β»÷ΊΫπ τΒΡΈέΥ°Νς»κΒΌ»χΚ”(ΕύηßΚ”÷ßΝς)Θ§‘λ≥…ΗΟΚ”90%“‘…œΒΡΕ·÷≤ΈοΥάΆωΓΘ’β «ΦΧ«–Εϊ≈Β±¥άϊΚΥ–Ι¬©“‘ά¥Θ§≈Ζ÷όΉν―œ÷ΊΒΡΜΖΨ≥Έέ»Ψ ¬ΦΰΓΘ«ηΤχ[(CN)2]ΚΆ«ηΜ·ΈοΕΦ «ΨγΕΨ–‘Έο÷ Θ§«ηΖ÷Ή”ΒΡΫαΙΙ ΫΈΣNΓ‘CΘ≠CΓ‘NΘ§–‘÷ ”ꬱպœύΥΤΘ§œ¬Ν––π ω¥μΈσΒΡ «(ΓΓΓΓΓΓ )
AΓΓ «ηΖ÷Ή”÷–ΥΡ‘≠Ή”Ι≤÷±œΏΘ§ «Ζ«ΦΪ–‘Ζ÷Ή”ΓΓΓΓΓΓΓΓΓΓΓΓ BΓΓ «ηΖ÷Ή”÷–CΓ‘NΦϋ≥Λ¥σ”ΎCΓ‘CΦϋ≥Λ
CΓΓ «ηΤχΡή”κ«ΩΦν»ή“ΚΖ¥”ΠΒΟΒΫ«ηΜ·ΈοΚΆ¥Έ«ηΥα―ΈΓΓΓΓΓΓ DΓΓ «ηΜ·«β‘Ύ“ΜΕ®ΧθΦΰœ¬Ρή”κœ©ΧΰΖΔ…ζΦ”≥…Ζ¥”Π
18Θ°Ω…”Ο”Ύ«χ±πNa2SΓΔNa2SO3ΓΔNa2SO4ΓΔNa2CO3ΓΔNa2SiO3 ΓΔNa2S2O3Νυ÷÷»ή“ΚΒΡ“Μ÷÷ ‘ΦΝ «(ΓΓΓΓ )
AΓΔNaOHΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΓΔ―ΈΥαΓΓΓΓΓΓΓΓΓΓΓΓΓΓ CΓΔΖ”ΧΣ ‘“ΚΓΓΓΓΓΓΓΓΓΓΓΓ DΓΔBaCl2
17Θ°‘ΎœύΆ§ΧθΦΰœ¬Ϋχ––0.24gMg”κΔΌ0.2mol/L 80mLΒΡ―ΈΥαΘΜΔΎ0.2mol/L100mLΒΡ¥ΉΥαΖ¥”ΠΘ§œ¬Ν–ΥΒΖ®¥μΈσΒΡ «(ΓΓΓΓΓΓ )
AΘ°ΝΫΗωΖ¥”ΠΩΣ Φ ±ΒΡΖ¥”ΠΥΌ¬ ΘΚV(HCl)¥σ”ΎV(CH3COOH)
BΘ°Ζ¥”ΠΫχ––Άξ»Ϊ≤ζ…ζΒΡΤχΧεΒΡΈο÷ ΒΡΝΩΘΚn(HCl)Β»”Ύn(CH3COOH)
CΘ°‘Ύ…œ ω―ΈΥα»ή“Κ÷–Φ”»κ…ΌΝΩΒΡ¥ΉΥαΡΤΙΧΧεΘ§≤ΜΗΡ±δ≤ζ…ζΤχΧεΒΡΈο÷ ΒΡΝΩΘ§ΒΪΡή ΙΗΟΖ¥”ΠΜ·―ßΖ¥”ΠΥΌ¬ ΫΒΒΆΓΘ
DΘ°‘Ύ…œ ω¥ΉΥα»ή“Κ÷–Φ”»κ…ΌΝΩΝρΥαΆ≠»ή“ΚΘ§Ω…“‘Φ”ΩλΜ·―ßΖ¥”ΠΥΌ¬ Θ§ΒΪΤχΧεΒΡΈο÷ ΒΡΝΩ≤ΜΖΔ…ζΗΡ±δΓΘ
16. œ¬Ν–»ή“Κ÷–Θ§ΈΔΝΘ≈®Ε»ΙΊœΒ’ΐ»ΖΒΡ «(ΓΓΓΓΓΓ )
ΓΓ AΘ°Κ§”–NH4+ΓΔCl-ΓΔH+ΓΔOH-άκΉ”ΒΡ»ή“Κ÷–Θ§ΤδάκΉ”≈®Ε»“ΜΕ® «ΘΚc(Cl-)>c(NH4+)>c(H+)>c(OH-)
BΘ°pH=8ΒΡΑ±Υ°”ꬻ̷οßΒΡΜλΚœ»ή“Κ÷–ΘΚc(Cl-)>c(NH4+)
CΘ°0.1mol/L ΒΡNa2S»ή“Κ÷–ΘΚc(OH-)=c(H+)+c(HS-)+2c(H2S)
DΘ°pH=3ΒΡ“Μ‘ΣΥαΚΆpH=11ΒΡ“Μ‘Σ«ΩΦνΒ»ΧεΜΐΜλΚœΚσΒΡ»ή“Κ÷–ΘΚc(OH-)=c(H+)
15. Ρ≥»ή“Κ÷–Κ§”–ΝΫ÷÷»ή÷ NaClΚΆH2SO4Θ§ΥϋΟ«ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ3ΓΟ1ΓΘ”Ο ·ΡΪΉςΒγΦΪΒγΫβΗΟΜλΚœ»ή“Κ ±Θ§ΗυΨίΒγΦΪ≤ζΈοΘ§Ω…Οςœ‘Ζ÷ΈΣ»ΐΗωΫΉΕΈΓΘœ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ )
A.“θΦΪΉ‘ ΦΉ‘÷’÷ΜΈω≥ωH2 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓB.»ή“ΚpH≤ΜΕœ‘ω¥σΘ§ΉνΚσΈΣ7
C.ΒγΫβΉνΚσΫΉΕΈΈΣΒγΫβΥ° ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓD.―τΦΪœ»Έω≥ωCl2Θ§ΚσΈω≥ωO2
14Θ°œ¬Ν–Μ·―ßΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «(ΓΓ )
AΘ°‘ΎœΓΑ±Υ°÷–Ά®»κΙΐΝΩCO2:ΓΓ NH3ΓΛH2O+CO2=NH4++HCO3-
BΘ°…ΌΝΩSO2Ά®»κCa(ClO)2»ή“Κ÷–ΘΚSO2+H2O+Ca2++2ClO-=CaSO3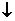 +2HClO
+2HClO
CΘ°”ΟœΓHNO3»ή“ΚFeSΙΧΧεΘΚFeS+2H+=Fe2++H2S
DΘ°«β―θΜ·ΗΤ»ή“Κ”κΒ»Έο÷ ΒΡΝΩΒΡœΓΝρΥαΜλΚœΘΚCa2++OH-+H++SO4
2- =CaSO4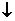 +H2O
+H2O
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com