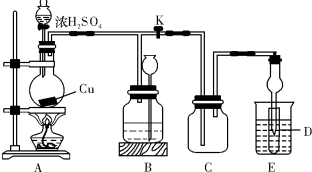
某校研究性学习小组同学在实验时把SO
2通入装有BaCl
2溶液的试管中,出现了白色浑浊物.
(1)实验小组的同学查阅了工具书上的相关数据,经过计算推导得出:即使把SO
2通入BaCl
2溶液中至饱和,也不可能生成BaSO
3,故白色浑浊物只能是BaSO
4.你认为所查阅的数据为:SO
2饱和溶液中各离子的浓度、SO
2的溶解度以及
BaSO3的溶度积或BaSO3的溶解度或Ksp(BaSO3)
BaSO3的溶度积或BaSO3的溶解度或Ksp(BaSO3)
.
(2)小组同学对白色浑浊物成分及产生原因进行了各种合理的假设,并分别设计实验验证假设如下:
|
假设 |
实验验证方法及现象 |
| 假设1 |
白色浑浊物是BaSO3. |
在白色浑浊物中加入过量盐酸,变澄清 在白色浑浊物中加入过量盐酸,变澄清 . |
| 假设2 |
白色浑浊物是BaSO4,造成原因是
BaCl2溶液中溶解的氧气把亚硫酸氧化成硫酸 BaCl2溶液中溶解的氧气把亚硫酸氧化成硫酸 . |
把BaCl2溶液煮沸,冷却后滴加苯液封,再通入SO2.出现轻微浑浊. |
| 假设3 |
白色浑浊物是BaSO4,造成原因是
SO2中混有空气,把亚硫酸氧化成硫酸 SO2中混有空气,把亚硫酸氧化成硫酸 . |
反应开始前,先向制取SO2的装置中通入纯净的CO2,再把产生的SO2通入BaCl2溶液中.不出现浑浊. |
请把上表填充完全.
(3)写出在验证假设2的实验时,溶液中发生的反应的化学方程式:
2SO2+O2+2H2O=2H2SO4或SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4
2SO2+O2+2H2O=2H2SO4或SO2+H2O=H2SO3、2H2SO3+O2=2H2SO4
、
H2SO4+BaCl2=BaSO4↓+2HCl
H2SO4+BaCl2=BaSO4↓+2HCl
;
(4)请你再提供一种假设.白色浑浊物是BaSO
4,造成原因是
BaCl2溶液中含有Ba(NO)3、HNO3、H2O2、Fe3+等均可
BaCl2溶液中含有Ba(NO)3、HNO3、H2O2、Fe3+等均可
.

 (2011?湖南二模)下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变混浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物.请回答下列问题:
(2011?湖南二模)下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变混浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物.请回答下列问题: