
题目列表(包括答案和解析)

(10分)阅读材料:过氧化钠在工业上有广泛的用途,常用做漂白剂、杀菌剂、消毒剂、去臭剂、氧化剂等。过氧化钠为淡黄色粉末,在空气中吸收水分和二氧化碳的同时放出氧气。与水反应,生成氢氧化钠和过氧化氢,由于反应放出大量的热,后者很快分解成水和氧气。过氧化钠能与稀酸反应。过氧化钠相对密度为2.805,难溶于乙醇,有氧化性,易引起燃烧爆炸,应避免与有机物和可燃物质接触。钠在氧气中燃烧可生成过氧化钠。
请回答下列问题:
(1)过氧化钠的物理性质(写两点) 、 ;
过氧化钠的化学性质(写两点) 、 。[来源:]
(2)下列有关过氧化钠的说法正确的是
A.过氧化钠应密封保存
B.过氧化钠可作供氧剂
C.生成过氧化钠的反应属于分解反应
D.在生成过氧化钠的反应中,氧气体现氧化性
(3)写出过氧化钠与水反应时,发生的所有化学反应的文字表达式 。
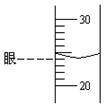
(4)欲量取一定量稀酸与过氧化钠反应。使用量筒量取液体时,视线要与量筒内液体__________保持水平,再读出所取液体的体积数。下图为量筒的一部分,该量筒中液体的体积读数为______mL。
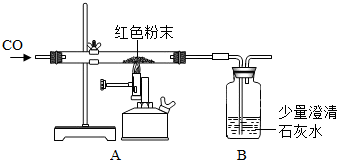
| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
| ||
| ||
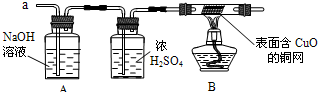
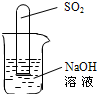
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | 试管中有大量的气泡产生,伸入的带火星的木条复燃 |
FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | 起催化作用的不是Cl- |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的 Fe(NO3)3溶液 ,并把带火星的木条伸入试管 |
试管中有大量气泡产生,带火星的木条复燃 |
起催化作用的是Fe3+ |
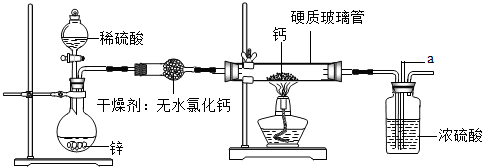
| 实验操作 | 实验现象 | 实验结论及解释 |
| ①取少量硬质玻璃管中的固体于试管中,滴入少量的水,收集产生的气体,并用燃着的木条点燃 | 气体燃烧,产生淡蓝色火焰 气体燃烧,产生淡蓝色火焰 |
有氢气生成 |
| ②继续向溶液中滴加酚酞 | 呈红色 | 生成 Ca(OH)2 Ca(OH)2 (填化学式) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com