
题目列表(包括答案和解析)
(8分)已知:①MnO4—
+e- MnO42―
(绿色)(强碱性条件)
MnO42―
(绿色)(强碱性条件)
②MnO4—+ 8H+ + 5e- Mn2+ (无色)+ 4H2O(强酸性条件)
Mn2+ (无色)+ 4H2O(强酸性条件)
(1)在KOH溶液中,KMnO4与K2SO3溶液发生反应, 写出反应的离子方程式 。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式 .
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,MnO4‑ 具有氧化性,最合适的亚铁盐是 (选填编号),可用来酸化KMnO4溶液的试剂是 (选填编号)
a. FeCl2 b. FeSO4 c.Fe(NO3)2 d稀硫酸 e. 盐酸 f. 硝酸
(4)向20 mL浓度为0.05mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4‑ 全部转化为Mn2+ ,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于 mL
(8分)已知:①MnO4— +e- MnO42―(绿色)(强碱性条件)
MnO42―(绿色)(强碱性条件)
②MnO4—+ 8H+ + 5e- Mn2+(无色)+ 4H2O(强酸性条件)
Mn2+(无色)+ 4H2O(强酸性条件)
(1)在KOH溶液中,KMnO4与K2SO3溶液发生反应, 写出反应的离子方程式 。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式 .
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,MnO4?具有氧化性,最合适的亚铁盐是 (选填编号),可用来酸化KMnO4溶液的试剂是 (选填编号)
a. FeCl2 b. FeSO4 c.Fe(NO3)2 d稀硫酸 e. 盐酸 f. 硝酸
(4)向20 mL浓度为0.05mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4?全部转化为Mn2+ ,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于 mL

| 2b |
| a |
| 2b |
| a |
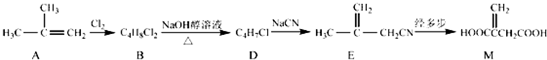
 +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O
+NaCl+H2O +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O
+NaCl+H2O

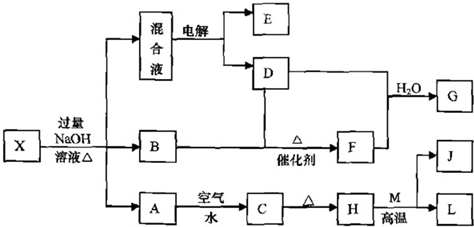
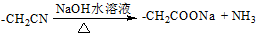 ,E经五步转成变成M的合成反应流程为:
,E经五步转成变成M的合成反应流程为: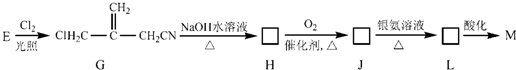

| NaOH水溶液 |
| △ |
 +NaCl+NH3
+NaCl+NH3
| NaOH水溶液 |
| △ |
 +NaCl+NH3
+NaCl+NH3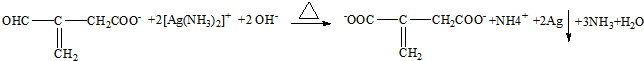
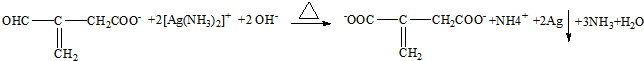
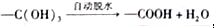 ,E经三步转变成M的合成反应流程为
,E经三步转变成M的合成反应流程为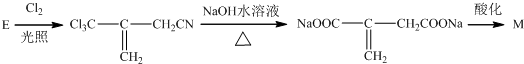



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com