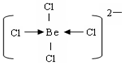
【化学一选修2化学与技术】
晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等.以下是工业上制取纯硅的一种方法.
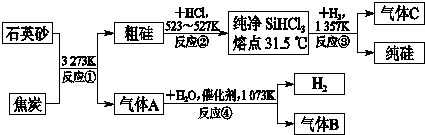
请回答下列问题(各元素用相应的元素符号表示):
(1)在上述生产过程中,属于置换反应的有
(填反应代号).
(2)利用反应③能制得纯硅的原因是
.
(3)化合物W的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂.将石英砂和纯碱按一定比例混合加热至1373~1623K反应,生成化合物W,其化学方程式是
.
(4)A、B、C三种气体在生产过程中可循环使用的是
(写化学式);在“节能减排”中作为减排目标的一种气体是
(写化学式);分别通入W溶液中能得到白色沉淀的气体是
(写化学式).
(5)工业上合成氨的原料H
2是先将焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H
2,提纯水煤气得到纯净的H
2的化学方程式为
、
、
.
(6)反应生成的气体只是A而不是B的原因是
.