
题目列表(包括答案和解析)
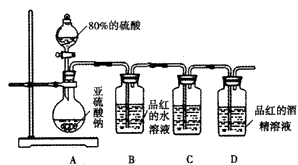
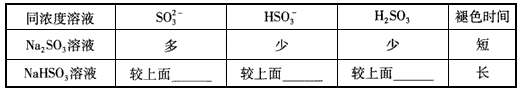
某研究性学习小组将15 mL氯气慢慢溶于1000 mL自来水,发现溶于自来水后的溶液黄绿色很浅,接近无色.为探究氯气溶于自来水中是否可与水反应,某同学作出如下假设:
①氯气溶于自来水,不与水反应;②氯气溶于自来水,可与水反应.
(1)甲同学(甲、乙为小组成员)设想用测定pH的方法探究以上假设.请你利用甲同学刚制得的液体,帮助甲同学设计实验方案.实验中可选用下列仪器、用品和药品:玻璃片、玻璃棒、pH试纸(含比色卡),石蕊试液、酚酞、蒸馏水、自来水、烧杯、胶头滴管、pH计(使用时将待测液加入烧杯中,把pH计插入待测液中,待读数稳定后,直接读取溶液的pH值).
写出实验步骤(不必填满,也可根据你的设计添加步骤④…),
①________________________________.
②________________________________.
③________________________________.
(2)乙同学设想选用AgNO3溶液探究上述问题,该设想是否正确,并解释原因.答:________________________________.
铝的氧化物是________氧化物,熔点________,硬度________,难溶于________,也不与水直接反应.既能与________又能与________的氧化物是两性氧化物.两性氢氧化物是指既能与________又能与________的氢氧化物,氢氧化铝就是________.
某研究性学习小组将15mL氯气慢慢溶于1000mL自来水,发现溶于自来水后的溶液黄绿色很浅,接近无色。为探究氯气溶于自来水中是否可与水反应,某同学做出如下假设:
①氯气溶于自来水,不与水反应; ②氯气溶于自来水,可与水反应。
(1)甲同学(甲、乙为小组成员)设想用测定pH的方法探究以上假设。请你利用甲同学刚制得的液体,帮助甲同学设计实验方案。实验中可选用下列仪器、用品和药品:玻璃片、玻璃棒、pH试纸(含比色卡),石蕊试液、酚酞、蒸馏水、自来水、烧杯、胶头滴管、pH计(使用时将待测液加入烧杯中,把pH计插入待测液中,待读数稳定后,直接读取溶液的pH值)。
写出实验步骤(不必填满,也可根据你的设计添加步骤④…),
①__________________________________________________________________。
②__________________________________________________________________。
③__________________________________________________________________。
(2)乙同学设想选用AgNO3溶液探究上述问题,该设想是否正确,并解释原因。答:
__________________________________________________________________。
实验目的 | 实验结果 | 结论 |
a.比较钠、镁、铝与水反应的难易程度 | 钠与_____________水剧烈反应;镁与水反应的条件是_____________,加热时反应剧烈程度也不如钠与冷水反应;铝与水反应不如钠、镁剧烈,即使加热,反应仍很缓慢 | 钠、镁、铝原子失电子能力:钠 ________镁_________铝 |
b.比较镁铝与同浓度盐酸反应的难易程度 | 与同浓度同体积盐酸反应时,剧烈程度:镁_____铝 | |
c.比较钠、镁、铝的最高价氧化物对应水化物的碱性强弱 | NaOH是___________碱;Mg(OH)2是_____________碱,只溶于酸而不与碱反应;Al(OH)3碱性最弱,是____________性氢氧化物,既可溶于酸又可溶于强碱 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com