
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
(±Ψ–ΓΧβ¬ζΖ÷12Ζ÷)
»γΆΦΘ®1Θ© «“Μ’ΐΖΫΧεΒΡ±μΟφ’ΙΩΣΆΦΘ§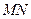 ΚΆ
ΚΆ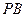 «ΝΫΧθΟφΕ‘Ϋ«œΏΘ§«κ‘ΎΆΦΘ®2Θ©ΒΡ’ΐΖΫΧε÷–ΫΪ
«ΝΫΧθΟφΕ‘Ϋ«œΏΘ§«κ‘ΎΆΦΘ®2Θ©ΒΡ’ΐΖΫΧε÷–ΫΪ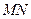 ΚΆ
ΚΆ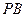 Μ≠≥ωά¥Θ§≤ΔΨΆ’βΗω’ΐΖΫΧεΫβΨωœ¬ΟφΈ Χβ.
Μ≠≥ωά¥Θ§≤ΔΨΆ’βΗω’ΐΖΫΧεΫβΨωœ¬ΟφΈ Χβ.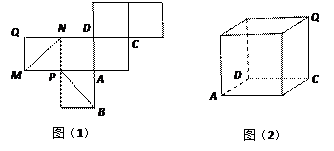
Θ®ΔώΘ©«σ÷ΛΘΚ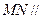 ΤΫΟφ
ΤΫΟφ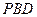 ΘΜ
ΘΜ
Θ®ΔρΘ©«σ÷ΛΘΚ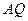 ΓΆΤΫΟφ
ΓΆΤΫΟφ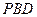 ΘΜ
ΘΜ
Θ®ΔσΘ©«σΕΰΟφΫ«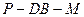 ΒΡ¥σ–ΓΘ°
ΒΡ¥σ–ΓΘ°
(±Ψ–ΓΧβ¬ζΖ÷12Ζ÷)
 »γΆΦΘ®1Θ© «“Μ’ΐΖΫΧεΒΡ±μΟφ’ΙΩΣΆΦΘ§
»γΆΦΘ®1Θ© «“Μ’ΐΖΫΧεΒΡ±μΟφ’ΙΩΣΆΦΘ§![]() ΚΆ
ΚΆ![]() «ΝΫΧθΟφΕ‘Ϋ«œΏΘ§«κ‘ΎΆΦΘ®2Θ©ΒΡ’ΐΖΫΧε÷–ΫΪ
«ΝΫΧθΟφΕ‘Ϋ«œΏΘ§«κ‘ΎΆΦΘ®2Θ©ΒΡ’ΐΖΫΧε÷–ΫΪ![]() ΚΆ
ΚΆ![]() Μ≠≥ωά¥Θ§≤ΔΨΆ’βΗω’ΐΖΫΧεΫβΨωœ¬ΟφΈ Χβ.
Μ≠≥ωά¥Θ§≤ΔΨΆ’βΗω’ΐΖΫΧεΫβΨωœ¬ΟφΈ Χβ.
Θ®ΔώΘ©«σ÷ΛΘΚ![]() ΤΫΟφ
ΤΫΟφ![]() ΘΜ
ΘΜ
Θ®ΔρΘ©«σ÷ΛΘΚ![]() ΓΆΤΫΟφ
ΓΆΤΫΟφ![]() ΘΜ
ΘΜ
Θ®ΔσΘ©«σΕΰΟφΫ«![]() ΒΡ¥σ–ΓΘ°
ΒΡ¥σ–ΓΘ°
Θ®±Ψ–ΓΧβ¬ζΖ÷12Ζ÷Θ©
‘Ύ“ΜΗω Β―ι÷–Θ§“Μ÷÷―Σ«ε±ΜΉΔ…δΒΫ500÷Μκύ σΧεΡΎΘ°Ήν≥θΘ§’β–©κύ σ÷–150÷Μ”–‘≤–ΈœΗΑϊΘ§250÷Μ”–Ά÷‘≤–ΈœΗΑϊΘ§100÷Μ”–≤ΜΙφ‘ρ–ΈΉ¥œΗΑϊΘ°±ΜΉΔ…δ’β÷÷―Σ«ε÷°ΚσΘ§ΟΜ”–“Μ÷ΜΨΏ”–‘≤–ΈœΗΑϊΒΡκύ σ±ΜΗ–»ΨΘ§50÷ΜΨΏ”–Ά÷‘≤–ΈœΗΑϊΒΡκύ σ±ΜΗ–»ΨΘ§ΨΏ”–≤ΜΙφ‘ρ–ΈΉ¥œΗΑϊΒΡκύ σ»Ϊ≤Ω±ΜΗ–»ΨΘ°ΗυΨί ‘―ιΫαΙϊΘ§ΙάΦΤΨΏ”–œ¬Ν–άύ–ΆΒΡœΗΑϊΒΡκύ σ±Μ’β÷÷―Σ«εΗ–»ΨΒΡΗ≈¬ ΘΚ
Θ®1Θ©‘≤–ΈœΗΑϊΘΜ
Θ®2Θ©Ά÷‘≤–ΈœΗΑϊΘΜ
Θ®3Θ©≤ΜΙφ‘ρ–ΈΉ¥œΗΑϊ.
ΙΊ”ΎΗΏΥΙœϊ»ΞΖ®ΒΡΟη ω¥μΈσΒΡ «
AΘ°ΗΏΥΙœϊ»ΞΖ® «“Μ÷÷ΥψΖ®
BΘ°ΗΏΥΙœϊ»ΞΖ®Ω…“‘Ϋβ»Έ“βΒΡΕΰ‘Σ“Μ¥ΈΖΫ≥ΧΉι
CΘ°ΗΏΥΙœϊ»ΞΖ® «ΫβΕΰ‘Σ“Μ¥ΈΖΫ≥ΧΉιΒΡΈ®“ΜΥψΖ®
DΘ°ΗΏΥΙœϊ»ΞΖ®≤ΜΡήΫβ“Μ‘ΣΕΰ¥ΈΖΫ≥Χ
±Ψ–ΓΧβ¬ζΖ÷12Ζ÷)ΗΏΕΰΦΕΡ≥¥Έ ΐ―ß≤β ‘÷–,ΥφΜζ¥”ΗΟΡξΦΕΥυ”–―ß…ζ÷–≥ι»ΓΝΥ100ΟϊΆ§―ßΒΡ ΐ―ß≥…Φ®(¬ζΖ÷150Ζ÷),Ψ≠Ά≥ΦΤ≥…Φ®‘Ύ ΒΡ”–6»Υ,‘Ύ
ΒΡ”–6»Υ,‘Ύ ΒΡ”–4»Υ.‘Ύ
ΒΡ”–4»Υ.‘Ύ ,
, Ης«χΦδΖ÷≤Φ«ιΩω»γ”“ΆΦΥυ ΨΒΡΤΒ¬ Ζ÷≤Φ÷±ΖΫΆΦ,»τ÷±ΖΫΆΦ÷–,
Ης«χΦδΖ÷≤Φ«ιΩω»γ”“ΆΦΥυ ΨΒΡΤΒ¬ Ζ÷≤Φ÷±ΖΫΆΦ,»τ÷±ΖΫΆΦ÷–, ΚΆ
ΚΆ Ε‘”Π–ΓΨΊ–ΈΗΏΕ»œύΒ»,«“
Ε‘”Π–ΓΨΊ–ΈΗΏΕ»œύΒ»,«“ Ε‘”Π–ΓΨΊ–ΈΗΏΕ»”÷«ΓΈΣ
Ε‘”Π–ΓΨΊ–ΈΗΏΕ»”÷«ΓΈΣ Ε‘”Π–ΓΨΊ–ΈΗΏΕ»ΒΡ“ΜΑκ.
Ε‘”Π–ΓΨΊ–ΈΗΏΕ»ΒΡ“ΜΑκ.
(1)»ΖΕ®ΆΦ÷– ΒΡ÷Β;
ΒΡ÷Β;
(2)…ηΒΟΖ÷‘Ύ110Ζ÷“‘…œ(Κ§110Ζ÷)ΈΣ”≈–ψ,‘ρ’β¥Έ≤β ‘ΒΡ”≈–ψ¬ «Εύ…Ό?
(3)Ρ≥ΑύΙ≤”–―ß…ζ50»Υ,»τ“‘ΗΟ¥ΈΆ≥ΦΤΫαΙϊΈΣ“άΨί,œ÷ΥφΜζ¥”ΗΟΑύ―ß…ζ÷–≥ι≥ω3»Υ, ‘ρ÷Ν…Ό≥ιΒΫ“ΜΟϊ ΐ―ß≥…Φ®”≈–ψ―ß…ζΒΡΗ≈¬ «Εύ…Ό?
ΓΨΧβΈΡΓΩ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com