
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)

(1)ЯШЙиБеЛюШћaЃЌНЋ6.4 gЭЦЌКЭ12 mL18 molЁЄL-1ЕФХЈСђЫсЗХдкдВЕзЩеЦПжаЙВШШжСЗДгІЭъГЩЃЌЗЂЯжЩеЦПжаЛЙгаЭЦЌЪЃгрЁЃдйДђПЊЛюШћaЃЌНЋЦјЧђжаЕФбѕЦјЛКЛКМЗШыдВЕзЩеЦПЃЌзюКѓЭЦЌЭъШЋЯћЪЇЁЃ
ЂйаДГіЩЯЪіЙ§ГЬжаЩеЦПФкЗЂЩњЕФЛЏбЇЗНГЬЪНЃК
ДђПЊЛюШћaжЎЧА_________________________________________________________ЃЌ
ДђПЊЛюШћaжЎКѓ_________________________________________________________ЃЌ
ЂкBЪЧгУРДЪеМЏЪЕбщжаВњЩњЕФЦјЬхЕФзАжУЃЌЕЋМЏЦјЦПФкЕФЕМЙмЮДЛШЋЃЌЧыжБНгдкД№ЬтОэЕФЭМЩЯАбЕМЙмВЙГфЭъећЁЃ
(2)ЪЕМЪЩЯЃЌдкДђПЊЛюШћaжЎЧАСђЫсШдгаЪЃгрЁЃЮЊЖЈСПВтЖЈгрЫсЕФЮяжЪЕФСПЃЌМзЁЂввСНбЇЩњНјааСЫШчЯТЩшМЦЃК
ЂйМзбЇЩњЩшМЦЗНАИЪЧЃКЯШВтЖЈЭгыХЈСђЫсЗДгІВњЩњSO2ЕФСПЃЌдйЭЈЙ§МЦЫуШЗЖЈгрЫсЕФЮяжЪЕФСПЁЃЫћВтЖЈSO2ЕФЗНЗЈЪЧНЋзАжУAВњЩњЕФЦјЬхЛКЛКЭЈЙ§зАжУDЃЌДгЖјВтГізАжУAВњЩњЦјЬхЕФЬхЛ§(вбелЫуГЩБъзМзДПі)ЁЃФуШЯЮЊМзбЇЩњЩшМЦЕФЪЕбщЗНАИжаDзАжУжаЕФЪдМСЮЊ___________(ЬюЛЏбЇЪН)ЁЃ
ЂкввбЇЩњЩшМЦЕФЗНАИЪЧЃКНЋЗДгІКѓЕФШмвКРфШДКѓШЋВПвЦШыЕНЩеБжаЯЁЪЭЃЌВЂАДе§ШЗВйзїХфжЦ100 mLШмвКЃЌдйШЁ20 mLгкзЖаЮЦПжаЃЌгУ_______________________зїжИЪОМСЃЌгУБъзМЧтбѕЛЏФЦШмвКНјааЕЮЖЈЁВвбжЊЃКCu(OH)2ПЊЪМГСЕэЕФpHдМЮЊ5ЁГЃЌбЁдёИУжИЪОМСЕФРэгЩЮЊ____________________________________ЃЛдйЧѓГігрЫсЕФЮяжЪЕФСПЃЌШєКФШЅa molЁЄL-1ЧтбѕЛЏФЦШмвКb mLЃЌдђдгрЫсЕФЮяжЪЕФСПЮЊ_________ molЁЃ(гУКЌaЁЂbЕФБэДяЪНРДБэЪО)
ФГЛЏбЇПЮЭтаЫШЄаЁзщЮЊЬНОПЭИњХЈСђЫсЕФЗДгІЧщПіЃЌЩшМЦСЫЯТЭМЫљЪОзАжУНјаагаЙиЪЕбщЃК

(1)ЯШЙиБеЛюШћaЃЌНЋ6.4 gЭЦЌКЭ10 mL 18 mol/LЕФХЈСђЫсЗХдкдВЕзЩеЦПжаЙВШШжСЗДгІЭъГЩЃЌЗЂЯжЩеЦПжаЛЙгаЭЦЌЪЃгрЁЃдйДђПЊЛюШћaЃЌНЋЦјЧђжаЕФбѕЦјЛКЛКМЗШыдВЕзЩеЦПЃЌзюКѓЭЦЌЭъШЋЯћЪЇЁЃ
ЂйаДГіЩЯЪіЙ§ГЬжадВЕзЩеЦПФкЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ДђПЊЛюШћaжЎЧА___________________________________________________ЃЛ
ДђПЊЛюШћaжЎКѓ___________________________________________________ЁЃ
ЂкBЪЧгУРДЪеМЏЪЕбщжаВњЩњЕФЦјЬхЕФзАжУЃЌЕЋМЏЦјЦПФкЕФЕМЙмЮДЛШЋЃЌЧыжБНгдкЭМЩЯАбЕМЙмВЙГфЭъећЁЃ
(2)ЪЕМЪЩЯЃЌдкДђПЊЛюШћaжЎЧАСђЫсШдгаЪЃгрЁЃЮЊЖЈСПВтЖЈгрЫсЕФЮяжЪЕФСПЃЌМзЁЂввСНбЇЩњНјааСЫШчЯТЩшМЦЃК
ЂйМзбЇЩњЩшМЦЕФЗНАИЪЧЃКЯШВтЖЈЭгыХЈСђЫсЗДгІВњЩњSO2ЕФСПЃЌдйЭЈЙ§МЦЫуШЗЖЈгрЫсЕФЮяжЪЕФСПЁЃЫћВтЖЈSO2ЕФЗНЗЈЪЧНЋзАжУAВњЩњЕФЦјЬхЛКЛКЭЈЙ§зАжУDЃЌДгЖјВтГізАжУAВњЩњЦјЬхЕФЬхЛ§(вбелЫуГЩБъзМзДПіЯТ)ЁЃФуШЯЮЊМзбЇЩњЩшМЦЕФЪЕбщЗНАИжаDзАжУжаЕФЪдМСЮЊ______________________(ЬюЛЏбЇЪН)ЁЃ
ЂкввбЇЩњЩшМЦЕФЗНАИЪЧЃКНЋЗДгІКѓЕФШмвКРфШДКѓШЋВПвЦШыЕНЩеБжаЯЁЪЭЃЌВЂАДе§ШЗВйзїХфжЦ100 mLШмвКЃЌдйШЁ20 mLгкзЖаЮЦПжаЃЌгУ________зїжИЪОМСЃЌгУБъзМЧтбѕЛЏФЦШмвКНјааЕЮЖЈ[вбжЊЃКCu(OH)2ПЊЪМГСЕэЕФpHдМЮЊ5]ЃЌбЁдёИУжИЪОМСЕФРэгЩЮЊ__________________________________________________ЃЛдйЧѓГігрЫсЕФЮяжЪЕФСПЃЌШєКФШЅa mol/LЧтбѕЛЏФЦШмвКb mLЃЌдђдгрЫсЕФЮяжЪЕФСПЮЊ________mol(гУКЌaЁЂbЕФБэДяЪНРДБэЪО)ЁЃ
ФГЛЏбЇПЮЭтаЫШЄаЁзщЮЊЬНОПЭИњХЈСђЫсЕФЗДгІЧщПіЃЌЩшМЦСЫЯТЭМЫљЪОзАжУНјаагаЙиЪЕбщЃК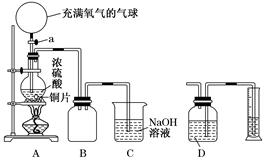
(1)ЯШЙиБеЛюШћaЃЌНЋ6.4 gЭЦЌКЭ10 mL 18 mol/LЕФХЈСђЫсЗХдкдВЕзЩеЦПжаЙВШШжСЗДгІЭъГЩЃЌЗЂЯжЩеЦПжаЛЙгаЭЦЌЪЃгрЁЃдйДђПЊЛюШћaЃЌНЋЦјЧђжаЕФбѕЦјЛКЛКМЗШыдВЕзЩеЦПЃЌзюКѓЭЦЌЭъШЋЯћЪЇЁЃ
ЂйаДГіЩЯЪіЙ§ГЬжадВЕзЩеЦПФкЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ДђПЊЛюШћaжЎЧА___________________________________________________ЃЛ
ДђПЊЛюШћaжЎКѓ___________________________________________________ЁЃ
ЂкBЪЧгУРДЪеМЏЪЕбщжаВњЩњЕФЦјЬхЕФзАжУЃЌЕЋМЏЦјЦПФкЕФЕМЙмЮДЛШЋЃЌЧыжБНгдкЭМЩЯАбЕМЙмВЙГфЭъећЁЃ
(2)ЪЕМЪЩЯЃЌдкДђПЊЛюШћaжЎЧАСђЫсШдгаЪЃгрЁЃЮЊЖЈСПВтЖЈгрЫсЕФЮяжЪЕФСПЃЌМзЁЂввСНбЇЩњНјааСЫШчЯТЩшМЦЃК
ЂйМзбЇЩњЩшМЦЕФЗНАИЪЧЃКЯШВтЖЈЭгыХЈСђЫсЗДгІВњЩњSO2ЕФСПЃЌдйЭЈЙ§МЦЫуШЗЖЈгрЫсЕФЮяжЪЕФСПЁЃЫћВтЖЈSO2ЕФЗНЗЈЪЧНЋзАжУAВњЩњЕФЦјЬхЛКЛКЭЈЙ§зАжУDЃЌДгЖјВтГізАжУAВњЩњЦјЬхЕФЬхЛ§(вбелЫуГЩБъзМзДПіЯТ)ЁЃФуШЯЮЊМзбЇЩњЩшМЦЕФЪЕбщЗНАИжаDзАжУжаЕФЪдМСЮЊ______________________(ЬюЛЏбЇЪН)ЁЃ
ЂкввбЇЩњЩшМЦЕФЗНАИЪЧЃКНЋЗДгІКѓЕФШмвКРфШДКѓШЋВПвЦШыЕНЩеБжаЯЁЪЭЃЌВЂАДе§ШЗВйзїХфжЦ100 mLШмвКЃЌдйШЁ20 mLгкзЖаЮЦПжаЃЌгУ________зїжИЪОМСЃЌгУБъзМЧтбѕЛЏФЦШмвКНјааЕЮЖЈ[вбжЊЃКCu(OH)2ПЊЪМГСЕэЕФpHдМЮЊ5]ЃЌбЁдёИУжИЪОМСЕФРэгЩЮЊ__________________________________________________ЃЛдйЧѓГігрЫсЕФЮяжЪЕФСПЃЌШєКФШЅa mol/LЧтбѕЛЏФЦШмвКb mLЃЌдђдгрЫсЕФЮяжЪЕФСПЮЊ________mol(гУКЌaЁЂbЕФБэДяЪНРДБэЪО)ЁЃ
(11Зж)ФГЛЏбЇПЮЭтаЫШЄаЁзщЮЊЬНОПЭИњХЈСђЫсЕФЗДгІЧщПіЃЌЩшМЦСЫЯТЭМЫљЪОзАжУНјаага
ЙиЪЕбщЃК
ЃЈ1ЃЉЯШЙиБеЛюШћaЃЌНЋ6.4 gЭЦЌКЭ12 mL 18 mol/LЕФХЈСђЫсЗХдкдВЕзЩеЦПжаЙВШШжСЗДгІЭъГЩЃЌЗЂЯжЩеЦПжаЛЙгаЭЦЌЪЃгрЃЎдйДђПЊЛюШћaЃЌНЋЦјЧђжаЕФбѕЦјЛКЛКМЗШыдВЕзЩеЦПЃЌзюКѓЭЦЌЭъШЋЯћЪЇЃЎ
ЂйаДГіЩЯЪіЙ§ГЬжаЩеЦПФкЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ДђПЊЛюШћaжЎЧА ЃЛ
ДђПЊЛюШћaжЎКѓ ЁЃ
ЂкBЪЧгУРДЪеМЏЪЕбщжаВњЩњЕФЦјЬхЕФзАжУЃЌЕЋМЏЦјЦПФкЕФЕМЙмЮДЛШЋЃЌЧыжБНгдкЭМЩЯАбЕМЙмВЙГфЭъећЁЃ
ЃЈ2ЃЉЪЕМЪЩЯЃЌдкДђПЊЛюШћaжЎЧАСђЫсШдгаЪЃгрЁЃЮЊЖЈСПВтЖЈгрЫсЕФЮяжЪЕФСПЃЌМзЁЂввСНбЇЩњНјааСЫШчЯТЩшМЦЃК
ЂйМзбЇЩњЩшМЦЗНАИЪЧЃКЯШВтЖЈЭгыХЈСђЫсЗДгІВњЩњSO2ЕФСПЃЌдйЭЈЙ§МЦЫуШЗЖЈгрЫсЕФЮяжЪЕФСПЁЃЫћВтЖЈSO2ЕФЗНЗЈЪЧНЋзАжУAВњЩњЕФЦјЬхЛКЛКЭЈЙ§зАжУDЃЌДгЖјВтГізАжУAВњЩњЦјЬхЕФЬхЛ§(вбелЫуГЩБъзМзДПі)ЁЃФуШЯЮЊМзбЇЩњЩшМЦЕФЪЕбщЗНАИжаDзАжУжаЪдМСЮЊЃК (ЬюЛЏбЇЪН)ЁЃ
ЂкввбЇЩњЩшМЦЕФЗНАИЪЧЃКНЋЗДгІКѓЕФШмвКРфШДКѓШЋВПвЦШыЕНЩеБжаЯЁЪЭЃЌВЂАДе§ШЗВйзїХфжЦ100 mLШмвКЃЌдйШЁ20 mLгкзЖаЮЦПжаЃЌгУ зїжИЪОМСЃЌгУБъзМЧтбѕЛЏФЦШмвКНјааЕЮЖЈ[вбжЊЃКCu(OH)2ПЊЪМГСЕэЕФpHдМЮЊ5]ЃЌбЁдёИУжИЪОМСЕФРэгЩЮЊ ЃЌдйЧѓГігрЫсЕФЮяжЪЕФСПЃЌШєКФШЅa mol/LЧтбѕЛЏФЦШмвКb mLЃЌдђдгрЫсЕФЮяжЪЕФСПЮЊ mol(гУКЌaЁЂbЕФБэДяЪНРДБэЪО)ЁЃ
(11Зж)ФГЛЏбЇПЮЭтаЫШЄаЁзщЮЊЬНОПЭИњХЈСђЫсЕФЗДгІЧщПіЃЌЩшМЦСЫЯТЭМЫљЪОзАжУНјаага
ЙиЪЕбщЃК

ЃЈ1ЃЉЯШЙиБеЛюШћaЃЌНЋ6.4 gЭЦЌКЭ12 mL 18 mol/LЕФХЈСђЫсЗХдкдВЕзЩеЦПжаЙВШШжСЗДгІЭъГЩЃЌЗЂЯжЩеЦПжаЛЙгаЭЦЌЪЃгрЃЎдйДђПЊЛюШћaЃЌНЋЦјЧђжаЕФбѕЦјЛКЛКМЗШыдВЕзЩеЦПЃЌзюКѓЭЦЌЭъШЋЯћЪЇЃЎ
ЂйаДГіЩЯЪіЙ§ГЬжаЩеЦПФкЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃК
ДђПЊЛюШћaжЎЧА ЃЛ
ДђПЊЛюШћaжЎКѓ ЁЃ
ЂкBЪЧгУРДЪеМЏЪЕбщжаВњЩњЕФЦјЬхЕФзАжУЃЌЕЋМЏЦјЦПФкЕФЕМЙмЮДЛШЋЃЌЧыжБНгдкЭМЩЯАбЕМЙмВЙГфЭъећЁЃ
ЃЈ2ЃЉЪЕМЪЩЯЃЌдкДђПЊЛюШћaжЎЧАСђЫсШдгаЪЃгрЁЃЮЊЖЈСПВтЖЈгрЫсЕФЮяжЪЕФСПЃЌМзЁЂввСНбЇЩњНјааСЫШчЯТЩшМЦЃК
ЂйМзбЇЩњЩшМЦЗНАИЪЧЃКЯШВтЖЈЭгыХЈСђЫсЗДгІВњЩњSO2ЕФСПЃЌдйЭЈЙ§МЦЫуШЗЖЈгрЫсЕФЮяжЪЕФСПЁЃЫћВтЖЈSO2ЕФЗНЗЈЪЧНЋзАжУAВњЩњЕФЦјЬхЛКЛКЭЈЙ§зАжУDЃЌДгЖјВтГізАжУAВњЩњЦјЬхЕФЬхЛ§(вбелЫуГЩБъзМзДПі)ЁЃФуШЯЮЊМзбЇЩњЩшМЦЕФЪЕбщЗНАИжаDзАжУжаЪдМСЮЊЃК (ЬюЛЏбЇЪН)ЁЃ
ЂкввбЇЩњЩшМЦЕФЗНАИЪЧЃКНЋЗДгІКѓЕФШмвКРфШДКѓШЋВПвЦШыЕНЩеБжаЯЁЪЭЃЌВЂАДе§ШЗВйзїХфжЦ100 mLШмвКЃЌдйШЁ20 mLгкзЖаЮЦПжаЃЌгУ зїжИЪОМСЃЌгУБъзМЧтбѕЛЏФЦШмвКНјааЕЮЖЈ[вбжЊЃКCu(OH)2ПЊЪМГСЕэЕФpHдМЮЊ5]ЃЌбЁдёИУжИЪОМСЕФРэгЩЮЊ ЃЌдйЧѓГігрЫсЕФЮяжЪЕФСПЃЌШєКФШЅa mol/LЧтбѕЛЏФЦШмвКb mLЃЌдђдгрЫсЕФЮяжЪЕФСПЮЊ mol(гУКЌaЁЂbЕФБэДяЪНРДБэЪО)ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com