
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ12ЗжЃЉФмдДЖЬШБЪЧШЫРрЩчЛсУцСйЕФжиДѓЮЪЬтЁЃМзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃЙЄвЕЩЯКЯГЩМзДМЕФЗДгІЮЊЃКCO(g)ЃЋ2H2(g)CH3OH(g)ЃЛІЄH
ЃЈ1ЃЉвбжЊЃЌИУЗДгІдк300ЁцЃЌ5MPaЬѕМўЯТФмздЗЂНјааЃЌдђІЄH 0ЃЌЁїS 0 ЃЈЬюЁАЃМЃЌЃОЛђЃНЁБЃЉЁЃ
ЃЈ2ЃЉдк300ЁцЃЌ5MPaЬѕМўЯТЃЌНЋ0.20molЕФ COгы0.58mol H2ЕФЛьКЯЦјЬхГфШы2LУмБеШнЦїЗЂЩњЗДгІЃЌЗДгІЙ§ГЬжаМзДМЕФЮяжЪЕФСПХЈЖШЫцЪБМфЕФБфЛЏШчЭМЫљЪОЁЃ
Ђйдк0ЁЋ2minФкЃЌвдH2БэЪОЕФЦНОљЗДгІЫйТЪЮЊ molЁЄL-1ЁЄs-1ЁЃ
ЂкСаЪНМЦЫу300ЁцЪБИУЗДгІЕФЦНКтГЃЪ§K = ЁЃ
Ђл300ЁцЪБЃЌНЋ0.50mol COЁЂ1.00mol H2КЭ1.00 molCH3OHГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌДЫЪБЗДгІНЋ ЁЃ
AЃЎЯђе§ЗНЯђвЦЖЏ BЃЎЯђФцЗНЯђвЦЖЏ CЃЎДІгкЦНКтзДЬЌ DЃЎЮоЗЈХаЖЯ
ЂмЯТСаДыЪЉПЩдіМгМзДМВњТЪЕФЪЧ
AЃЎбЙЫѕШнЦїЬхЛ§ BЃЎНЋCH3OH(g)ДгЬхЯЕжаЗжРы
CЃЎГфШыHeЃЌЪЙЬхЯЕзмбЙЧПдіДѓ DЃЎдйГфШы0.20mol COКЭ0.58mol H2
ЃЈ3ЃЉШєЦфЫќЬѕМўВЛБфЃЌЪЙЗДгІдк500ЁцЯТНјааЃЌдкЭМжазїГіМзДМЕФЮяжЪЕФСПХЈЖШЫцЪБМфЕФБфЛЏЕФЪОвтЭМЁЃ
ЁОНтЮіЁПЃЈ1ЃЉИљОнЗДгІЕФЬиЕуПЩжЊЁїSаЁгк0ЃЌвђЮЊЗДгІдк300ЁцЃЌ5MPaЬѕМўЯТФмздЗЂНјааЃЌЫљвдИљОнЁїGЃНЁїHЃTЁЄЁїSПЩжЊЗДгІЪЧЗХШШЗДгІЁЃ
ЃЈ2ЃЉЂйЗДгІЫйТЪЭЈГЃгУЕЅЮЛЪБМфФкХЈЖШЕФБфЛЏСПРДБэЪОЃЌИљОнЭМЯёПЩжЊЗДгІНјааЕН2minЪБМзДМ
ЕФХЈЖШВЛдйЗЂЩњБфЛЏЃЌЦНКтЪБМзДМЕФЮяжЪЕФСПЪЧ0.04molЃЌдђЯћКФЧтЦјЪЧ0.08molЃЌЫљвддк0ЁЋ2min
ФкЃЌвдH2БэЪОЕФЦНОљЗДгІЫйТЪЮЊ![]() ЁЃ
ЁЃ
ЂкЦНКтЪБЧтЦјЕФХЈЖШЪЧ![]() ЃЌCOЕФЦНКтХЈЖШЪЧ
ЃЌCOЕФЦНКтХЈЖШЪЧ
![]() ,ЫљвдИУЮТЖШЯТЕФЦНКтГЃЪ§ЮЊ
,ЫљвдИУЮТЖШЯТЕФЦНКтГЃЪ§ЮЊ![]() ЁЃ
ЁЃ
Ђл300ЁцЪБЃЌНЋ0.50mol COЁЂ1.00mol H2КЭ1.00 molCH3OHГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌДЫЪБЫќУЧЕФХЈЖШЗжБ№ЮЊ0.25mol/LЁЂ0.50mol/LЁЂЁЂ0.50mol/LЃЌвђЮЊ![]() ЃО4ЃЌЫљвдЗДгІЯђФцЗДгІЗНЯђвЦЖЏЁЃ
ЃО4ЃЌЫљвдЗДгІЯђФцЗДгІЗНЯђвЦЖЏЁЃ
ЂмбЙЫѕЬхЛ§ЃЌбЙЧПдіДѓЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЁЃбЁЯюBЪЧНЕЕЭЩњГЩЮяХЈЖШЃЌЦНКтвВЯђе§ЗДгІЗН
ЯђвЦЖЏЁЃГфШыHeЃЌЪЙЬхЯЕзмбЙЧПдіДѓЃЌЕЋЮяжЪЕЋХЈЖШУЛгаБфЛЏЃЌЫљвдЦНКтВЛвЦЖЏЁЃдйГфШы0.20mol
COКЭ0.58mol H2ЃЌЯрЕБгкдіДѓЬхЯЕЕФбЙЧПЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌЫљвдД№АИЪЧABDЁЃ
ЃЈ3ЃЉвђЮЊЗДгІЪЧЗХШШЗДгІЃЌЫљвдЩ§ИпЮТЖШЦНКтЯђФцЗДгІЗНЯђвЦЖЏЃЌЕЋЗДгІЫйТЪЛсМгПьЃЌЫљвдЭМ
ЯёЮЊ
ЃЈ12ЗжЃЉФмдДЖЬШБЪЧШЫРрЩчЛсУцСйЕФжиДѓЮЪЬтЁЃМзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃЙЄвЕЩЯКЯГЩМзДМЕФЗДгІЮЊЃКCO(g)ЃЋ2H2(g) CH3OH(g)ЃЛІЄH
CH3OH(g)ЃЛІЄH
ЃЈ1ЃЉвбжЊЃЌИУЗДгІдк300ЁцЃЌ5MPaЬѕМўЯТФмздЗЂНјааЃЌдђІЄH 0ЃЌЁїS 0 ЃЈЬюЁАЃМЃЌЃОЛђЃНЁБЃЉЁЃ
ЃЈ2ЃЉдк300ЁцЃЌ5MPaЬѕМўЯТЃЌНЋ0.20molЕФ COгы0.58mol H2ЕФЛьКЯЦјЬхГфШы2LУмБеШнЦїЗЂЩњЗДгІЃЌЗДгІЙ§ГЬжаМзДМЕФЮяжЪЕФСПХЈЖШЫцЪБМфЕФБфЛЏШчЭМЫљЪОЁЃ

Ђйдк0ЁЋ2minФкЃЌвдH2БэЪОЕФЦНОљЗДгІЫйТЪЮЊ molЁЄL-1ЁЄs-1 ЁЃ
ЂкСаЪНМЦЫу300ЁцЪБИУЗДгІЕФЦНКтГЃЪ§K = ЁЃ
Ђл300ЁцЪБЃЌНЋ0.50mol COЁЂ1.00mol H2КЭ1.00 mol CH3OHГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌДЫЪБЗДгІНЋ ЁЃ
AЃЎЯђе§ЗНЯђвЦЖЏ BЃЎЯђФцЗНЯђвЦЖЏ CЃЎДІгкЦНКтзДЬЌ DЃЎЮоЗЈХаЖЯ
ЂмЯТСаДыЪЉПЩдіМгМзДМВњТЪЕФЪЧ
AЃЎбЙЫѕШнЦїЬхЛ§ BЃЎНЋCH3OH(g)ДгЬхЯЕжаЗжРы
CЃЎГфШыHeЃЌЪЙЬхЯЕзмбЙЧПдіДѓ DЃЎдйГфШы0.20mol COКЭ0.58mol H2
ЃЈ3ЃЉШєЦфЫќЬѕМўВЛБфЃЌЪЙЗДгІдк500ЁцЯТНјааЃЌдкЭМжазїГіМзДМЕФЮяжЪЕФСПХЈЖШЫцЪБМфЕФБфЛЏЕФЪОвтЭМЁЃ
ЁОНтЮіЁПЃЈ1ЃЉИљОнЗДгІЕФЬиЕуПЩжЊЁїSаЁгк0ЃЌвђЮЊЗДгІдк300ЁцЃЌ5MPaЬѕМўЯТФмздЗЂНјааЃЌЫљвдИљОнЁїGЃНЁїHЃTЁЄЁїSПЩжЊЗДгІЪЧЗХШШЗДгІЁЃ
ЃЈ2ЃЉЂйЗДгІЫйТЪЭЈГЃгУЕЅЮЛЪБМфФкХЈЖШЕФБфЛЏСПРДБэЪОЃЌИљОнЭМЯёПЩжЊЗДгІНјааЕН2minЪБМзДМ
ЕФХЈЖШВЛдйЗЂЩњБфЛЏЃЌЦНКтЪБМзДМЕФЮяжЪЕФСПЪЧ0.04molЃЌдђЯћКФЧтЦјЪЧ0.08molЃЌЫљвддк0ЁЋ2min
ФкЃЌвдH2БэЪОЕФЦНОљЗДгІЫйТЪЮЊ ЁЃ
ЁЃ
ЂкЦНКтЪБЧтЦјЕФХЈЖШЪЧ ЃЌCOЕФЦНКтХЈЖШЪЧ
ЃЌCOЕФЦНКтХЈЖШЪЧ
 ,ЫљвдИУЮТЖШЯТЕФЦНКтГЃЪ§ЮЊ
,ЫљвдИУЮТЖШЯТЕФЦНКтГЃЪ§ЮЊ ЁЃ
ЁЃ
Ђл300ЁцЪБЃЌНЋ0.50mol COЁЂ1.00mol H2КЭ1.00 mol
CH3OHГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌДЫЪБЫќУЧЕФХЈЖШЗжБ№ЮЊ0.25mol/LЁЂ0.50mol/LЁЂЁЂ0.50mol/LЃЌвђЮЊ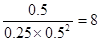 ЃО4ЃЌЫљвдЗДгІЯђФцЗДгІЗНЯђвЦЖЏЁЃ
ЃО4ЃЌЫљвдЗДгІЯђФцЗДгІЗНЯђвЦЖЏЁЃ
ЂмбЙЫѕЬхЛ§ЃЌбЙЧПдіДѓЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЁЃбЁЯюBЪЧНЕЕЭЩњГЩЮяХЈЖШЃЌЦНКтвВЯђе§ЗДгІЗН
ЯђвЦЖЏЁЃГфШыHeЃЌЪЙЬхЯЕзмбЙЧПдіДѓЃЌЕЋЮяжЪЕЋХЈЖШУЛгаБфЛЏЃЌЫљвдЦНКтВЛвЦЖЏЁЃдйГфШы0.20mol
COКЭ0.58mol H2ЃЌЯрЕБгкдіДѓЬхЯЕЕФбЙЧПЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЃЌЫљвдД№АИЪЧABDЁЃ
ЃЈ3ЃЉвђЮЊЗДгІЪЧЗХШШЗДгІЃЌЫљвдЩ§ИпЮТЖШЦНКтЯђФцЗДгІЗНЯђвЦЖЏЃЌЕЋЗДгІЫйТЪЛсМгПьЃЌЫљвдЭМ
ЯёЮЊ

ЃЈ13ЗжЃЉЯТБэЮЊдЊЫижмЦкБэжаЧАЫФжмЦкЕФВПЗждЊЫиЃЈДгзѓЕНгвАДдзгађЪ§ЕндіХХСаЃЌВПЗжЩцМАЕНЕФдЊЫиЮДИјГідЊЫиЗћКХЃЉЃЌИљОнвЊЧѓЛиД№ЯТСаИїаЁЬтЃК
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЁЁ |
ЁЁ |
|
|
|
|
|
|
|
|
|
|
ЁЁ |
|
|
|
|
ЁЁ |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
ЁЁ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЃЈ1ЃЉдквдЩЯБэИёжаЫљгадЊЫиРяЛљЬЌдзгЕФЕчзгХХВМжа4sЙьЕРЩЯжЛга1ИіЕчзгЕФдЊЫига ЃЈЬюдЊЫиУћГЦЃЉЁЃ
ЃЈ2ЃЉИљОндЊЫидзгЕФЭтЮЇЕчзгХХВМЕФЬиеїЃЌПЩНЋдЊЫижмЦкБэЧАЫФжмЦкдЊЫиЗжГЩ4ИіЧјгђЃЌЗжБ№ЮЊsЧјЁЂpЧјЁЂdЧјЁЂdsЧјЃЌЃЌдђЪєгкsЧјЕФдЊЫига жжЃЌЪєгкdЧјЕФдЊЫига жжЁЃЕкЖўжмЦкдЊЫижаГ§NeЭтЕчИКадгЩИпЕНЕЭЕФШ§жждЊЫивРДЮЪЧ ,ЕчРыФмгЩИпЕНЕЭЕФШ§жждЊЫивРДЮЪЧ ЁЃ
ЃЈ3ЃЉMnЁЂFeОљЮЊЕкЫФжмЦкЙ§ЖЩдЊЫиЃЌСНдЊЫиЕФВПЗжЕчРыФмЪ§ОнСагкЯТБэЃК
|
дЊЫи |
Mn |
Fe |
|
|
ЕчРыФм ЃЈ kJЁЄmolЃ1ЃЉ |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
3248 |
2957 |
ЛиД№ЯТСаЮЪЬтЃК
MnдЊЫиЕФЕчзгХХВМЪНЮЊ____________________________________ЃЌ
Fe2+ЕФЕчзгХХВМЭМЮЊ__________________________
БШНЯСНдЊЫиЕФI2ЁЂI3ПЩжЊЃЌЦјЬЌMn2+дйЪЇШЅвЛИіЕчзгБШЦјЬЌFe2+дйЪЇШЅвЛИі ЕчзгФбЁЃЖдДЫЃЌФуЕФНтЪЭЪЧЃК_____________________________
ЁОНтЮіЁПЃЈ1ЃЉПМВщдЊЫижмЦкБэЕФНсЙЙКЭдзгКЫЭтЕчзгЕФХХВМЙцТЩЁЃИљОнЙЙдьдРэПЩжЊ4sЙьЕРЩЯжЛга1ИіЕчзгЕФдЊЫиЪЧKЁЂCrКЭ CuЁЃ
ЃЈ2ЃЉГ§dsЧјЭтЃЌЧјЕФУћГЦРДздгкЙЙдьдРэзюКѓЬюШыЕчзгЕФФмМЖЕФЗћКХЃЌМДsЧјАќРЈЕкIAКЭЂђAЃЌЙВ2СаЁЃpЧјАќРЈЕкЂѓAЕНЕк ЂїAвдМА0зхЃЌЙВ6СаЁЃDЧјАќРЈЕк3СаЕНЕк10СаЃЌЙВ8СаЁЃdsЧјАќРЈЕк11КЭ12СаЃЌЙВ2СаЁЃЗЧН№ЪєаддНЧПЃЌЕчИКаддНДѓЃЌЕквЛЕчРыФмвВдНДѓЃЌЗЧН№ЪєадЪЧClЃОSЃОPЃЌЫљвдЕчИКадЪЧClЃОSЃОPЁЃгЩгкPдзгЕФ3pЙьЕРЪєгкАыГфТњЃЌЪєгкЕквЛЕчРыФмЪЧClЃОPЃОSЁЃ
ЃЈ3ЃЉИљОнЙЙдьдРэПЩвдаДГіУЬдЊЫиЕФЕчзгХХВМЃЌМД1s22s22p63s23p63d54s2ЃЌFe2+ЕФЕчзгХХВМЭМЮЊ1s22s22p63s23p63d6ЁЃгЩгкMn2+ЕФ3dЙьЕРЪєгкАыГфТњЃЌБШНЯЮШЖЈЃЌЫљвддйЪЇШЅ1ИіЕчзгЫљашвЊЕФФмСПОЭИпЁЃЖјFe2+ЕФ3dЙьЕРЩЯга6ИіЕчзгЃЌFe3+ЕФ3dЙьЕРЩЯга5ИіЕчзгЃЌЪєгкВЛГфТњБШНЯЮШЖЈЃЌвђДЫ3dФмМЖгЩВЛЮШЖЈЕФ3d6ЕНЮШЖЈЕФ3d5АыГфТњзДЬЌЃЌашвЊЕФФмСПЯрЖдвЊЩйЁЃ
ЃЈ13ЗжЃЉЯТБэЮЊдЊЫижмЦкБэжаЧАЫФжмЦкЕФВПЗждЊЫиЃЈДгзѓЕНгвАДдзгађЪ§ЕндіХХСаЃЌВПЗжЩцМАЕНЕФдЊЫиЮДИјГідЊЫиЗћКХЃЉЃЌИљОнвЊЧѓЛиД№ЯТСаИїаЁЬтЃК
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ЁЁ | ЁЁ |
|
|
|
|
|
|
|
|
|
| ЁЁ |
|
|
|
| ЁЁ |
|
|
|
|
|
|
|
|
|
| |||||||||
|
|
| ЁЁ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ЃЈ1ЃЉдквдЩЯБэИёжаЫљгадЊЫиРяЛљЬЌдзгЕФЕчзгХХВМжа4sЙьЕРЩЯжЛга1ИіЕчзгЕФдЊЫига ЃЈЬюдЊЫиУћГЦЃЉЁЃ
ЃЈ2ЃЉИљОндЊЫидзгЕФЭтЮЇЕчзгХХВМЕФЬиеїЃЌПЩНЋдЊЫижмЦкБэЧАЫФжмЦкдЊЫиЗжГЩ4ИіЧјгђЃЌЗжБ№ЮЊsЧјЁЂpЧјЁЂdЧјЁЂdsЧјЃЌЃЌдђЪєгкsЧјЕФдЊЫига жжЃЌЪєгкdЧјЕФдЊЫига жжЁЃЕкЖўжмЦкдЊЫижаГ§NeЭтЕчИКадгЩИпЕНЕЭЕФШ§жждЊЫивРДЮЪЧ ,ЕчРыФмгЩИпЕНЕЭЕФШ§жждЊЫивРДЮЪЧ ЁЃ
ЃЈ3ЃЉMnЁЂFeОљЮЊЕкЫФжмЦкЙ§ЖЩдЊЫиЃЌСНдЊЫиЕФВПЗжЕчРыФмЪ§ОнСагкЯТБэЃК
| дЊЫи | Mn | Fe | |
| ЕчРыФм ЃЈ kJЁЄmolЃ1ЃЉ | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 |
ЛиД№ЯТСаЮЪЬтЃК
MnдЊЫиЕФЕчзгХХВМЪНЮЊ____________________________________ЃЌ
Fe2+ЕФЕчзгХХВМЭМЮЊ__________________________
БШНЯСНдЊЫиЕФI2ЁЂI3ПЩжЊЃЌЦјЬЌMn2+дйЪЇШЅвЛИіЕчзгБШЦјЬЌFe2+дйЪЇШЅвЛИі ЕчзгФбЁЃЖдДЫЃЌФуЕФНтЪЭЪЧЃК_____________________________
ЁОНтЮіЁПЃЈ1ЃЉПМВщдЊЫижмЦкБэЕФНсЙЙКЭдзгКЫЭтЕчзгЕФХХВМЙцТЩЁЃИљОнЙЙдьдРэПЩжЊ4sЙьЕРЩЯжЛга1ИіЕчзгЕФдЊЫиЪЧKЁЂCrКЭ CuЁЃ
ЃЈ2ЃЉГ§dsЧјЭтЃЌЧјЕФУћГЦРДздгкЙЙдьдРэзюКѓЬюШыЕчзгЕФФмМЖЕФЗћКХЃЌМДsЧјАќРЈЕкIAКЭЂђAЃЌЙВ2СаЁЃpЧјАќРЈЕкЂѓAЕНЕк ЂїAвдМА0зхЃЌЙВ6СаЁЃDЧјАќРЈЕк3СаЕНЕк10СаЃЌЙВ8СаЁЃdsЧјАќРЈЕк11КЭ12СаЃЌЙВ2СаЁЃЗЧН№ЪєаддНЧПЃЌЕчИКаддНДѓЃЌЕквЛЕчРыФмвВдНДѓЃЌЗЧН№ЪєадЪЧClЃОSЃОPЃЌЫљвдЕчИКадЪЧClЃОSЃОPЁЃгЩгкPдзгЕФ3pЙьЕРЪєгкАыГфТњЃЌЪєгкЕквЛЕчРыФмЪЧClЃОPЃОSЁЃ
ЃЈ3ЃЉИљОнЙЙдьдРэПЩвдаДГіУЬдЊЫиЕФЕчзгХХВМЃЌМД1s22s22p63s23p63d54s2ЃЌFe2+ЕФЕчзгХХВМЭМЮЊ1s22s22p63s23p63d6ЁЃгЩгкMn2+ЕФ3dЙьЕРЪєгкАыГфТњЃЌБШНЯЮШЖЈЃЌЫљвддйЪЇШЅ1ИіЕчзгЫљашвЊЕФФмСПОЭИпЁЃЖјFe2+ЕФ3dЙьЕРЩЯга6ИіЕчзгЃЌFe3+ЕФ3dЙьЕРЩЯга5ИіЕчзгЃЌЪєгкВЛГфТњБШНЯЮШЖЈЃЌвђДЫ3dФмМЖгЩВЛЮШЖЈЕФ3d6ЕНЮШЖЈЕФ3d5АыГфТњзДЬЌЃЌашвЊЕФФмСПЯрЖдвЊЩйЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com