
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
¹¤̉µÉÏͨ³£ÔÚºăÈƯĂܱƠÈƯÆ÷ÖĐ²ÉÓĂCO(g)ºÍH2 (g)·´Ó¦´ß»¯ºÏ³É¼×´¼CH3OH(g)£º
£¨1£©̉ÑÖª£º¢Ù 2CO(g) + O2 (g) = 2CO2 (g) ¦¤H =" -566.0" kJ¡¤mol-1
¢Ú 2H2(g) + O2 (g) ="2" H2O (g) ¦¤H =" -398.0" kJ¡¤mol-1
¢Û2CH3OH(g) +3O2 (g) =2CO2 (g) +4 H2O(g) ¦¤H =" -1104.0" kJ¡¤mol-1
ỘCO(g)ÓëH2(g)ºÏ³ÉCH3OH(g)µÄÈÈ»¯Ñ§·½³̀ʽÊÇ_______________¡£
£¨2£©¾ƯÑĐ¾¿£¬·´Ó¦¹ư³̀ÖĐÆđ´ß»¯×÷ÓõÄΪCuO£¬·´Ó¦̀åϵÖĐº¬ÉÙÁ¿CO2ÓĐÀûÓÚά³Ö´ß»¯¼ÁCuOµÄÁ¿²»±ä£¬Ộ̉ÊÇ£º_______________________________ (ÓĂ»¯Ñ§·½³̀ʽ±íʾ)¡£
£¨3£©ÅĐ¶Ï·´Ó¦´ïµ½Æ½ºâ×´̀¬µÄ̉À¾ƯÊÇ£῭î×ÖĸĐ̣ºÅ£¬ÏÂͬ£©__________¡£
A. »́ºÏÆø̀åµÄĂܶȲ»±ä
B. »́ºÏÆø̀åµÄƽ¾ùÏà¶Ô·Ö×ÓÖÊÁ¿²»±ä
C. CH3OH(g)¡¢CO(g)¡¢H2(g)µÄŨ¶È¶¼²»ÔÙ·¢Éú±ä»¯
D.Éú³ÉCH3OH(g)µÄËÙÂÊÓëÏûºÄCO(g)µÄËÙÂÊÏàµÈ
£¨4£©Ï±íËùÁĐÊư¾ƯÊÇ·´Ó¦ÔÚ²»Í¬Î¶ÈϵĻ¯Ñ§Æ½ºâ³£Êư£¨K£©¡£
| ÎÂ¶È | 250¡æ | 300¡æ | 350¡æ |
| K | 2.041 | 0.250 | 0.012 |
| ÈƯÆ÷ | ¼× | ̉̉ | ±û | |
| ·´Ó¦ÎïͶÈëÁ¿ | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| ƽºâÊư¾Ư | CH3OHµÄŨ¶È£¨mol/L£© | c 1 | c 2 | c 3 |
| ·´Ó¦µÄÄÜÁ¿±ä»¯µÄ¾ø¶ÔÖµ(kJ) | a | b | c | |
| ̀åϵѹǿ£¨Pa£© | P1 | P2 | P3 | |
| ·´Ó¦Îïת»¯ÂÊ | ¦Á1 | ¦Á2 | ¦Á3 | |
£¨1£©ÔÚ̉»¶῭å»ưµÄĂܱƠÈƯÆ÷ÖĐ£¬½øĐĐÈçÏ»¯Ñ§·´Ó¦£¬CO2(g)+H2(g)![]() CO(g)+H2O(g)¡£Æ仯ѧƽºâ³£ÊưKÓëζÈtµÄ¹ØϵÈçÏ¡£Çë»Ø´đÏÂÁĐÎỀ⣺
CO(g)+H2O(g)¡£Æ仯ѧƽºâ³£ÊưKÓëζÈtµÄ¹ØϵÈçÏ¡£Çë»Ø´đÏÂÁĐÎỀ⣺
| t¡æ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
¢Ù¸Ă·´Ó¦µÄ»¯Ñ§Æ½ºâ³£ÊưµÄ±í´ïʽK = £¬ÓÉÉϱíÊư¾Ư¿ÉµĂ£¬¸Ă·´Ó¦Îª ·´Ó¦¡££῭î¡°ÎüÈÈ¡±»̣¡°·ÅÈÈ¡±£©
¢Ú800¡æ£¬¹̀¶¨ÈƯÆ÷µÄĂܱƠÈƯÆ÷ÖĐ£¬·ÅÈë»́ºÏÎÆäʼŨ¶ÈΪc(CO)=0.01 mol¡¤L£1¡¢c(H2O)=0.03mol¡¤L£1¡¢c(CO2)=0.01 mol¡¤L£1¡¢c(H2)=0.05 mol¡¤L£1£¬Ộ·´Ó¦¿ªÊ¼Ê±£¬H2OµÄÏûºÄËÙÂʱÈÉú³ÉËÙÂÊ (̀´ó£¢¡¢£¢Đ¡£¢»̣£¢²»ÄÜÈ·¶¨£¢)
¢Û830¡æ£¬ÔÚ1 LµÄ¹̀¶¨ÈƯÆ÷µÄĂܱƠÈƯÆ÷ÖĐ·ÅÈë2 mol CO2ºÍ1 mol H2£¬Æ½ºâºóCO2µÄת»¯ÂÊΪ ¡£
£¨2£©Ä¿Ç°¹¤̉µÉÏÓĐ̉»ÖÖ·½·¨ÊÇÓĂCO2À´Éú²úȼÁϼ״¼¡£Îª̀½¾¿·´Ó¦ÔÀí£¬ÏÖ½øĐĐÈçÏÂʵÑ飬ÔÚ̀å»ưΪ1LµÄĂܱƠÈƯÆ÷ÖĐ£¬³äÈë1mol CO2ºÍ3mol H2£¬ÔÚ500¡æÏ·¢Éú·´Ó¦£ºCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ¡÷H=£49.0kJ¡¤mol£1¡£²âµĂCO2(g)ºÍCH3OH(g)µÄŨ¶ÈËæʱ¼ä±ä»¯ÈçͼËùʾ£º
CH3OH(g)+H2O(g) ¡÷H=£49.0kJ¡¤mol£1¡£²âµĂCO2(g)ºÍCH3OH(g)µÄŨ¶ÈËæʱ¼ä±ä»¯ÈçͼËùʾ£º
¢ÙƽºâʱCH3OHµÄ̀å»ư·ÖÊưwΪ ¡£
¢ÚÏÖÔÚζȡ¢ÈƯ»ưÏàͬµÄ3¸öĂܱƠÈƯÆ÷ÖĐ£¬°´²»Í¬·½Ê½Í¶Èë·´Ó¦Î±£³ÖºăΡ¢ºăÈƯ£¬²âµĂ·´Ó¦´ïµ½Æ½ºâʱµÄÓĐ¹ØÊư¾ƯÈçÏ¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
| ÈƯÆ÷ | ʵÑé1 | ʵÑé2 | ʵÑé3 |
| ·´Ó¦ÎïͶÈëÁ¿£¨Ê¼̀¬£© | 1mol CO2¡¢3mol H2 | 1mol CH3OH¡¢1mol H2O | 2mol CH3OH¡¢2mol H2O |
| CH3OHµÄƽºâŨ¶È/mol¡¤L£1 | C1 | C2 | C3 |
| ·´Ó¦µÄÄÜÁ¿±ä»¯ | ·Å³ö x kJ | ÎüÊƠy kJ | ÎüÊƠz kJ |
| ̀åϵѹǿ/Pa | P1 | P2 | P3 |
| ·´Ó¦Îïת»¯ÂÊ | a1 | a2 | a3 |
A£®2 C1>C3 B£®x+y=49.0 C£®2P2<P3
D£®£¨a1+a3£©<1 E£®2P1>P3 F£®a1= a2
¢ÛÔÚ̉»¸ö×°ÓĐ¿É̉ƶ¯»îÈûµÄÈƯÆ÷ÖĐ½øĐĐÉÏÊö·´Ó¦£ºCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)¡£·´Ó¦´ïµ½Æ½ºâºó£¬²âµĂCH3OHµÄÎïÖʵÄÁ¿Îªa mol£¬±£³ÖÈƯÆ÷ÄÚµÄζȺÍѹǿ²»±ä£¬Ị̈ƽºầåϵÖĐͨÈëÉÙÁ¿µÄH2£¬Ôٴδﵽƽºâºó£¬²âµĂCH3OHµÄÎïÖʵÄÁ¿Îªb mol£¬Çë±È½Ïa¡¢bµÄ´óĐ¡ ¡£
CH3OH(g)+H2O(g)¡£·´Ó¦´ïµ½Æ½ºâºó£¬²âµĂCH3OHµÄÎïÖʵÄÁ¿Îªa mol£¬±£³ÖÈƯÆ÷ÄÚµÄζȺÍѹǿ²»±ä£¬Ị̈ƽºầåϵÖĐͨÈëÉÙÁ¿µÄH2£¬Ôٴδﵽƽºâºó£¬²âµĂCH3OHµÄÎïÖʵÄÁ¿Îªb mol£¬Çë±È½Ïa¡¢bµÄ´óĐ¡ ¡£

| ||
| ||
| ||
| ̀«Ñô¹â |
| ||
| ζÈ/¡æ | 0 | 100 | 200 | 300 | 400 |
| ƽºâ³£Êư | 667 | 13 | 1.9¡Á10-2 | 2.4¡Á10-4 | 1¡Á10-5 |
ÔÚ̉»ºăΡ¢ºăÈƯĂܱƠÈƯÆ÷ÖĐ³äÈë1mol CO2ºÍ3 mol H2£¬̉»¶῭ơ¼₫Ï·¢Éú·´Ó¦£º
CO2(g)+3H2(g) CH3OH (g)+H2O(g) ¡÷H=£49.0 kJ/mol
CH3OH (g)+H2O(g) ¡÷H=£49.0 kJ/mol
ijÖÖ·´Ó¦ÎïºÍÉú³ÉÎïµÄŨ¶ÈËæʱ¼ä±ä»¯ÈçͼËùʾ¡£»Ø´đÏÂÁĐÎỀ⣺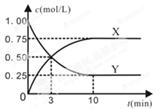
£¨1£©YµÄ»¯Ñ§Ê½ÊÇ ¡£
£¨2£©·´Ó¦½øĐе½3minʱ£¬ vƠư vÄæ(̀î¡°£¾¡±»̣¡°<¡±¡¢¡°=¡±)¡£·´Ó¦Ç°3min£¬H2µÄƽ¾ù·´Ó¦ËÙÂÊv£¨H2£©= mol¡¤L-1¡¤min-1¡£
£¨3£©²»ÄÜÅĐ¶Ï¸Ă·´Ó¦´ïµ½»¯Ñ§Æ½ºâ×´̀¬µÄ̉À¾ƯÊÇ ¡£
| A£®ÈƯÆ÷ÄÚ¸÷Æø̀åµÄ̀å»ư±È±£³Ö²»±ä | B£®»́ºÏÆø̀åĂܶȲ»±ä |
| C£®3vÄ棨CH3OH£© =vƠư£¨H2£© | D£®H2ת»¯ÂÊΪ75% |
 CO2(g) + 3H2(g)µÄƽºâ³£ÊưK= £¨¼ÆËă½á¹û±£Áô2Î»Đ¡Êư£©¡£
CO2(g) + 3H2(g)µÄƽºâ³£ÊưK= £¨¼ÆËă½á¹û±£Áô2Î»Đ¡Êư£©¡£ £¨2012?ăÉĐĐÇø¶₫Ä££©ÑĐ¾¿ºÍ¿ª·¢CO2ºÍCOµÄ´´ĐÂÀûÓĂÊÇ»·¾³±£»¤ºÍ×ÊÔ´ÀûÓõÄË«Ó®¿Î̀⣮CO¿ÉÓĂÓںϳɼ״¼£®ÔÚѹǿΪ0.1MPàơ¼₫Ï£¬ÔÚ̀å»ưΪb LµÄĂܱƠÈƯÆ÷ÖĐ³äÈëa mol COºÍ2a mol H2£¬ÔÚ´ß»¯¼Á×÷ÓĂϺϳɼ״¼£ºCO£¨g£©+2H2£¨g£©?CH3OH£¨g£©£¬Æ½ºâʱCOµÄת»¯ÂÊÓëζȡ¢Ñ¹Ç¿µÄ¹ØϵÈçͼ£º
£¨2012?ăÉĐĐÇø¶₫Ä££©ÑĐ¾¿ºÍ¿ª·¢CO2ºÍCOµÄ´´ĐÂÀûÓĂÊÇ»·¾³±£»¤ºÍ×ÊÔ´ÀûÓõÄË«Ó®¿Î̀⣮CO¿ÉÓĂÓںϳɼ״¼£®ÔÚѹǿΪ0.1MPàơ¼₫Ï£¬ÔÚ̀å»ưΪb LµÄĂܱƠÈƯÆ÷ÖĐ³äÈëa mol COºÍ2a mol H2£¬ÔÚ´ß»¯¼Á×÷ÓĂϺϳɼ״¼£ºCO£¨g£©+2H2£¨g£©?CH3OH£¨g£©£¬Æ½ºâʱCOµÄת»¯ÂÊÓëζȡ¢Ñ¹Ç¿µÄ¹ØϵÈçͼ£º¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com