
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
 Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®
Ģ¼ŗĶĢ¼µÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠµÄÓ¦ÓĆ·Ē³£¹ć·ŗ£¬ŌŚĢį³«½”æµÉś»īŅŃ³É³±Į÷µÄ½ńĢģ£¬”°µĶĢ¼Éś»ī”±²»ŌŁÖ»ŹĒŅ»ÖÖĄķĻė£¬øüŹĒŅ»ÖÖÖµµĆĘŚ“żµÄŠĀµÄÉś»ī·½Ź½£®| øßĪĀ |
| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
| øßĪĀ |
| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖłŠčŹ±¼ä/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
¾Ż±ØµĄ£¬ŌŚĪ÷²Ų¶³ĶĮµÄŅ»¶ØÉī¶ČĻĀ£¬·¢ĻÖĮĖ“¢Į澎“óµÄ”°æÉČ¼±ł”±£¬ĖüÖ÷ŅŖŹĒ¼×ĶéŗĶĖ®ŠĪ³ÉµÄĖ®ŗĻĪļ£ØCH4”¤nH2O£©”£
£Ø1£©ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬”°æÉČ¼±ł”±»į·¢Éś·Ö½ā·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø2£©¼×ĶéæÉÖĘ³ÉŗĻ³ÉĘų£ØCO”¢H2£©£¬ŌŁÖĘ³É¼×“¼£¬“śĢęČÕŅę¹©Ó¦½ōÕŵÄČ¼ÓĶ”£
¢ŁŌŚ101 KPaŹ±£¬1£®6 g CH4£Øg£©ÓėH2O£Øg£©·“Ӧɜ³ÉCO”¢H2£¬ĪüČČ20£®64 kJ”£Ōņ¼×ĶéÓėH2O£Øg£©·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
¢ŚCH4²»ĶźČ«Č¼ÉÕŅ²æÉÖʵĆŗĻ³ÉĘų£ŗCH4£Øg£©+ O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
”÷H=-35.4 kJ”¤mol-1”£Ōņ“ÓŌĮĻŃ”ŌńŗĶÄÜŌ“ĄūÓĆ½Ē¶Č£¬±Č½Ļ·½·Ø¢ŁŗĶ¢Ś£¬ŗĻ³É¼×“¼µÄŹŹŅĖ·½·ØĪŖ£ØĢīŠņŗÅ£©£»ŌŅņŹĒ ”£
¢ŪŌŚĪĀ¶ČĪŖT£¬Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1 mol CO”¢2 mol H2£¬·¢Éś·“Ó¦
CO£Øg£©+ 2H2£Øg£© CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
I£®H2µÄ×Ŗ»ÆĀŹĪŖ £»
II£®ŌŚĻąĶ¬Ģõ¼žĻĀ£¬ČōĘšŹ¼Ź±ĻņĆܱÕČŻĘ÷ÖŠ¼ÓČėa mol CH3 OH£Øg£©£¬·“Ó¦Ę½ŗāŗóĪüŹÕČČĮæQ2 kJ£¬ĒŅQ1+Q2=Q£¬Ōņa= mol”£
III£®ŅŃÖŖĘšŹ¼µ½Ę½ŗāŗóµÄCOÅضČÓėŹ±¼äµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£Ōņt1Ź±½«Ģå»ż±äĪŖ5Lŗó£¬Ę½ŗāĻņ ·“Ó¦·½ĻņŅĘ¶Æ£ØĢī”°Õż”±»ņ”°Äę”±£©£»

ŌŚÉĻĶ¼ÖŠ»³ö“ÓtlæŖŹ¼µ½ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬
COÅضČÓėŹ±¼äµÄ±ä»ÆĒ÷ŹĘĒśĻß”£
£Ø3£©½«CH4Éč¼Ę³ÉČ¼ĮĻµē³Ų£¬ĘäĄūÓĆĀŹøüøߣ¬×°ÖĆŹ¾ŅāČēÓŅĶ¼£ØA”¢BĪŖ¶ąæ׊ŌĢ¼°ō£©”£

³ÖŠųĶØČĖ¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéĢå»żVL”£
¢ŁO<V”Ü44£®8 LŹ±£¬µē³Ų×Ü·“Ó¦·½³ĢŹ½ĪŖ £»
¢Ś44£®8 L<V”Ü89£®6 LŹ±£¬øŗ¼«µē¼«·“Ó¦ĪŖ £»
¢ŪV=67£®2 LŹ±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ £»
¾Ż±ØµĄ£¬ŌŚĪ÷²Ų¶³ĶĮµÄŅ»¶ØÉī¶ČĻĀ£¬·¢ĻÖĮĖ“¢Į澎“óµÄ”°æÉČ¼±ł”±£¬ĖüÖ÷ŅŖŹĒ¼×ĶéŗĶĖ®ŠĪ³ÉµÄĖ®ŗĻĪļ£ØCH4”¤nH2O£©”£
£Ø1£©ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬”°æÉČ¼±ł”±»į·¢Éś·Ö½ā·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø2£©¼×ĶéæÉÖĘ³ÉŗĻ³ÉĘų£ØCO”¢H2£©£¬ŌŁÖĘ³É¼×“¼£¬“śĢęČÕŅę¹©Ó¦½ōÕŵÄČ¼ÓĶ”£
¢ŁŌŚ101 KPaŹ±£¬1£®6 g CH4£Øg£©ÓėH2O£Øg£©·“Ӧɜ³ÉCO”¢H2£¬ĪüČČ20£®64 kJ”£Ōņ¼×ĶéÓėH2O£Øg£©·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
¢ŚCH4²»ĶźČ«Č¼ÉÕŅ²æÉÖʵĆŗĻ³ÉĘų£ŗCH4£Øg£©+![]() O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
”÷H=-35.4 kJ”¤mol-1”£Ōņ“ÓŌĮĻŃ”ŌńŗĶÄÜŌ“ĄūÓĆ½Ē¶Č£¬±Č½Ļ·½·Ø¢ŁŗĶ¢Ś£¬ŗĻ³É¼×“¼µÄŹŹŅĖ·½·ØĪŖ£ØĢīŠņŗÅ£©£»ŌŅņŹĒ ”£
¢ŪŌŚĪĀ¶ČĪŖT£¬Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1 mol CO”¢2 mol H2£¬·¢Éś·“Ó¦
CO£Øg£©+ 2H2£Øg£©![]() CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
I£®H2µÄ×Ŗ»ÆĀŹĪŖ £»
II£®ŌŚĻąĶ¬Ģõ¼žĻĀ£¬ČōĘšŹ¼Ź±ĻņĆܱÕČŻĘ÷ÖŠ¼ÓČėa mol CH3 OH£Øg£©£¬·“Ó¦Ę½ŗāŗóĪüŹÕČČĮæQ2 kJ£¬ĒŅQ1+Q2=Q£¬Ōņa= mol”£
III£®ŅŃÖŖĘšŹ¼µ½Ę½ŗāŗóµÄCOÅضČÓėŹ±¼äµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£Ōņt1Ź±½«Ģå»ż±äĪŖ5Lŗó£¬Ę½ŗāĻņ ·“Ó¦·½ĻņŅĘ¶Æ£ØĢī”°Õż”±»ņ”°Äę”±£©£»
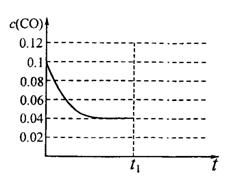
ŌŚÉĻĶ¼ÖŠ»³ö“ÓtlæŖŹ¼µ½ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬
COÅضČÓėŹ±¼äµÄ±ä»ÆĒ÷ŹĘĒśĻß”£
£Ø3£©½«CH4Éč¼Ę³ÉČ¼ĮĻµē³Ų£¬ĘäĄūÓĆĀŹøüøߣ¬×°ÖĆŹ¾ŅāČēÓŅĶ¼£ØA”¢BĪŖ¶ąæ׊ŌĢ¼°ō£©”£
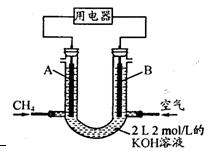
³ÖŠųĶØČĖ¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéĢå»żVL”£
¢ŁO<V”Ü44£®8 LŹ±£¬µē³Ų×Ü·“Ó¦·½³ĢŹ½ĪŖ £»
¢Ś44£®8 L<V”Ü89£®6 LŹ±£¬øŗ¼«µē¼«·“Ó¦ĪŖ £»
¢ŪV=67£®2 LŹ±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ £»
¾Ż±ØµĄ£¬ŌŚĪ÷²Ų¶³ĶĮµÄŅ»¶ØÉī¶ČĻĀ£¬·¢ĻÖĮĖ“¢Į澎“óµÄ”°æÉČ¼±ł”±£¬ĖüÖ÷ŅŖŹĒ¼×ĶéŗĶĖ®ŠĪ³ÉµÄĖ®ŗĻĪļ£ØCH4”¤nH2O£©”£
£Ø1£©ŌŚ³£ĪĀ³£Ń¹ĻĀ£¬”°æÉČ¼±ł”±»į·¢Éś·Ö½ā·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø2£©¼×ĶéæÉÖĘ³ÉŗĻ³ÉĘų£ØCO”¢H2£©£¬ŌŁÖĘ³É¼×“¼£¬“śĢęČÕŅę¹©Ó¦½ōÕŵÄČ¼ÓĶ”£
¢ŁŌŚ101 KPaŹ±£¬1£®6 g CH4£Øg£©ÓėH2O£Øg£©·“Ӧɜ³ÉCO”¢H2£¬ĪüČČ20£®64 kJ”£Ōņ¼×ĶéÓėH2O£Øg£©·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
¢ŚCH4²»ĶźČ«Č¼ÉÕŅ²æÉÖʵĆŗĻ³ÉĘų£ŗCH4£Øg£©+![]() O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
O2£Øg£©===CO£Øg£©+2H2£Øg£©£»
”÷H=-35.4 kJ”¤mol-1”£Ōņ“ÓŌĮĻŃ”ŌńŗĶÄÜŌ“ĄūÓĆ½Ē¶Č£¬±Č½Ļ·½·Ø¢ŁŗĶ¢Ś£¬ŗĻ³É¼×“¼µÄŹŹŅĖ·½·ØĪŖ£ØĢīŠņŗÅ£©£»ŌŅņŹĒ ”£
¢ŪŌŚĪĀ¶ČĪŖT£¬Ģå»żĪŖ10LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1 mol CO”¢2 mol H2£¬·¢Éś·“Ó¦
CO£Øg£©+ 2H2£Øg£©![]() CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
CH3OH£Øg£©£»”÷H=-Q kJ”¤mol-1£ØQ>O£©£¬“ļµ½Ę½ŗāŗóµÄŃ¹ĒæŹĒæŖŹ¼Ź±Ń¹ĒæµÄ0£®6±¶£¬·Å³öČČĮæQ1kJ”£
I£®H2µÄ×Ŗ»ÆĀŹĪŖ £»
II£®ŌŚĻąĶ¬Ģõ¼žĻĀ£¬ČōĘšŹ¼Ź±ĻņĆܱÕČŻĘ÷ÖŠ¼ÓČėa mol CH3 OH£Øg£©£¬·“Ó¦Ę½ŗāŗóĪüŹÕČČĮæQ2 kJ£¬ĒŅQ1+Q2=Q£¬Ōņa= mol”£
III£®ŅŃÖŖĘšŹ¼µ½Ę½ŗāŗóµÄCOÅضČÓėŹ±¼äµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£Ōņt1Ź±½«Ģå»ż±äĪŖ5Lŗó£¬Ę½ŗāĻņ ·“Ó¦·½ĻņŅĘ¶Æ£ØĢī”°Õż”±»ņ”°Äę”±£©£»
ŌŚÉĻĶ¼ÖŠ»³ö“ÓtlæŖŹ¼µ½ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬
COÅضČÓėŹ±¼äµÄ±ä»ÆĒ÷ŹĘĒśĻß”£
£Ø3£©½«CH4Éč¼Ę³ÉČ¼ĮĻµē³Ų£¬ĘäĄūÓĆĀŹøüøߣ¬×°ÖĆŹ¾ŅāČēÓŅĶ¼£ØA”¢BĪŖ¶ąæ׊ŌĢ¼°ō£©”£
³ÖŠųĶØČĖ¼×Ķ飬ŌŚ±ź×¼×“æöĻĀ£¬Ļūŗļ×ĶéĢå»żVL”£
¢ŁO<V”Ü44£®8 LŹ±£¬µē³Ų×Ü·“Ó¦·½³ĢŹ½ĪŖ £»
¢Ś44£®8 L<V”Ü89£®6 LŹ±£¬øŗ¼«µē¼«·“Ó¦ĪŖ £»
¢ŪV=67£®2 LŹ±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ £»
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com