
题目列表(包括答案和解析)
①Na2S ②Na2SO3 ③Na2S2O3 ④NaHSO4
将混合物溶于适量水中,各物质恰好完全反应,生成沉淀n mol,产生一种气体V L(标准状况,假设气体被全部收集),该气体不能使湿润的品红试纸褪色,过滤,将滤液蒸干,得一纯净物。
(1)原混合物至少由________________种物质组成。
(2)计算(1)中各组分可能的物质的量是______________________________________。
已知某白色混合物粉末由下表中的部分离子组成:
|
完成以胆矾为原料制取氧化铜固体实验,并用氧化铜和氯酸钾的混合物制氧气,测量生成氧气的体积。试回答:
(1)向CuSO4溶液中滴加NaOH溶液至不再产生沉淀,反应的离子方程式为
。
(2)将溶液和沉淀放入蒸发皿中加热,直至沉淀全部变黑,冷却后过滤。过滤时由于操作失误,造成滤液浑浊,但滤纸尚未破损。造成滤液浑浊的原因可能是 。
(3)某同学设计了如图所示的装置,用于测量氯酸钾催化作用下分解生成氧气的体积。
①用氧化桶和氯酸钾的混合物制氧气的化学方程式为 。
②检查装置气密性后,将CuO和KClO3的混合物平铺在试管底部,将量筒装满水倒扣在水槽中。后续操作的正确顺序是(用下列操作中的部分或全部步骤代号回答)
。a.用酒精灯给试管中的药品加热
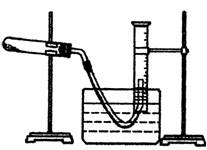 b.待有连续气泡产生时,将导气管出气端管口伸入盛满水的量筒内
b.待有连续气泡产生时,将导气管出气端管口伸入盛满水的量筒内
c.将导气管出气端管口伸入盛满水的量筒内
d.使量筒内液面与水槽中液面持平,然后读数
e.停止加热,使试管冷却至室温(如图,导管出口高于液面)
③按正确操作及顺序完成实验后,测得的气体体积比理论值低,可能的原因是
(4)请设计两种不加热制备氧气的实验方案(用化学方程式表示,反应物不得重复使用)。
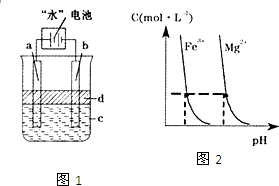 “水”电池是利用淡水与海水之间含盐量的差别进行发电的一种新型电池.(1)研究表明,电池用二氧化锰纳米棒为正极材料可提高发电效率,这是利用纳米材料具有
“水”电池是利用淡水与海水之间含盐量的差别进行发电的一种新型电池.(1)研究表明,电池用二氧化锰纳米棒为正极材料可提高发电效率,这是利用纳米材料具有
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com