
题目列表(包括答案和解析)
(1)Y的元素符号是___________________。
(2)XW的电子式是________________。
(3)XW与YX3反应生成一种盐,该盐水溶液的pH_______________7(填“大于”“小于”或“等于”),其原因是(用离子方程式表示)___________________。
(4)Z元素氢化物的沸点比H2O_______________(填“低”或“高”)。Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式________________。
(5)已知X单质和Y单质反应生成YX3是可逆反应,ΔH<0。将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的是_________________。
a.达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,YX3的体积分数增大
(1)Y的元素符号是__________。
(2)XW的电子式是__________。
(3)XW与YX3反应生成一种盐,该盐水溶液的pH__________7(填“大于”“小于”或“等于”),其原因是(用离子方程式表示)_________________________。
(4)Z元素氢化物的沸点比H2O(填“低”或“高”)。Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式________________________________。
(5)已知X单质和Y单质反应生成YX3是可逆反应,ΔH<0。将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的是______。
a.达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,YX3的体积分数增大
X、Y、Z、W均为10电子的分子或离子。X有5个原子核。通常状况下,W为无色液体。它们之间转化关系如图所示,请回答:
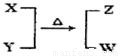
(1)工业上每制取1molZ要放出46.2 kJ的热量,写出该反应的热化学方程式: 。
(2)工业制取Z的化学平衡常数K与T的关系如下表:
|
T/K |
298 |
398 |
498 |
…… |
|
K/(mol·L—1)—2 |
4.1×106 |
K1 |
K2 |
…… |
请完成下列问题:
①试比较K1、K2的大小,K1 K2(填写“>”“=”或“<”)
②恒温固定体积的容器中,下列各项能作为判断该反应达到化学平衡状态的依据的是 (填序号字母)。
A.容器内各物质的浓度之比为化学计量数比
B.混合气体密度保持不变
C.容器内压强保持不变
D.混合气体相对分子质量保持不变
(3)某化学小组同学模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。
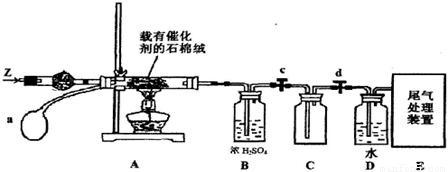
①A中发生反应的化学方程式是 。
②B中浓H2SO4的作用是 。
(4)写出D装置中反应的化学方程式 。
(5)a中通入空气的作用 。
X、Y、Z、W均为10电子的分子或离子。X有5个原子核。通常状况下,W为无色液体。它们之间转化关系如图所示,请回答: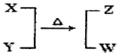
(1)工业上每制取1molZ要放出46.2 kJ的热量,写出该反应的热化学方程式: 。
(2)工业制取Z的化学平衡常数K与T的关系如下表:
| T/K | 298 | 398 | 498 | …… |
| K/(mol·L—1)—2 | 4.1×106 | K1 | K2 | …… |

X、Y、Z、W为原子序数依次增大的四种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水。
(1)Y的元素符号是____________。
(2)XW的电子式是____________。
(3)XW与YX3反应生成一种盐,该盐水溶液的pH________7(填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)_________________________。
(4)Z元素氢化物的沸点比H2O_______(填“低”或“高”)。Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式_____________________。
(5)已知X单质和Y单质反应生成YX3是可逆反应,△H<0。将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法正确的是_______。
a. 达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b. 反应过程中,Y单质的体积分数始终为50%
c. 达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d. 达到化学平衡的过程中气体平均相对分子质量减小
e. 达到化学平衡后,升高温度,YX3的体积分数增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com