
题目列表(包括答案和解析)
(1)写出工业电解食盐水制取H2和Cl2的化学方程式:_______________________。
(2)工业上要得到纯盐酸并保障工人工作安全,如何合成氯化氢是关键的一步。则下列合成氯化氢气体的方法能达到生产目的的是________。
A.点燃H2和Cl2的混合物,二者体积(标准状况下测定)比为1∶1最合适。
B.点燃H2和Cl2的混合物,二者体积(同温同压下测定)比不应为1∶1。
C.纯净的H2在过量的Cl2中安静地燃烧。
D.纯净的Cl2在过量的H2中安静地燃烧。
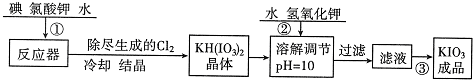
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
| 1270 |
| 3w |
| 423.33 |
| w |
| 1270 |
| 3w |
| 423.33 |
| w |
| 实验步骤 | 实验操作 | 实验现象 |
| 步骤1 | 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 步骤2 | 滴入5滴淀粉溶液和1mL0.1 mol?L-1KI溶液,振荡. | 溶液无变化 |
| 步骤3 | 然后再滴入1滴1 mol?L-1的H2SO4,振荡. | 溶液变蓝色 |
| 2n-7 |
| 2n+1 |
| 2n-7 |
| 2n+1 |
(16分)(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上 (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上(填“有”或“没有”) 气泡产生。

(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是 ,
有关的电极反应式:锌片 ;铜片 。
图丙所示原电池中,电子流向为 。
(3)图乙、图丙是一个将 能转化为 能的装置,人们把它叫做原电池。
(16分)(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上 (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上(填“有”或“没有”) 气泡产生。
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是 ,
有关的电极反应式:锌片 ;铜片 。
图丙所示原电池中,电子流向为 。
(3)图乙、图丙是一个将 能转化为 能的装置,人们把它叫做原电池。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com