
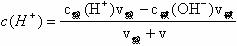
③碱过量时:
2. 强酸和强碱混合
①恰好完全反应:pH=7
②酸过量时:
(2)强碱混合: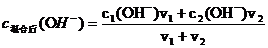
然后,再根据c(H+)= Kw/ c(OH-),求算c(H+)。
3.酸酸混合或碱碱混合溶液pH值计算
(1)强酸混合:
2.溶液的稀释:
规律:酸:pH= a,加水稀释10n倍,强酸:pH= a + n,弱酸:pH < a + n
无限稀释,pH接近7,但不会小于7
碱:pH= b,加水稀释10n倍,强碱:pH= b-n,弱碱:pH > b-n
无限稀释,pH接近7,但不会小于7。
1.单一溶液的pH值计算:pH=-lgc(H+)
3.释稀溶液与PH的关系:
①对于强酸溶液,每稀释10倍,PH增大一个单位,无论如何冲稀也不会等于或大于7;对于强碱溶液,每冲稀10倍,PH减小一个单位,无论如何冲稀也不会等于或小于7。
②对于PH相同的强酸和弱酸(强碱或弱碱)溶液冲稀相同的倍数,强酸或强碱溶液的PH变化大,这是因为强酸或强碱已完全电离,而弱酸或弱碱还能继续电离出H+、OH-。
要点二:PH值的计算
2.酸碱性与PH值的关系:
用PH值的大小来判断溶液的酸碱性,须注意温度:
常温下,PH=7的溶液为中性;在
1.溶液酸碱性的判断依据:
c(H+) >c(OH-),溶液呈酸性;c(H+)=c(OH-),溶液呈中性;c(H+)<c(OH-),溶液呈碱性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com