
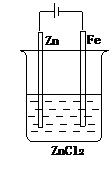
形成条件
①活动性不同的两电极(连接)
②电解质溶液(电极插入其中并与电极自发反应)
③形成闭合回路
①两电极接直流电源
②两电极插入电解质溶液
③形成闭合回路
①镀层金属接电源正极,待镀金属接电源负极
②电镀液必须含有镀层金属的离子
电极名称
负极:较活动金属
正极:较不活动金属(或能导电的非金属)
阳极:与电源正极相连的极
阴极:与电源负极相连的极
名称同电解,但有限制条件
阳极:必须是镀层金属
阴极:镀件
电极反应
负极:氧化反应、金属失电子
正极:还原反应,溶液中的阳离子得电子
阳极:氧化反应,溶液中的阴离子失电子,或电极金属失电子
阴极:还原反应,溶液中的阳离子得电子
阳极:金属电极失电子
阴极:电镀液中阳离子得电子
电子流向
4.电冶金:Mg、Al的制取,如,电解熔融NaCl制金属Na:2NaCl(熔融) =2Na + Cl2↑
六、三池的比较
原电池
电解池
电镀池
定义
将化学能转变成电解的装置
将电能转变成化学能的装置
应用电解原理在某些金属表面镀上一层其它金属的装置
装置举例
3.电解精炼铜:以粗铜为阳极,精铜为阴极,含铜离子的溶液作电解质溶液。电解时发生如下反应:阳极(粗铜):Cu -2e- = Cu2+;阴极(纯铜):Cu2+ + 2e- = Cu。
2.电镀:待镀金属制品作阴极,镀层金属作阳极,含有镀层金属离子的溶液作电镀液,阳极反应:M ? ne- =Mn+(进入溶液),阴极反应Mn+ + ne- =M(在镀件上沉积金属)
1.氯碱工业(电解饱和食盐水):2NaCl + 2H2O == 2NaOH + H2↑ + Cl2↑
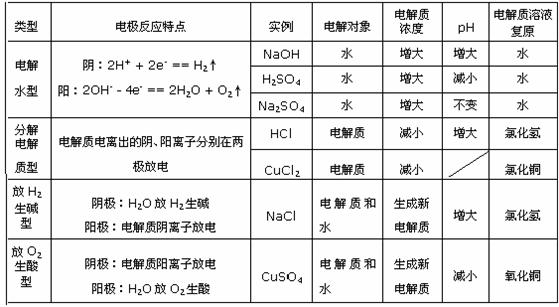 5.原电池、电解池、电镀池的判断
5.原电池、电解池、电镀池的判断
(1)若无外接电源,可能是原电池,然后根据原电池的形成条件判断
(2)若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池,当阳极金属与电解质溶液中的金属离子相同,则为电镀池
(3)若无明显外接电源的串联电路,则应利用题中信息找出能发生自发氧化还原反应的装置为原电池。
(4)可充电电池的判断:放电时相当于原电池,负极发生氧化反应,正极发生还原反应;充电时相当于电解池,放电时的正极变为电解池的阳极,与外电源正极相连,负极变为阴极,与外电源负极相连。
五、电解原理的应用
4.酸、碱、盐溶液电解规律(惰性电极)
2.书写燃料电池电极反应式时应注意如下几点:
(1)电池的负极一定是可燃性气体,失电子,发生氧化反应;电池的正极一定是助燃气体,得电子,发生还原反应。
(2)写电极反应时,一定要注意电解质是什么,其中的离子要和电极反应中出现的离子相对应,碱性电解质时,电极反应式不能出现H+;酸性电解质时,电极反应式不能出现OH-。
(3)可由正负两极的电极反应式相叠加得到总电极反应式,但要注意是在得失电子守恒前提下;电极反应要注意是燃料反应和燃料产物与电解质溶液反应的相叠加的反应式。
⒈ 电极的判断与电极上的反应。
(1)阳极:与电源正极相连的电极,是发生氧化反应;若惰性材料(石墨、Pt、Au )作阳极,失电子的是溶液中的阴离子;若为活性金属电极(Pt、Au除外),失电子的是电极本身,表现为金属溶解。
(2)阴极:是与电源负极相连的电极,电极本身不参与反应;溶液中的阳离子在阴极上得电子,发生还原反应。
⒉ 电流或电子的流向:电解池中电子由电源负极流向阴极,被向阴极移动的某种阳离子获得,而向阳极移动的某种阴离子或阳极本身在阳极上失电子,电子流向电源正极。
⒊ 离子的放电顺序:主要取决于离子本身的性质,也与溶液浓度、温度、电极材料等有关。
(1)阴极(得电子能力):Ag+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+> K+,但应注意,电镀时通过控制条件(如离子浓度等),Fe2+和Zn2+可先于H+放电。
(2)阳极(失电子能力):若阳极材料为活性电极(Pt、Au 除外),则电极本身失去电子,而溶液中的阴离子不参与电极反应;若阳极材料为惰性电极,则有S2->I->Br->Cl->OH->含氧酸根离子及F-等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com