
32.[化学-有机化学基础](13分)
已知:
为合成某种液晶材料的中间体M,有人提出如下不同的合成途径
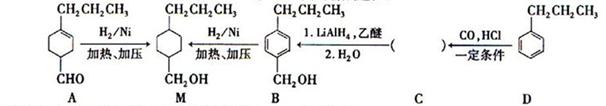
(1)常温下,下列物质能与A发生反应的有_______(填序号)
a.苯 b.Br2/CCl4 c.乙酸乙酯 d.KMnO4/H+溶液
(2)M中官能团的名称是____,由C→B反应类型为________。
(3)由A催化加氢生成M的过程中,可能有中间生成物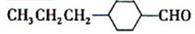 和______(写结构简式)生成
和______(写结构简式)生成
(4)检验B中是否含有C可选用的试剂是_____(任写一种名称)。
(5)物质B也可由C10H13Cl与NaOH水溶液共热生成,C10H13Cl的结构简式为______。
(6)C的一种同分异构体E具有如下特点:
a.分子中含—OCH3CH3 b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式__________________。
31.[化学—物质结构与性质](13分)
(1)依据第2周期元素第一电离能的变化规律,参照右图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:
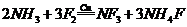
①上述化学方程式中的5种物质所属的晶体类型有_________(填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
②基态铜原子的核外电子排布式为________。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
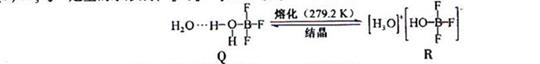
①晶体Q中各种微粒间的作用力不涉及___________(填序号)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力
②R中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。
(4)已知苯酚(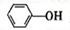 )具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子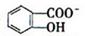 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
30.[物理选修3-5](本题共有两小题,每小题6分,共12分。每小题只有一个符合题意)
(1)在卢瑟福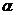 粒子散射实验中,金箔中的原子核可以看作静止不动,下列各图画出的是其中两个
粒子散射实验中,金箔中的原子核可以看作静止不动,下列各图画出的是其中两个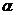 粒子经历金箔散射过程的径迹,其中正确的是____。(填选图下方的字母)
粒子经历金箔散射过程的径迹,其中正确的是____。(填选图下方的字母)
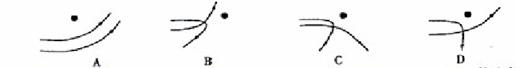
(2)将静置在地面上,质量为M(含燃料)的火箭模型点火升空,在及短时间内以相对地面的速度v0竖直向下喷出质量为m的炽热气体。忽略喷气过程重力和空气阻力的影响,则喷气结束时火箭模型获得的速度大小是 。(填选项前的事母)
A.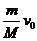 B.
B. 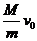 C.
C. 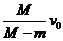 D.
D. 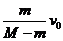
29.[物理-选修3-3](本题共有两小题,每小题6分,共12分。每小题只有一个选项符合题意)
(1)下列四﹣中,能正确反映分子间作用力f和分子势能EP随分子间距离r变化关系的图线是 。(填选图下方的字母)
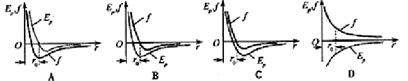
(2)某自行车轮胎的容积为V.里面已有压强为P0的空气,现在要使轮胎内的气压增大到P,设充气过程为等温过程,空气可看作理想气体,轮胎容积保持不变,则还要向轮胎充入温度相同,压强也是P0,体积为
的空气。(填选项前的字母)
A.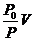 B.
B. 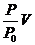 C.
C. 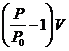 D.
D. 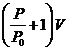
28.(12分)
甘蓝型油菜花色性状由三对等位基因控制,三对等位基因分别位于三对同源染色体上。花色表现型与基因型之间的对应关系如表。
|
表现型 |
白花 |
乳白花 |
黄花 |
金黄花 |
|
基因型 |
AA____ |
Aa____ |
aaB____ a___ D__ |
aabbdd |
请回答:
(1)白花(AABBDD)×黄花(aaBBDD),F1基因型是____,F1测交后代的花色表现型及其比例是____。
(2)黄花(aaBBDD)×金黄花,F1自交,F2中黄花基因型有____种,其中纯合个体占黄花的比例是____。
(3)甘蓝型油菜花色有观赏价值,欲同时获得四种花色表现型的子一代,可选择基因型为____的个体自交,理论上子一代比例最高的花色表现型是____。
27.(16分)
为探究铅中毒对大鼠学习记忆的影响,将大鼠分为四组,其中一组饮水,其余三组饮醋酸铅溶液,60天后进行检测。
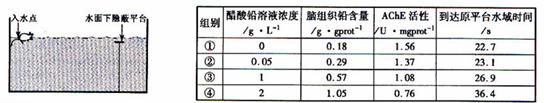
检测a:用下图水迷宫(池水黑色,大鼠无法看到平台)进行实验,大鼠从入水点入水,训练其寻找水面下隐蔽平台,重复训练4天后撤去平台,测定大鼠从入水点到达原平台水域的时间;
检测b:测定脑组织匀浆铅含量及乙酰胆碱酶(AchE)活性。AchE活性检测原理:AchE可将乙酰胆碱(Ach)水解为胆碱和乙酸,胆碱与显色剂显色,根据颜色深浅计算活性。
请回答:
(1)表中用于评价大鼠学习记忆能力的指标是____,通过该指标可知____组大鼠学习记忆能力最弱。
(2)ACh是与学习记忆有关的神经递质,该递质由突触前膜释放进入____,与突触后膜上的受体结合,引发突触后膜____变化。ACh发挥效应后在____酶的催化下水解,本实验是通过检测单位时间内____的生成量,进而计算该酶的活性。
(3)表中结果表明:脑组织铅含量越高,ACh水解速度越____。
(4)水迷宫实验过程中,使短期记忆转化为长期记忆的措施是____,以此强化神经元之间的联系。
26.(12分)
为研究淹水时KNO3对甜樱桃根呼吸的影响,设四组盆栽甜樱桃,其中一组淹入清水,其余三组分别淹入不同浓度的KNO3溶液,保持液面高出盆土表面,每天定时测定甜樱桃根有氧呼吸速率,结果如图。
请回答:
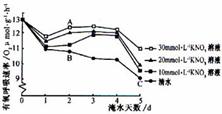 (1)细胞有氧呼吸生成CO2的场所是____,分析图中A、B、C三点,可知____点在单位时间内与氧结合的[H]最多。
(1)细胞有氧呼吸生成CO2的场所是____,分析图中A、B、C三点,可知____点在单位时间内与氧结合的[H]最多。
(2)图中结果显示,淹水时KNO3对甜樱桃根有氧呼吸速率降低有____作用,其中____mmol·L-1的KNO3溶液作用效果最好。
(3)淹水缺氧使地上部分和根系的生长均受到阻碍,地上部分叶色变黄,叶绿素含量减少,使光反应为暗反应提供的[H]和____减少;根系缺氧会导致根细胞无氧呼吸增强,实验过程中能否改用CO2作为检测有氧呼吸速率的指标?请分析说明____。
25.(15分)
固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想:
甲:Mg(NO3)2、NO2、O2 乙:MgO、NO2、O2 丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)实验前,小组成员经讨论认定猜想丁不成立,理由是_____________。
查阅资料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
针对甲、乙、丙猜想,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
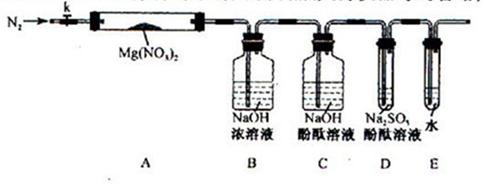
(2)实验过程
①取器连接后,放人固体试剂之前,关闭k,微热硬质玻璃管(A),观察到E 中有气泡连续放出,表明________
② 称取Mg(NO3)2固体3 . 79 g置于A中,加热前通人N2以驱尽装置内的空气,其目的是________;关闭K,用酒精灯加热时,正确操作是先________然后固定在管中固体部位下加热。
③ 观察到A 中有红棕色气体出现,C、D 中未见明显变化。
④ 待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1 . 0g
⑤ 取少量剩余固体于试管中,加人适量水,未见明显现象。
( 3 )实验结果分析讨论
① 根据实验现象和剩余固体的质量经分析可初步确认猜想_______是正确的。
② 根据D 中无明显现象,一位同学认为不能确认分解产物中有O2,因为若有O2,D中将发生氧化还原反应:_____________________(填写化学方程式),溶液颜色会退去;小组讨论认定分解产物中有O2存在,未检侧到的原因是_____________________。
③ 小组讨论后达成的共识是上述实验设计仍不完善,需改进装里进一步研究。
24.(14分)
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。其次除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO42-,其原因是___________[已知:Ksp(BaSO4)= 1.1 ×10-10 Ksp(BaCO3)= 5.1 ×10-9]
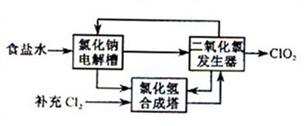 ②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有____________(填化学式),发生器中生成ClO2的化学方程式为___________。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
□ (D) +24NaClO3+12H2SO4=□ClO2↑+□CO2↑+18H2O+□_________
(3)ClO2和Cl2均能将电镀废水中的CN-氧化为无毒的物质,自身被还原为Cl-。处理含CN-相同量得电镀废水,所需Cl2的物质的量是ClO2的_______倍
23.(16分)
利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。
(1)工业上可用组成为K2O·M2O3·2RO2·nH2O的无机材料纯化制取的氢气
①已知元素M、R均位于元素周期表中第3周期,两种元素原子的质量数之和为27,则R的原子结构示意图为_________
②常温下,不能与M单质发生反应的是_________(填序号)
 a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH e.Na2CO3固体
a.CuSO4溶液 b.Fe2O3 c.浓硫酸 d.NaOH e.Na2CO3固体
(2)利用H2S废气制取氢气来的方法有多种
①高温热分解法
已知:H2S(g)==H2+1/2S2(g)
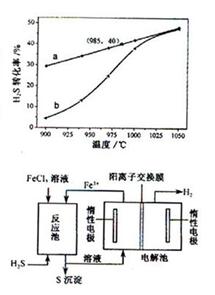
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见右图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=________;说明温度的升高,曲线b向曲线a逼近的原因:___________
②电化学法
该法制氢过程的示意图如右。反应池中反应物的流向采用气、液逆流方式,其目的是___________;反应池中发生反应的化学方程式为_____________________。反应后的溶液进入电解池,电解总反应的离子方程式为_______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com