
4.氯仿(CHCl3)不溶于水,密度比水大,是一种良好的有机溶剂,因保存不当受光照易被氧化而产生剧毒的光气(COCl2),反应如下:2CHCl3+O2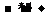 2HCl+2COCl2,则有关氯仿的以下实验操作正确的是( )
2HCl+2COCl2,则有关氯仿的以下实验操作正确的是( )
A用酚酞试液检查氯仿是否变质 B用硝酸银溶液检查氯仿是否变质
C用水检验氯仿是否变质 D需要倾倒氯仿检验时应在通风橱中进行
3.黄金首饰的纯度常用“K”来表示24K是纯金、标号为18K的首饰中黄金的质量分数是( )
A 25% B 75% C 18% D 36%
2.下列措施是为了防止环境污染的是( )
A食盐加碘 B禁止使用含铅汽油 C禁止饮用工业酒精 D禁止鸣放鞭炮
1.酸雨对下列物质的腐蚀作用最强的是( )
A铜制塑像 B大理石雕刻 C水泥路面 D铝制窗框
29.20.0克CuO溶于123.5克温热的20.0% H2SO4溶液。冷却到20 ℃时能从溶液中析出多少克CuSO4· 5H2O晶体?(20 ℃时CuSO4的溶解度为20.7克/100克水)
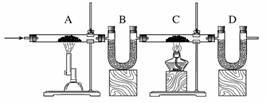
28.如下图所示,A管中盛有干燥的炭粉,C管中盛有干燥的氧化铜粉末,B、D两个U型管中装有氢氧化钠和氧化钙的固体混合物,用来充分吸收二氧化碳气体。将3.0克干燥的二氧化碳气体全部通入A管进行实验,实验结束后,B管质量增加0.8克,D管质量增加3.3克,计算进入C管和离开C管的一氧化碳的质量各为多少?
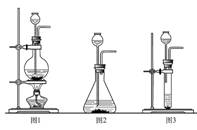
27.超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸之用。它与二氧化碳反应的化学方程式为4KO2+2CO2 = 2K2CO3+3O2,某学生为了验证这一实验,以大理石、足量的盐酸和超氧化钾为原料制取O2,设计出如下实验装置:
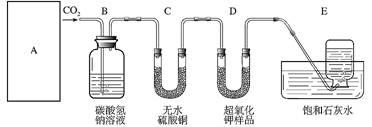
⑴A是制取CO2的装置,应从下列图1、图2、图3中选择 。B装置的作用是吸收A装置中产生的盐酸酸雾,C装置内可能出现的现象是 。为了检验E中收集到的气体,可以在取出集气瓶后,用 的木条伸入集气瓶内,木条会 。
⑵若E中的石灰水出现少量的白色沉淀,这是因为 。
⑶表明D中的超氧化钾样品接近反应完毕时的现象是 。
26.铜绿的主要成分是碱式碳酸铜(Cu2(OH)2CO3),它能跟酸反应生成铜盐、水和二氧化碳。某同学用小刀把家中旧铜器上的铜绿刮下,用来依次制取较纯净的硫酸铜、氧化铜和铜(为避免掺入固体杂质,他没有采用金属或碳置换化合物中的铜的方法)。制取步骤分为四步:
⑴填写下面表示制取步骤和方法的方框图(方框内填写所制取物质的化学式,方框前的横线上填写所加入的试剂及简要操作)。
铜绿 |
|
 |
Cu(OH)2 |
 |
|
 |
|
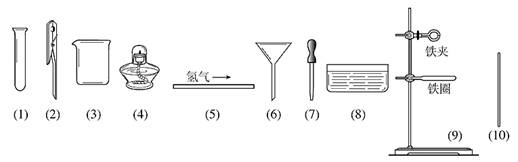
⑵根据上面的操作步骤,在下列所示仪器中选择实验所需用的仪器编号和名称:
⑶写出A、C操作过程中涉及的反应的化学方程式:
。
⑷如果实验装置及生成铜以前的操作都正确,但最后没有生成铜,这是因为 。
25.某学生在课外活动中用一定量的二价金属R和稀硫酸反应来制取氢气,所做5次实验结果记录如下表(假设每次实验所产生的氢气全部被收集,体积在同温同压下测定)。根据上述实验结果进行分析、计算,并回答下列问题:
⑴上述实验中,金属一定过量的组的编号是 ,稀硫酸一定过量的组的编号是 。
⑵若在当时实验条件下,H2的密度为0.085克/升,则反应所用金属R的相对原子质量为 。
⑶若所使用的稀硫酸密度为1.12克/厘米3,则反应所用的硫酸溶液中溶质的质量分数为 。
24.有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH中的一种或几种,为证明其组成,进行如下实验:
⑴取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是 ,原混合物中一定不含有 。
⑵向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原混合物中一定含有 。
⑶将实验⑴中得到的滤液分成两份,将实验⑵中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验⑵中产生的气体里含有 。
⑷向实验⑶中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有 ,根据实验全过程推断,原混合物中还含有 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com