
ij»Æ¹¤³§ÖʵƵēæ¼ī(Na2CO3)ÖŠŗ¬ÓŠÉŁĮæĀČ»ÆÄĘ”£ĻÖČ”Ä³ÖÖ½öŗ¬ĀČ»ÆÄĘŌÓÖŹµÄ“æ¼īѳʷ11.1g£¬Č«²æČܽāŌŚ120gĖ®ÖŠ£¬ŌŁ¼ÓČėĀČ»Æ±µČÜŅŗ144g£¬Ē”ŗĆĶźČ«·“Ó¦²¢Éś³ÉĢ¼Ėį±µ³Įµķ”£¹żĀĖøÉŌļŗó£¬³ĘµĆ³ĮµķÖŹĮæĪŖ19.7g”£
Ēó£ŗ1£®“æ¼īѳʷ֊Na2CO3µÄÖŹĮ攣
2£®ĀĖŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż”£
29£®(6·Ö)
[ŹµŃéĢ½¾æ]ĒāŃõ»ÆÄĘČÜŅŗÖŠÄÄŅ»ÖÖĮ£×Ó(H2O”¢Na+”¢OH-)ÄÜŹ¹ÖøŹ¾¼Į±äÉ«”£
[ŹµŃé²½Öč]
(1)ŌŚµŚŅ»Ö§ŹŌ¹ÜÖŠ¼ÓČėŌ¼2mLÕōĮóĖ®£¬µĪČė¼øµĪĪŽÉ«·ÓĢŖŹŌŅŗ£¬¹Ū²ģĻÖĻó”£
(2)ŌŚµŚ¶žÖ§ŹŌ¹ÜÖŠ¼ÓČėŌ¼2mLNaCl(pH=7)ČÜŅŗ£¬µĪČė¼øµĪĪŽÉ«·ÓĢŖŹŌŅŗ£¬¹Ū²ģĻÖĻó”£
(3)ŌŚµŚČżÖ§ŹŌ¹ÜÖŠ¼ÓČėŌ¼2mLNaOHČÜŅŗ£¬µĪČė¼øµĪĪŽÉ«·ÓĢŖŹŌŅŗ£¬¹Ū²ģĻÖĻó”£
ĶعżÉĻŹöŹµŃéĢ½¾æ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃé(1)擵½µÄĻÖĻóŹĒ___________________£¬ÄćµĆµ½µÄ½įĀŪŹĒ_________________________£»
ŹµŃé(2)擵½µÄĻÖĻóŹĒ___________________£¬ÄćµĆµ½µÄ½įĀŪŹĒ_________________________£»
ŹµŃé(3)擵½µÄĻÖĻóŹĒ___________________£¬ÄćµĆµ½µÄ½įĀŪŹĒ_________________________£»
28£®(4·Ö)Ä³Ń§ÉśĪŖĮĖÖ¤Ć÷ij°×É«¹ĢĢåŹĒĮņĖįļ§£¬ĖūÉč¼ĘĮĖĮ½²½³ĢŠņ£ŗ
(1)µŚŅ»²½£ŗĪŖĮĖÖ¤Ć÷NH4+µÄ“ęŌŚ£¬±ŲŠėµÄ²Ł×÷²½ÖčŹĒ_______________________________£¬µ±¹Ū²ģµ½______________________________µÄĻÖĻóŹ±£¬Ö¤Ć÷ÓŠNH4+“ęŌŚ”£
(2)µŚ¶ž²½£ŗĪŖĮĖÖ¤Ć÷SO42-µÄ“ęŌŚ£¬øĆѧɜÉč¼ĘĮĖČżÖÖ·½°ø£ŗ¢Ł¼ÓČėBaCl2ČÜŅŗ£¬ŌŁ¼ÓĻ”ŃĪĖį£»¢Ś¼ÓČė¹żĮæŃĪĖį»ÆĮĖµÄBaCl2ČÜŅŗ£»¢ŪĻČ¼Ó¹żĮæŃĪĖįĖį»Æ£¬ŌŁ¼ÓBaCl2ČÜŅŗ”£ÄćČĻĪŖÉĻŹöČżÖÖ·½°øÖŠ×īŗĻĄķµÄŅ»ÖÖ·½°øŹĒ____________________£¬¼ņŹöŗĻĄķµÄĄķÓÉ____________ ___________________________________”£
27£®(9·Ö)ŅŃÖŖøÉŌļ¼Į”°¼īŹÆ»Ņ”±µÄ³É·ŻŹĒ£ŗCaOŗĶNaOH£¬ŌŚ³±ŹŖµÄæÕĘųÖŠ¼«Ņ×±äÖŹ”£Ä³Š”×éµÄĶ¬Ń§¶ŌŹµŃéŹŅÖŠŅ»Ęæ·ÅÖĆŅŃ¾ĆµÄ”°¼īŹÆ»Ņ”±½ųŠŠĮĖČēĻĀµÄĢ½¾æ£ŗ
”””” (1)¼×Ķ¬Ń§²ĀĻė£ŗѳʷֻÓėæÕĘųÖŠµÄĖ®ÕōĘū·¢ÉśĮĖ×÷ÓĆ”£ŌņNaOH»į________________£»CaO»į±äÖŹ£¬Ęä·“Ó¦µÄĄąŠĶĪŖ__________________·“Ó¦”£
”””” (2)ŅŅĶ¬Ń§²ĀĻė£ŗ(Ēė½«±ķøńĢīŠ“ĶźÕū)
|
²Ā”””” Ļė |
ŹµŃéÉč¼Ę |
ĻÖĻó |
ÅŠ¶Ļ |
|
|
²ĀĻėa |
ѳʷŗ¬Ģ¼ĖįŃĪ |
ȔɣĮæѳʷ£¬µĪ¼ÓŃĪĖį |
ĪŽĘųÅŻ·Å³ö |
”” |
|
²ĀĻėb |
ѳʷ֊ŗ¬ÓŠNa2CO3£¬ĒŅ»¹ŗ¬ÓŠCaO”¢Ca(OH)2”¢CaCO3ÖŠµÄŅ»ÖÖ |
ȔɣĮæČÜÓŚĖ®£¬¹żĀĖ£¬ŌŚĀĖŅŗÖŠµĪČėĻ”ŃĪĖį |
”” |
²ĀĻėb³ÉĮ¢ |
(3)±ūĶ¬Ń§½ųŠŠĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé£ŗ
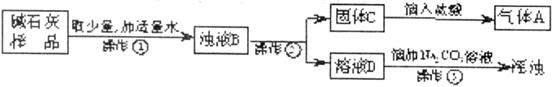
”””” Ķ¼ÖŠ²Ł×÷¢Ł”¢¢Ś¶¼ŅŖÓƵ½²£Į§°ō£¬ĘäÖŠ²Ł×÷¢Ł²£Į§°ōµÄ×÷ÓĆŹĒ______________________£»“Ó²Ł×÷¢ŪµÄĻÖĻó·ÖĪö£¬ČÜŅŗDÖŠŗ¬ÓŠµÄĪļÖŹŹĒ____________£»Š“³öČÜŅŗDÓėNa2CO3ČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½__________________________£¬·“Ó¦ĄąŠĶĪŖ_______________”£
26£®(4·Ö)“ÓA-DÖŠŃ”ŌńÕżČ·µÄŠņŗÅ£¬ĢīæÕ(1)-(4)Ģā”£
A£®¼ÓŹŹĮæĻ”ŃĪĖį£¬½Į°č”¢Õō·¢”¢½į¾§”””””””””””” B£®¼ÓŹŹĮæĻ”ŃĪĖį£¬½Į°č”¢¹żĀĖ”¢Ļ“µÓ
C£®¼ÓŹŹĮæĖ®£¬Čܽā”¢¹żĀĖ”¢Õō·¢”¢½į¾§”””””””” D£®¼ÓŹŹĮæĖ®£¬Čܽā”¢¹żĀĖ”¢Ļ“µÓ
(1)Ģį“æŗ¬ÓŠÉŁĮæÄąÉ³µÄ“ÖŃĪ________________________£»
(2)“Ó²ŻÄ¾»ŅÖŠĢįČ”Ģ¼Ėį¼Ų________________________£»
(3)³żČ„ĀČ»ÆÄĘÖŠµÄÉŁĮæĢ¼ĖįÄĘ________________________£»
(4)ŹµŃéŹŅ³£ÓĆ¼ÓČČĀČĖį¼ŲÓė¶žŃõ»ÆĆĢµÄ»ģŗĻĪļĄ“ÖĘČ”ŃõĘų£¬ÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
2KClO3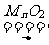 2KCl+3O2”ü£¬“Ó·“Ó¦ŗóµÄ²ŠŌüÖŠ»ŲŹÕ¶žŃõ»ÆĆĶ(MnO2²»ČÜÓŚĖ®) __________.
2KCl+3O2”ü£¬“Ó·“Ó¦ŗóµÄ²ŠŌüÖŠ»ŲŹÕ¶žŃõ»ÆĆĶ(MnO2²»ČÜÓŚĖ®) __________.
25£®(4·Ö)¼×ŗĶŅŅĮ½ÖÖĪļÖŹµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾£ŗ
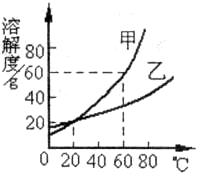
(1)20”ꏱ£¬¼×ĪļÖŹµÄČܽā¶Č___________ (Ģī”°“óÓŚ”±”¢”°µČÓŚ”±»ņ”°Š”ÓŚ”±)ŅŅĪļÖŹµÄČܽā¶Č£»
(2)60”ꏱ£¬ŌŚ100gĖ®ÖŠ¼ÓČė80g¼×¹ĢĢ壬³ä·Ö½Į°čĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹżŹĒ____________”£
(3)80”ꏱ£¬Ä³ČÜŅŗĖłČܽāµÄ¼×ŗĶŅŅĪļÖŹ¶¼Ņѱ„ŗĶ”£°ŃøĆČÜŅŗĄäČ“µ½ŹŅĪĀ£¬ÓŠ¾§ĢåĪö³ö£¬¾¼ģŃé·¢ĻÖĪö³öµÄ¾§ĢåÖ÷ŅŖŹĒ¼×£¬ĘäŌŅņŹĒ___________ (Ģī±ąŗÅ)
”” ¢Ł80”ꏱ£¬¼×µÄČܽā¶Čøü“ó”” ¢Ś80”ꏱ£¬ŅŅµÄČܽā¶Čøü“ó
”” ¢Ū¼×µÄČܽā¶ČŹÜĪĀ¶Č±ä»ÆµÄÓ°Ļģ±ČŅŅ“ó
(4)ČōÓŠŅ»¼×µÄČÜŅŗÖŠ»ģÓŠÉŁĮæŅŅŅŖĢį“æ¼×æɲÉÓĆ____________·½·Ø”£
24£®(5·Ö)2005Äź¹ś¼ŅÖŹ¼ą¾Ö·¢²¼¹«øę£ŗ½ūÖ¹Éś²ś»ņ½ųæŚÓŠŗ¦µÄDEHA(C22H42O4)ŌöĖܼĮµÄPVCŹ³Ę·±£ĻŹÄ¤”£ŹŠ³”ÉĻ±£ĻŹÄ¤µÄÖÖĄą½Ļ¶ą£¬ŅŖ±£Ö¤Ź³Ę·°²Č«£¬±ŲŠė×¢ŅāŹ¶±š”£
(1)DEHAÓÉ__________ÖÖŌŖĖŲ×é³É£¬·Ö×ÓÖŠC”¢HŌ×ÓøöŹż±ČĪŖ___________”£DEHAŹĒŅ»ÖÖ____________ (Ģī”°ÓŠ»śĪļ”±»ņ”°ĪŽ»śĪļ”±)£¬Ź¹ÓĆ²»µ±Ņ×ĶعżŹ³Īļ½ųČėČĖĢ唣
(2)ĖÜĮĻ±£ĻŹÄ¤²»ŅĖ°ü×°ČȵÄÓĶÕØŹ³Ę·£¬ŅņĪŖøßĪĀŹ±±£ĻŹÄ¤ÖŠŌöĖܼĮ·Ö×ÓøüČŻŅדӱ£ĻŹÄ¤½ųČėŹ³Ę·ÖŠ”£“ÓĪ¢¹Ū½Ē¶Č½āŹĶĘäŌŅņŹĒ__________________”£
(3)Č«ŹĄ½ēĆæğɜ²ś”¢Ź¹ÓĆŌ¼ÉĻĒ§Ķņ¶Ö±£ĻŹÄ¤£¬Ź¹ÓĆŗó³ÉĪŖĖÜĮĻĄ¬»ų£¬ĪŖĮĖ±£»¤»·¾³£¬ÄćĢį³öµÄŅ»ĢõŗĻĄķ»Æ½ØŅéŹĒ______________________________”£
23£®(4·Ö)±ū°±Ėį(C3H7O2N)ŹĒŅ»ÖÖ°±»łĖį£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Ćæøö±ū°±Ėį·Ö×ÓÖŠ¹²ŗ¬ÓŠ____________øöŌ×Ó£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæŹĒ____________£»
(2)±ū°±ĖįÖŠø÷ŌŖĖŲµÄÖŹĮæ±ČŹĒ____________£»
(3)±ū°±ĖįÖŠµŖŌŖĖŲµÄÖŹĮæ·ÖŹżŹĒ____________”£
22£®(8·Ö)ŅĄ¾ŻĖłŃ§µÄ»ÆѧÖŖŹ¶»Ų“š£ŗ
(1)ĻĀĮŠ“ėŹ©“ķĪóµÄŹĒ____________(ĢīŠņŗÅ)£ŗ¢ŁÓĶ¹ų²»É÷×Å»š£¬Į¢¼“øĒÉĻ¹ųøĒ£»¢ŚĖį»ņ¼īČÜŅŗ½¦ČėŃŪ¾¦Ąļ£¬Į¢¼“ÓĆ“óĮæĖ®³åĻ“£»¢ŪŹŅÄŚ×Å»šŹ±ÓĆŹŖĆ«½ķĪę×”æŚ±Ē”¢ŁéŁėĒ°½ųŃ°ÕŅ³öæŚ£»¢ÜÓĆÉśŹÆ»Ņ“¦Ąķ±»ĖįĪŪČ¾µÄŗÓĖ®£»¢ŻŹŅÄŚĆŗĘųŠ¹Ā©£¬Į¢¼“¹Ų±ÕĆŗĘųĘæ·§”¢²¢“ņµē»°±Ø¾Æ”£
(2)Ī“³ÉŹģĖ®¹ūŗ¬÷·Ėį¶ų¾ßӊɬĪ¶£¬ĶŃɬµÄ·½·ØÖ®Ņ»ŹĒÓĆŹÆ»ŅĖ®½žÅŻĖ®¹ū”£ŌņÓĆÉśŹÆ»ŅÖĘ³ÉŹÆ»ŅĖ®µÄ»Æѧ·½³ĢŹ½ĪŖ______________________________
(3)Ļ”ŹĶÅØĮņĖįŹ±£¬Ņ»¶ØŅŖ°Ń____________ŃŲČŻĘ÷±ŚĀżĀż×¢Čė____________ÖŠ£¬²¢²»¶Ļ½Į°č£¬ĘäŌŅņŹĒ_________________________”” _____________________________”£
(4)2007Äź6ŌĀ5ČÕ£¬ŌŚ”°ÄĻŗ£Ņ»ŗÅ”±“ņĄĢ³öµÄĪÄĪļÖŠ£¬”°öĢ½šĮśĪĘ½šŹÖļķ”±¹ā²Ź¶įÄ攢ĶźŗĆĪŽĖš£»Ķ¾µ±ķĆęÓŠĶŠā£»ĢśĘ÷ŌņŠā¼£°ß°ß»ņµ“Č»ĪŽ“ę”£ÕāĖµĆ÷½š”¢Ķ”¢ĢśÕāČżÖÖ½šŹōµÄ»ī¶ÆŠŌ“ÓĒæµ½ČõµÄĖ³ŠņŹĒ(ĢīŌŖĖŲ·ūŗÅ) ____________£»ŅŌĻĀ“ėŹ©²»ÄÜ×čÖ¹ĢśĘ÷ÉśŠāµÄŹĒ(ĢīŠņŗÅ) ____________£ŗ¢ŁÅēĘį”¢¢ŚĖ¢ĢĀ“É”¢¢ŪĖ®Ļ“”¢¢Ü¶ĘŅ»²ćÄĶøÆŹ“½šŹō”£
21£®(5·Ö)2007Äź6ŌĀ9ČÕ£¬”°°Ė¹ś¼ÆĶÅŹ×ÄŌ»įŅé”±Ņ»ÖĮĶ¬Ņā¼õÉŁĪĀŹŅĘųĢåµÄÅÅ·Å”£Ēėøł¾ŻĶ¼»Ų“š£ŗ
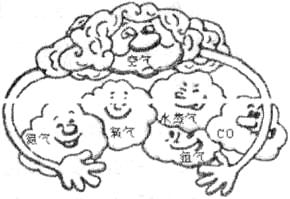
(1)ŌŚĪļÖŹ·ÖĄąÖŠæÕĘųŹōÓŚ____________”£
(2)ÓĆ»ÆѧŹ½ĢīæÕ£ŗÖĘŌģ»Æ·Ź²¢»¹æÉŅŌ×ö±£»¤ĘųµÄŹĒ______£»Äܹ©øųČĖĄąŗōĪüµÄŹĒ________£»ÉĻŹö”°ĪĀŹŅĘųĢå”±ŹĒÖø____________£»ĪĀŹŅĘųĢåŌö¶ąµÄÖ÷ŅŖŌŅņŹĒ__________________”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com