
37.(8分)在化学实验课上,老师让同学们完成分组实验:自己设计实验方案证明氢氧化钠与稀盐酸恰好完全反应。下面是来自不同小组的三位同学的实验过程,请你帮助他们分析、解决实验过程中遇到的问题。
[活动与探究](1)欢欢同学先按下图所示的方法向试管中加入约2mL氢氧化钠溶液。又滴入几滴无色酚酞试液,溶液变红,然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。请你指出欢欢同学操作中的错误:_________________。
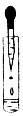
(2)迎迎同学先向试管中加入约2mL氢氧化钠溶液,又倾倒了一些稀盐酸之后,她想起还没有加入指示剂,于是又补加了几滴无色酚酞试液,发现溶液仍呈无色,于是她认为此时恰好完全反应。你认为迎迎同学得出的结构是否正确?____________________。
(3)妮妮同学先向试管中加入约2mL氢氧化钠溶液,又滴入几滴无色酚酞试液,溶液变红,然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。但在滴入稀盐酸的过程中,妮妮观察到曾有少量气泡出现。请你帮助她分析产生气泡的原因可能是_________________。 (写一条即可)。
[反思与评价]①请你帮迎迎想一想,要想证明她得出的“恰好完全反应”的结论是否正确,应选择的试剂是_________________________。
②根据以上三位同学的实验过程,请你思考一下,为了保证氢氧化钠溶液与稀盐酸恰好完全反应,实验成功的关键是______________、_______________、________________。
[拓展与应用]请举一例说明中和反应在生产、生活中的应用:__________________。
36.(8分)实验室一般用块状石灰石(大理石)和稀盐酸反应来制取二氧化碳,而不用粉末状石灰石(大理石)与稀盐酸反应制取二氧化碳、小杨、小柳、小梅三位同学对此进行探究。
[提出问题]实验室为什么不用粉末状石灰石(大理石)与稀盐酸反应来制取二氧化碳?
[作出猜想]①粉末状石灰石(大理石)与稀盐酸反应速率太慢;②粉末状石灰石(大理石)与稀盐酸反应速率太快。
[实验设计]装置如甲、乙图所示:广口瓶大小相同,胶头滴管大小相同。内装等体积、等质量、相同浓度的稀盐酸(设该盐酸能将石灰石完全反应)。实验时,同时将两胶头滴管内的盐酸全部挤入装有石灰石的小试管内。实验中观察到的现象是__________,石灰石跟稀盐酸发生反应的化学方程式为_____________。
[结论与解释]小杨认为,不能选用粉末状石灰石与稀盐酸反应来制取二氧化碳,原因是________________。小柳通过思考得出:当其他条件一定时,反应物之间接触面积越大,化学反应的速率就越快。
[拓展与应用](1)实验室能否用稀硫酸与块状石灰石(大理石)反应来制取二氧化碳? ___________,理由是__________________________。
(2)根据已有知识,请你归纳出另外两个可能影响化学反应速率的因素:____________,________________。
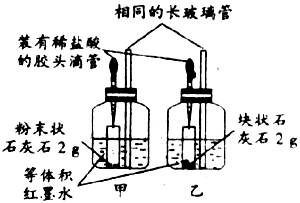
35.(4分)用下列装置进行证明质量守恒定律的实验。
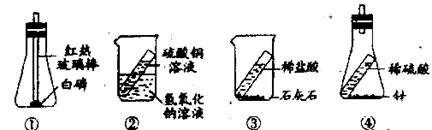
(1)反应前后容器中物质的总质量不相等的是__________(填序号)。
(2)能用于验证质量守恒定律的是____________(填序号)。
(3)再加一个实验,用天平称量光亮铁钉的质量为xg;其生锈后的质量为yg。则x和y的关系为:x________________(填“>”、“=”、“<”)。
(4)通过对以上几个实验的分析,你认为用有气体参加或生成的化学反应来验证质量定恒定律时,应__________,才能判定参加化学反应的反应物总质量和生成物总质量是否相等。
34.(4分)甲、乙、丙三种物质的溶解度曲线如图所示,据图回答:
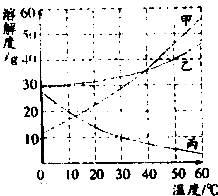
(1)50℃时,乙物质的溶解度是________________g;
(2)30℃时,三种物质的溶解度由大到小的顺序为_____________________;
(3)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是___________________;
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是___________________。
33.(6分)同学们在学习化学时,要对化学知识不断进行总结,请你参与总结。
(1)我们学习了盐,日常生活中所说的盐是指____________(填化学式),它是人体进行正常新陈代谢的必需品,有着广泛的用途,如_____________。
(2)我们认识了几种重要的盐,如碳酸钠和碳酸钙等。候氏制碱法中的“碱”实际上是____________(填化学式),由于这两种盐能与稀盐酸发生反应产生气体,所以可用此方法检验CO32-的存在,其原理是_____________(以碳酸钠为例,用化学方程式表示),该反应所属的化学反应基本类型是__________________。
32.(8分)请写出下列反应的化学方程式
(1)水在通电情况下分解______________________________。
(2)白磷在空气中燃烧__________________________________。
(3)甲烷(CH4)在空气中燃烧__________________________________。
(4)将二氧化碳通入足量澄清石灰水中___________________________________。
31.(3分)某品牌矿泉水,其外包装上部分文字说明如下图所示。请回答下列问题:

(1)说明书中的“钙”是指_______(填 “分子”、“原子” 或 “元素” );
(2)纯净优质的矿泉水属于________(填 “纯净物” 或 “混合物” )
(3)偏硅酸中硅元素的化合价是_________________。
30.与下列图像对应的叙述关系正确的是
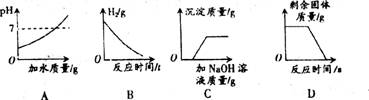
A.向pH=3的溶液中加水
B.一定质量的稀盐酸与锌粒反应
C.向H2SO4和CuSO4混合溶液中加NaOH溶液
D.煅烧一定质量的石灰石
第Ⅱ卷(非选择题共60分)
29.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂。下列叙述中,正确的是
A.丁酸乙酯是由20个原子构成的
B.丁酸乙酯的相对分子质量为116g
C.丁酸乙酯中碳、氢、氧元素的质量比为l8:3:8
D.一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2
28.除去下列各组物质中杂质,所选用的试剂及操作方法均正确的是(括号内的物质为杂质,所选试剂均足量)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com