
2.久置于空气中的下列物质,因被氧化而呈黄色的是
A.浓硝酸 B.氯化亚铁溶液 C.溴苯 D.溴化银
1.导致下列现象的主要原因与排放SO2有关的是
A.酸雨 B..光化学烟雾 C.臭氧空洞 D.温室效应
33.某天然碱(纯净物)可看作由CO2和NaOH反应后的产物所组成。称取天然碱样品四份,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如下表:
|
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
盐酸液的体积(mL) |
30 |
30 |
30 |
30 |
|
样品(g) |
3.32 |
4.15 |
5.81 |
7.47 |
|
二氧化碳的体积(mL) |
672 |
840 |
896 |
672 |
(1)由第Ⅰ组数据中的CO2体积与样品质量之比,可以推测用2.49g样品进行同样的实验时,产生CO2_________mL(标准状况)。
(2)另取3.32g天然碱样品于300℃加热分解至完全(300℃时NaCO3不分解),产生CO2112mL(标准状况)和水0.45g,计算并确定该天然碱的化学式。
(3)已知Na2CO3和HCL(aq)的反应分下列两步进行:
Na2CO3+HCL→NaCL+NaHCO3
Na2CO3+HCL→NaCL+CO2↑+H2O
(4)依据上表所列数据以及天然碱的化学式,讨论并确定上述实验中CO2(标准状况)体积V(mL)与样品质量W(g)之间的关系式。
32.美籍埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而获得1999年诺贝尔化学奖。激光有很多用途,例如波长为10.3微米的红外激光能切断B(CH3)3分子中的一个B-C键,使之与HBr发生取代反应:
B(CH3)3+HBr B(CH3)2Br+CH4
B(CH3)2Br+CH4
而利用9.6微米的红外激光却能切断两个B-C键,使之与HBr+CH4
而利用9.6微米的红外激光却能切断两个B-C键,并与HBr发生二元取代反应。
(1)试写出二元取代的代学方程式:
(2)试写出二元取代的化学方程式:
(3)现用5.6g B(CH3)3和9.72g HBr正好完全反应,则生成物中除了甲烷外,其他两种产物的物质的量之比为多少?
31.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应。
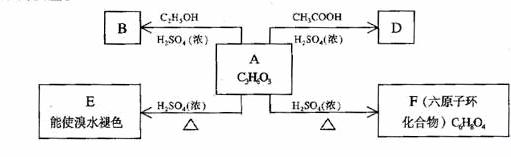
试写出:
化合物的结构简式:A___________________ B_________________
D___________________
化学方程式:A→E_____________________________________
A→F____________________________________
反应类型:A→E______________,A→F_______________
30.某烃A,分子量为140,其中碳的质量分数为0.857。A分子中有两个碳原子不与氢直接相连。A在一定条件下氧化只生成G,G能使石蕊试液变红。
已知
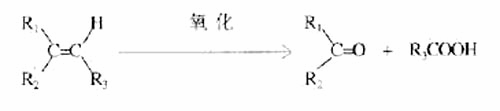
试写出:
(1) A的分子式________________
(2) 化合物A和G的结构简式:
A__________________________
G_________________________
(3)与G同类的同分异构体(含G)可能有________种
(五)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与G之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的钢的质量分数偏小的原因可能是_______________-,在B与G之间加入的装置可以是____________________,其中盛放的药品是__________________。
29.我国规定饮用水质量标准必须符合下列要求:
|
PH值 |
6.5-8.5 |
|
Ca2+,Mg2+总浓度 |
<0.0045mol/L |
|
细菌总数 |
<100个/mL |
以下是源水处理成自来水的工艺流程示意图
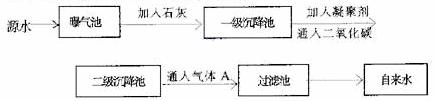
(1) 源水中含Ca2+、Mg2+、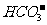 、CL-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_____________
、CL-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式_____________
(2) 凝聚剂除去悬浮固体颗粒的过程__________(填写编号,多选倒扣)
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O常用的凝聚剂,它在水中最终生成___________沉淀。
(3) 通入二氧化碳的目的是_________________和_____________。
(4) 气体A的作用是__________。这种作用是基于气体A和水反应的产物具有______________性。
(5) 下列物质中,______________可以作为气体A的代用品。(填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
(四)计算:样品中铜的质量分类=___________________(用含W、m1、m2的代数式表示)
(三)实验内容:
|
实验过程 |
实验现象 |
有关化学方程式 |
|
在C中加入样品标本W克,D中装入精品后并称量为m克。连接好仪器后,检查气密性 |
|
|
|
打开A的活塞,慢慢洋加溶液。 |
|
|
|
对G进行加热。当G中药品充分反应后。关闭A的活塞。停止加热: |
|
|
|
冷却后,称量D的质量为m2克。 |
|
|
(二)实验用品:仪器:天平、分液漏斗、锥形瓶、硬玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰。浓硫酸等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com