
14.在一定温度下,一定体积的密闭容器中如下平衡:H2(气)+ I2(气) 2HI(气)。已知H2和I2的起始浓度均为0.10mol·L-1,达平衡时HI的浓度为0.16mol·L-1。若H2和I2的起始浓度均变为0.20mol·L-1时,则平衡时H2的浓度(mol·L-1)是
A.0.16 B.0.08 C.0.04 D.0.02
13.20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是
A.25℃时,饱和KCl溶液的浓度大于4.0 mol·L-1
B.此溶溶中KCl的质量分数为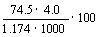 %
%
C.20℃时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液
D.将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
12.从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O====7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
A.Cu2S既是氧化产物又是还原产物
B.5mol FeS2发生反应,有10mol电子转移
C.产物中的SO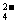 离子有一部分是氧化产物
离子有一部分是氧化产物
D.FeS2只作还原剂
11.已知0.lmol·L-1的二元酸H2A溶液的pH=4.0,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有:[Na+]+[H+]=[HA-]+[OH-]+2 [A2-]
D.在Na2A溶液中一定有:[Na+]>[A2-]>[H+]>[OH-]
10.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.Na2SO3溶液(BaCl2) B.FeCl2溶液(KSCN)
C.KI(淀粉溶液) D.HCHO溶液(石蕊试液)
9.用NA表示阿伏加德罗常数,下列叙述中正确的是
A.0.1 mol·L-1稀硫酸100mL中含有硫酸根个数为0.l NA
B.l mol CH3+(碳正离子)中含有电子数为10 NA
C.2.4g金属镁与足量的盐酸反应,转移电子数为2 NA
D.12.4g白磷中含有磷原子数为0.4 NA
8.下列指定微粒的个数比为2:1的是
A.Be2+离子中的质子和电子
B.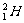 原子中的中子和质子
原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
7.近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80MPa下合成出金刚石,具有深远意义。下列说法不正确的是
A.由二氧化碳合成金刚石是化学变化
B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠
D.金刚石中只含有非极性共价键
31.(43分)Fe是地壳中含量很丰富的元素,也是生物体所必需的元素。
(1)(17分)自然界中铁矿石主要有赤铁矿和磁铁矿,金属铁是在高炉中冶炼的,高炉炼铁除了加入铁矿石外,还需加入焦炭和石灰石。请填空:
①写出磁铁矿主要成分的化学式: 。
②写出赤铁矿被还原成铁的化学方程式: 。
③写出焦炭在高炉中参与反应的两个化学方程式: 。
④写出CaCO3所参与反应的两个化学方程式: 。
28.(10分)在某些酶的催化下,人体内葡萄糖的代谢有如下过程:
葡萄糖→……→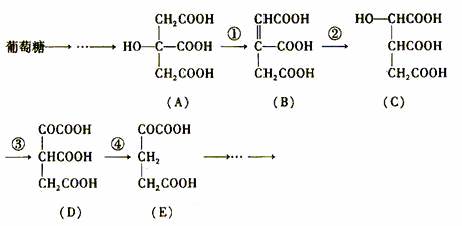
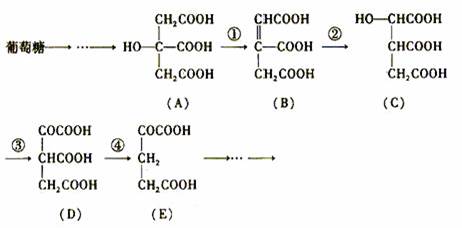 →……→
→……→
请填空:
(1)过程①是 反应,过程②是 反应,过程③是 反应(填写反应类型的名称)。
(2)过程④的另一种生成物是 (填写化学式)。
(3)上述物质中 和 互为同分异构体(填写字母代号)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com