
3.下列条件下,两瓶气体中所含的原子数相等的是
A.同压强、同体积的N2O和CO2
B.同温度、同体积的氮气和氯气
C.同体积、同密度的乙烯和丙烯
D.同温度、同压强、同体积的氦气和氢气
2.向盐酸中加入浓H2SO4时,会有白雾生成,不属于产生该现象的原因的是
A.盐酸具有挥发性
B.浓H2SO4具有吸水性
C.浓盐酸具有还原性
D.气体溶质的溶解度随温度升高而降低
1.下列说法正确的是
A.强极性键形成的化合物不一定是强电解质
B.强电解质溶液导电能力一定比弱电解质溶液强
C.NaCl溶液在电流的作用下电离成钠离子和氯离子
D.SO2的水溶液可以导电,所以SO2是电解质
25.(10分)铜是重要的工业原材料,现有Cu、Cu2O和CuO组成的混合物,某研究性学习小组为了探究其组成情况,向混合物中加入100mL 0.6mol/LHNO3溶液刚好使其溶解,同时收集到224mLNO气体(标准状况)。请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的化学反应方程式_______________________________;
(2)产物中硝酸铜的物质的量______________mol;
(3)如混合物中含0.01molCu,则其中Cu2O、CuO的物质的量分别是________mol、__________mol;
(4)如混合物中Cu的物质的量为X,求X的取值范围________________。
24.(8分)碘盐是日常生活中必不可少的调味品,我国强制推广食用加碘盐。根据GB5461--《国家食用盐标准》,碘元素含量为20-50mg/kg为合格。质量监督部门为检测某品牌加碘盐是否合格,进行了如下实验:称取250g 某品牌加碘盐样品,在酸性条件下用足量KI溶液将其中IO3-全部转化成I2,生成的I2再用0.010mol/L的硫代硫酸钠溶液滴定,滴定到终点时用去12mL。
有关反应如下:
①IO3-+5I-+6 H+ 3I2+3H2O
3I2+3H2O
②I2+2S2O32- 2I-+S4O62-
2I-+S4O62-
(1)用硫代硫酸钠溶液滴定I2时,应用_________作指示剂,滴定到终点的现象是________;
(2)试通过计算说明该加碘食盐是否为合格产品(写出具体的计算过程)。
23.(10分)塑料是日常生活中常用的合成高分子材料,常用塑料F、G均可由某烃经下列反应得到:
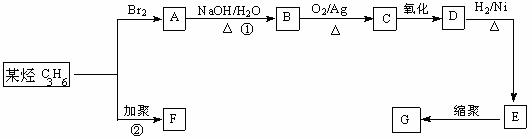
(1)写出高分子化合物G的结构简式:_____________________;
(2)写出反应①的化学方程式:_________________________________________;
(3)写出反应②化学方程式:_____________________________________________;
(4)PBT(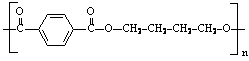 )是一种最重要的工程塑料之一。
)是一种最重要的工程塑料之一。
已知:①、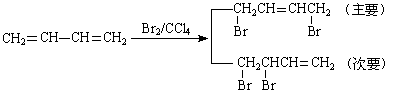
②、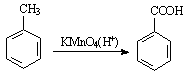
请设计方案以CH2=CHCH=CH2、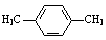 为原料合成PBT;请用反应流程图表示,并注明反应条件。
为原料合成PBT;请用反应流程图表示,并注明反应条件。
示例:由乙醇合成聚乙烯的反应流程图可表示为
CH3CH2OH CH2=CH2
CH2=CH2
 CH2-CH2
CH2-CH2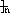
合成PBT的反应流程图为__________________________________________________
22.(8分)禽流感在全球的蔓延,使人们谈“禽”色变。从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物。
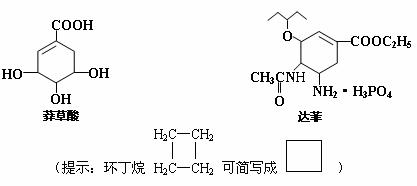
(1)达菲分子中含有的官能团有_____________________________________________;
(2)莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为: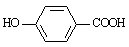 ),其反应类型为:_______________;
),其反应类型为:_______________;
(3)请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
_______________________________________________________________________;
(4)B的同分异构体中既含有酚羟基又含有酯基的共3种,写出其中一种同分异构体的结构简式______________________________。
21.(10分)在装修居室时,如使用不合格的建筑、装潢材料,易造成“室内空气污染”,影响人们身体健康,造成室内空气污染的有毒物质主要有甲醛、苯、氨、氡等。学好化学有助于我们设法减少居室内的空气污染,消除空气中的有害物质对人体可能产生的影响。回答下列问题:
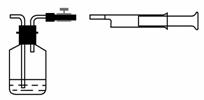 (1)我国《室内空气质量标准》规定室内空气中甲醛含量不得超过0.08mg/m3。小陈同学为测定新居内空气中甲醛含量是否超标,设计了如图所示的简易实验装置:
(1)我国《室内空气质量标准》规定室内空气中甲醛含量不得超过0.08mg/m3。小陈同学为测定新居内空气中甲醛含量是否超标,设计了如图所示的简易实验装置:
①请你帮助小陈同学选择装置中试剂瓶内的药品:_____(填序号);
a.银氨溶液 b.酸性高锰酸钾溶液 c.新制得氢氧化铜悬浊液
根据你的选择,为使实验现象明显,你认为对所选择试剂的浓度有什么要求__________________________________________________________________;
②在检查好装置气密性和选择好试剂瓶内的药品后,请你帮助小陈同学完成该实验的操作:________________________________________________________;
③若试剂瓶内溶液的体积和浓度已知,实验时还需测定的数据有:
_______________________________、________________________________;
(2)请你提出减少室内空气污染的措施:____________________________________;
20.(10分)下图是部分元素的单质及其化合物的转化关系图(有关反应的条件及部分反应物或生成物已略去);
已知:C、D、F均为单质,其中C、D在常温、常压下是气体;反应②是化工生产中的重要反应,生成物E具有漂白性;J、K均为不溶于水的沉淀,其中J为红褐色。
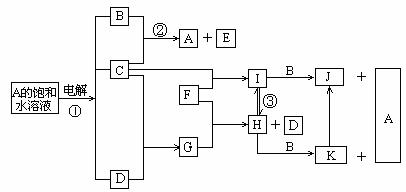
请回答下列问题:
(1)A的电子式:_______________;
(2)反应②的离子方程式是___________________________________;
(3)反应③的化学方程式是____________________________________;
(4)实验室由H制备少量K的方法:是用胶头滴管吸取B溶液,将滴管尖端插入盛有新制H溶液试管底部,慢慢挤出B溶液即可,观察到的现象为:
________________________________________________________;
(5)当有1.12L(标准状况)D生成时,反应①中转移的电子数为___________;
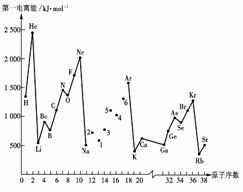
19.(8分)第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na--Ar之间六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_____________;
(3)上图中5号元素在周期表中的位置是________________________________________;
(4)上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:__________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com