
5. 下列说法或表示方法正确的是
A.反应物总能量低于生成物总能量时,该反应不能发生
B.向等质量的碳酸钠粉末滴加少量水和大量水的热效应相同
C.由石墨比金刚石稳定,可知C(石墨)→ C(金刚石);ΔH>0
D.在101 kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g) + O2(g) == 2H2O(l);ΔH=-285.8 kJ/ mol
4. 物质间某些方面存在相似性的同时还存在某些性质的递变性,下列说法正确的是
A.HClO4、H2SO4、H3PO4的酸性逐渐增强
B.等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的量由少到多
C.CH3CH2OH、 、CH3COOH电离出H+的能力由弱到强
、CH3COOH电离出H+的能力由弱到强
D.物质的量浓度相等的NaCl、MgCl2、AlCl3三种溶液的pH由小到大
3. 下列实验操作正确的是
①将未经湿润的pH试纸浸到某溶液中,过一会取出与标准比色卡比较测得该溶液的pH
②使用碱式滴定管盛装KMnO4溶液滴定Na2SO3溶液
③将3滴浓硫酸滴入蓬松的脱脂棉中搅拌加热,在其中加入2滴2%CuSO4溶液,再加入足量的10%NaOH溶液,并加热至沸腾,可证明纤维素的水解
④用热水加热乙醛和银氨溶液的混合液做乙醛的银镜实验
⑤向蛋白质溶液中加入无机盐(如Na2SO4、CuSO4)浓溶液,可使蛋白质盐析而分离提纯
⑥实验室制肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂
⑦配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加浓硫酸
⑧检验红砖中的氧化铁成分时,向红砖粉末中加入盐酸,放置至充分沉淀后,取上层清液于试管中,滴加KSCN溶液2滴-3滴即可
A、①③⑥⑧ B、②③⑥⑧ C、②④⑥⑦ D、③④⑧
2.分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
② 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③ 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④ 根据反应中的热效应将化学化学反应分为放热反应和吸热反应
⑤根据氧化物中含有金属元素属碱性或两性氧化物,含有非金属元素属酸性氧化物
⑥根据盐的离子组成分为复盐、混盐、络盐;还可分为正盐、酸式盐、碱式盐
⑦根据微粒间相互作用分为离子键、共价键、氢键等化学键和分子间作用力
⑧根据分子中含有苯环分为烃及其衍生物、芳烃及其衍生物,如苯乙烯是苯的同系物
A.①③⑧ B.②④⑥ C.①②④⑦ D.②③④⑤
1.下列物质使用合理的是
①铁酸钠(Na2FeO4)用于水消毒净化 ②用加酶洗衣粉洗涤毛料服装
③用甲醛溶液浸泡海产食品 ④酚醛树脂制作高弹力运动鞋
⑤硫黄熏制银耳,使银耳漂白 ⑥在制玻璃的原料中再加入Co2O3制成蓝色玻璃
A.②④⑥ B.①③⑤ C.①⑥ D.②③⑤⑥
25.(10分)取一定质量的NaBr、NaI的混合物平均分成五等份,分别加水配成溶液并编号为甲、乙、丙、丁、戊,在分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干、灼烧得固体,通入氯气的体积与最终所得固体质量记录如下:
|
编号 |
甲 |
乙 |
丙 |
丁 |
戊 |
|
固体组成 |
|
NaI
NaBr NaCl |
|
|
NaCl |
|
氯气的体积/mL |
V |
2V |
3V |
4V |
5V |
|
固体质量/g |
54.62 |
43.64 |
35.48 |
30.14 |
29.25 |
求:(1)请填写表中空白;
(2)标准状况下氯气的体积V为 ,原混合物中NaBr的物质的量为 。
24.(7分) 将1.95 g由Na2SO4和Na2CO3组成的混合物溶于水得溶液A,在A中加入10 mL未知浓度的BaCl2溶液恰好完全反应,过滤得沉淀B和滤液C,在C中加入足量AgNO3溶液,反应后又得沉淀5.74 g,向B中加入足量稀硫酸,沉淀不消失反而增加0.18 g.
计算:(1)BaCl2溶液中溶质的物质的量浓度;
(2)原混合物中Na2CO3的质量分数.(要求写出计算过程)
23.(12分)已知两个羟基同时连在同一碳原子上的结构是不稳定的,它要发生脱水反应:
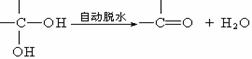
现有分子式为C9H8O2X2(X为一未知元素)的物质M,可在一定条件下发生上述一系列反应
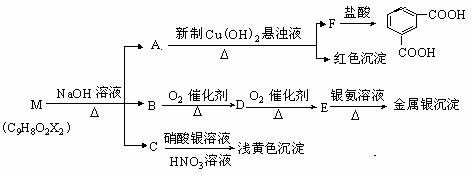
试回答下列问题:
⑴ X为 (填元素符号);
⑵A中所含的官能团为 ,上述转化中其中属于氧化反应的
共有 步(填数字);M与NaOH溶液共热反应的所属类型是 反应。
⑶ M的结构简式为 。
⑷写出下列反应的化学方程:
①B→D ;
②D在一定条件下发生加聚反应: ;
③E和银氨溶液反应的化学方程式: 。
22.(8分)已知X、Y、Z、H四种物质的混合蒸气(假设不反应),四种物质以任意比例混合,所得混合气体在相同条件下对氢气的相对密度为30。四种物质均含碳、氢、氧三种元素。且分子中碳原子数目关系为X>Y=Z=H。已知X和Y在浓硫酸作用下反应生成有支链的果香味物质,X、Z和H均为中性物质,Z分子中含二种官能团,其中一种和X中官能团相同,H中也含Z 中的一种官能团,H分子中有二种不同环境的氢原子。
写出X、Y、Z、H四种物质的结构简式:
X ,Y ,Z ,H 。
21.(8分)I. 叠氮酸钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质。
(1)NaN3中存在的化学键有 (答案可能不止一个,填字母)。
a.离子键 b.极性共价键 c.非极性共价键
(2)3mol NaN3受撞击会生成4mol 氮气和一种离子化合物A,可用于汽车保护气囊。请写出有关反应的化学方程式 ____ 。
Ⅱ.已知X、Y、Z、W是短周期中的四种非金属元素,它们的原子序数依次增大。X元素原
子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
⑴仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子方程式为_ 。
⑵这四种元素可组成原子个数比为5:1:1:3的化合物(按X、Y、Z、W的顺序),该化合物的水溶液与足量的NaOH溶液反应的离子方程式为: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com