
30. (15分)氮是地球上含量丰富的一种元素,氮及其化合拖把在工农业生产、生活中有着重要作用。请回答:
(15分)氮是地球上含量丰富的一种元素,氮及其化合拖把在工农业生产、生活中有着重要作用。请回答:
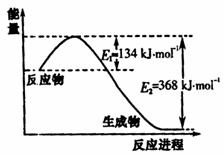
(1)右图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在一定体积的密闭容器中,进行如下化学反应:
 N2(g)+3H2(g) 2NH3(g),其化学平衡常数K与温度t的关系如下表:
N2(g)+3H2(g) 2NH3(g),其化学平衡常数K与温度t的关系如下表:
|
t/K |
298 |
398 |
498 |
… |
|
K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
完成下列问题:
①比较K1、K2的大小;K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保护不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出墁酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])>c(H+)>c(OH-)
C.2c(N2H62+)+c([N2H5·H2O+])+c(H+)=c(H+)+c(OH-)
D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-)>
[选做部分]
29.(12分)a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是子半径最小的元素,b的最高正价与最低负价的代数和为零,a与c、d与c均可形成原子个数比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素。
(1)画出f元素的原子结构示意图 。在a、c、d三种元素形成的化合物中存在的化学键类型是 。
(2)写出d、e两元素的最高价氧化的水化物之间反应的离子方程式 。
(3)写出下列反应的化学方程式(有机物用结构简式表示):
①将化合物a6b6与浓硫酸和浓硝酸的混合液共热并保持(55~60)℃反应 ;
②将a6b2c和氧气的混合气体通过加热的铜网反应 。
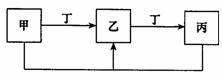 (4)甲、乙、丙、丁四种无机物具有如图所示的转化关系,甲是f的单质,且甲、乙、丙中均含有同一种元素,丁为金属单质,请写出检验乙中阳离子的一种方法:
(4)甲、乙、丙、丁四种无机物具有如图所示的转化关系,甲是f的单质,且甲、乙、丙中均含有同一种元素,丁为金属单质,请写出检验乙中阳离子的一种方法:
。
|
28.(15分)长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过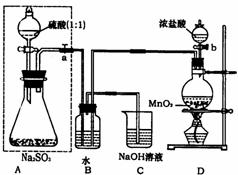 实验来测定苛无小亚硫酸钠试剂的被氧化的程度,设计了右图实验:请回答下面的问题:
实验来测定苛无小亚硫酸钠试剂的被氧化的程度,设计了右图实验:请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏
斗,则应该怎样检查虚线框内装置的
气密性?
。
(2)D装置中反应的化学方程式为 。B装置中反应
的离子方程式为 。
(3)称量ag Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀bg,原样品中Na2SO3的质量分为数为 。
(4)C装置中反应的离子方程式为 。
(5)现有以下试剂:蒸馏水、稀盐酸、稀硝酸、BaCl2溶液、Ba(NO3)2溶液,请从中选择合适试剂,设计一种不同的实验方法测定试样中无水亚硫酸钠被氧化的程度
。
15.近年来,科学家研制了一种新型的乙醇电池,它用酸性电解质(H+)作溶剂。电池总反应为:C2H5OH+3O2=2CO2+3H2O,下列说法不正确的是 ( )
A.乙醇在电池的负极上参加反应
B.1mol CH3CH2OH被氧化转移6mol电子
C.在外电路中电子由负极沿导线流向正极
D.电池正极的电极反应为4H++O2+4e-→2H2O
|
14.下列有关化学用语的叙述正确的是 ( )
 A.硫酸铝水解的化学方程式是:Al2(SO4)3+3H2O 2Al(OH)3+3H2SO4
A.硫酸铝水解的化学方程式是:Al2(SO4)3+3H2O 2Al(OH)3+3H2SO4
B.铜跟浓硝酸反应的离子方程式是:
Cu+4HNO3(浓)=Cu2++2NO3-+2NO2↑+2H2O
C.钢铁发生吸氧腐蚀时,负极发生的电极的反应为:2H2O+O2+4e-→4OH-
D.氢氧化亚铁在空气中久置变成红褐色的化学方程式为:
4Fe(OH)2+O2+2H2O 4Fe(OH)3
13.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂。已知它的结构式为Cl-S-S-Cl,易与水反应:2S2Cl2+2H2O 4HCl+SO2↑+2S↓。对该反应下列说法正确的是 ( )
A.S2Cl2既作氧化剂又作还原剂
B.S2Cl2只作氧化剂
C.每生成1mol SO2转移4mol电子
D.S2Cl2只作还原剂
12.在298K、1.01×105Pa下,将22g CO2通入1mol·L-1 NaOH溶液750mL中充分反应,测得反应放出x kJ的热量。已知该条件下,1mol CO2通入2mol·L-1 NaOH溶液1L中充分反应放出y kJ的热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的 ( )
A.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(2y-x)kJ·mol-1
B.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(2x-y)kJ·mol-1
C.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(4x-y)kJ·mol-1
D.2CO2(g)+2NaOH(aq)=2NaHCO3(aq) △H=-(8x-2y)kJ·mol-1
11.图表资料可以为我们提供很多信息。下面是某学生对图表资料的使用,其中不正确的是
( )
A.根据金属活动顺序表,判断某金属能否置换出稀硫酸中的氢
B.根据熔点数据,判断降低温度时,两种固体物质的混合溶液中哪种物质先析出
C.根据元素周期表,判断同主族两种元素的阳离子在用惰性电极电解其水溶液时,何
者先发生反应
D.根据酸碱盐的溶解性表,判断某些复分解反应能否发生
9.下列观点错误的是 ( )
A.酯化反应属于取代反应
B.根据在不溶液里或熔融状态下能否导电,可将化合物分为强电解质和弱电解质

 C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示溶液平衡,Al(OH)3 Al3++3OH-表
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示溶液平衡,Al(OH)3 Al3++3OH-表
示电离平衡
D.用稀盐酸洗涤AgCl沉淀比用水洗涤,损耗AgCl少
|
A.高温下60g SiO2与足量纯碱反应,最多可释放出2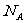 三个气体分子
三个气体分子
B.1mol C5H12分子中共价键总数为13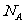
C.78g
Na2O2固体与H2O反应转移的电子数为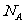
D.标准状况下,2.24L NH3和CH4的混合气体,所含电子总数为2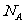
33.(8分)[化学--有机化学基础]
我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任务污染。这一材料是由我国最新研发成功的。PETG的结构简式为:
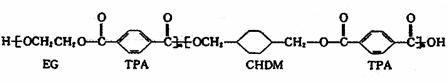
已知:
①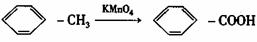
②RCOOR1+R2OH→RCOOR1+R1OH(R、R1、R6表示烃基)
这材料可采用右图合成路线:
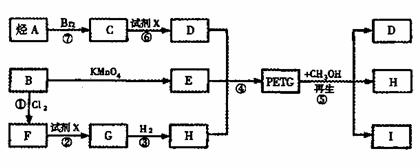
试回答下列问题:
(1)反应②⑥加入的试剂X是 ;
(2)①⑤的反应类型是:① ⑤ 。
(3)写出B、I的结构简式:B 、I 。
(4)合成时应控制的单体的物质的量(用m、n表示)
n(D): n(E):n(H)= 。
(5)写出化学方程式:
反应③ ;反应⑥ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com