
5.可逆反应mA(g)+nB(g)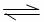 pC(g)+gD(g)的v-t图如下左图,若其它条件都不变,只是在反应前加入合适的催化剂,则其v-t图如下右图。
pC(g)+gD(g)的v-t图如下左图,若其它条件都不变,只是在反应前加入合适的催化剂,则其v-t图如下右图。
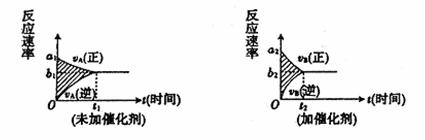
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2
⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等
⑧右图阴影部分面积更大,以上正确的为 ( )
A.②④⑤⑦ B.①④⑥⑧ C.②③⑤⑧ D.①③⑥⑦
4.下列各组物质的分类正确的是 ( )
①混合物:氯水、氨水、水玻璃、水银
②电解质:明矾、冰醋酸、石膏、纯碱
③非极性分子:CO2、CC14、CH2C12、对二甲苯
④同位素:1H+、2H+、3H+
⑤同素异形体:C60、C80、金刚石、石墨
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑦同分异构体:乙二酸二乙酯、乙二酸乙二酯,二乙酸乙二酯
A.②⑤ B.②④⑤⑦ C.②⑤⑥⑦ D.全部正确
3.未做实验而欺骗老师的学生是 ( )
A.老师:我用Na2SO3溶液与BaC12作用,有白色沉淀生成,加入稀HC1后沉淀消失
B.老师:我向Ba(OH)2溶液中通入SO2气体,也有沉淀生成
C.老师:我向BaC12溶液中通入SO2气体,也出现了白色沉淀
D.老师:我向用硝酸酸化过的BaC12溶液中通入SO2气体,也出现了白色沉淀
2.下列对应的甲、乙概念,不能组成一个物质的量的公式是 ( )
|
|
A |
B |
C |
D |
|
甲概念 |
结构微粒数 |
固体密度 |
标况时气体体积 |
溶液的物质的量浓度 |
|
乙概念 |
阿伏加德常数常 |
固体体积 |
气体摩尔体积 |
溶液的体积 |
1.下面是某同学用连线的方式对某一主题知识进行归纳的情况,有错误的一组是( )
A.性质与用途
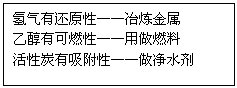
B.安全常识

C.元素与人体健康

D.环保与物质的利用

28.某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
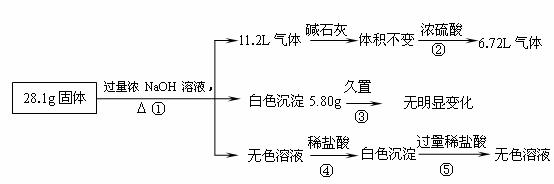
回答下列问题:
(1)混合物中是否存在FeCl2 否__ _ (填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4 是_ __ (填“是”或“否”),你的判断依据是:
气体通过浓酸减少4._____________________________-- 。
(3)写出反应④的离子反应式: AlO-+H++HO ==A l(OH__ 。
(4)请根据计算结果判断混合物中是否含有AlCl3(说出你的计算依据,不要求写计算过程):
27.(12分)如下图所示的装置,C、D、E、F、X、Y都是惰性电极。
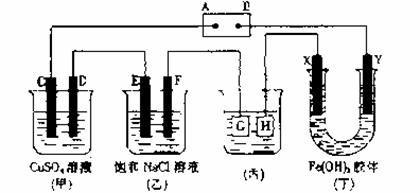
将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
(1)电源A极的名称是___ ____。
(2)甲装置中电解反应的总反应离子方程式是:___________________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是______ ______。
(4)欲用丙装置给铜镀一层银,G应该是_______(填“铜”或“银”),电镀液的主要成分是______ ___(填化学式)。
(5)装置丁中的现象是______________________,说明________ _____ 。
26.(4分)下列实验操作或对实验事实的叙述正确的是_________ __(填序号):
①用碱式滴定管量取20.00 mL 0.10mol/L KMnO4溶液;
②用托盘天平称取10.50 g干燥的NaCl固体;
③各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘纸上称量;
④配制Al2(SO4)3溶液时,加入少量的稀硫酸;
⑤将未经湿润的pH试纸浸到某溶液中,过一会取出与标准比色卡比较测得该溶液的pH;
⑥中和滴定中,锥形瓶用蒸馏水洗净后可直接往其中注入一定量的待测溶液;
⑦测定硫酸铜晶体中结晶水含量的实验至少需要加热2次,至少需要称量4次。
25.下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
B |
C |
D |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
E |
F |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)B和E的最高价氧化物对应的水化物中酸性较强的是 (填化学式),
写出可以验证该结论的一个离子反应方程式 。
(2)王水可溶解不能与硝酸反应的金属如Au、Pt等,其原因是王水中不仅含有HNO3、还有反应生成的Cl2和NOCl,假设NOCl中所有原子都达到了8电子稳定结构,试写出NOCl的电子式 。
(3)EBC-和A2D2在碱性条件下反应生成了ED42-和可参加大气循环的两种无毒无害气体及水,试写出该反应的离子方程式__________________________。
24.(6分)用惰性电极电解NaCl与NaHCO3混合溶液,测得溶液pH变化如下图所示。
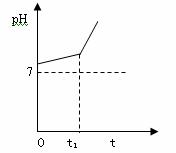
① 在0→t时间内,两个电极上的电极反应式为:
阳极 ;
阴极 。
②用离子方程式表明0→t1时间内,溶液pH升高比较缓慢的原因: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com