
14.向含下列离子的溶液中,加入过量的过氧化钠,振荡、静置、过滤,取沉淀洗涤后加足量盐酸,得到的溶液所含金属阳离子与原溶液相同的是 ( )
A.Na+、Mg2+ B.Fe2+、Cu2+ C.Al3+、Cu2+ D.Mg2+、Fe3+
13.甲、乙、丙、丁分别代有AgNO3、BaCl2、Na2CO3、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙→沉淀;甲+丙→沉淀;乙+丙→沉淀;丙+丁→沉淀;乙+丁→无色无味气体。则甲、乙、丙、丁四种溶液依次是 ( )
A.BaCl2、Na2CO3、盐酸、AgNO3 B.BaCl2、Na2CO3、AgNO3、盐酸
C.Na2CO3、盐酸、AgNO3、BaCl2 D.AgNO3、盐酸、BaCl2、NaCO3
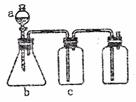
12.用下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂,)其中可行的是 ( )
|
|
气体 |
a |
b |
c |
|
A |
O2 |
双氧水 |
MnO2 |
浓硫酸 |
|
B |
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
|
C |
C2H4 |
浓硫酸 |
乙醇 |
碱石灰 |
|
D |
C2H2 |
水 |
电石 |
CuSO4溶液 |
11.向100mL0.1mol·L-1CH3COOH溶液中加入少量醋酸钠晶体或加等体积水稀释时,都会引起 ( )
A.溶液的pH增大 B.CH3COOH的电离平衡向右移动
C.溶液的导电能力减弱 D.溶液的酸性增强
9.用括号内的物质,不能将下列各组未知物--鉴别出来的是 ( )
A.CaCl2、NaBr、KI、KF(硝酸银溶液)
B.FeCl2、FeCl3、MgCl2、AlCl3(氨水)
C.苯、CCl4、苯酚溶液、苯乙烯(浓溴水)
D.FeO、CaO、FeS、MnO2(浓盐酸)
|
A.除去CO2中混有的少量SO2:将气体通过盛有足量饱和Na2CO3溶液的洗气瓶
B.除去乙醇中混有的少量水:在乙醇中加入新制的生石灰,加热蒸馏
C.除去蛋白质溶液中混有的少量食盐:渗析
D.提取溶解在水中的少量碘:加入CCl4振荡、静止分层后分液,再将有机层分离
8. 25℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是( )
25℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是( )
A.将水加热,KW增大,pH增大
B.向水中加入少量固体碳酸钠,c(H+)增大,KW增大
C.向水中加入少量固体碳酸钠,平衡向正反应方向移动,c(OH-)增大
D.向水中加入稀氨水,平衡向逆反应方向移动,c(OH-)减小
7.下列离子方程式正确的是 ( )
A.将少量SO2气体通入NaClO溶液中:SO2+H2O+ClO-=2H++SO2-4+Cl-
 B.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体
B.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体
Fe3++3H2O Fe(OH)3↓+3H+
C.碘化亚铁溶液中通入过量氯气:Cl2+2Fe2+ = 2Fe3+ + 2Cl-
D.碳酸氢钠溶液中滴入少量澄清石灰水:HCO-3+Ca2++OH- = CaCO3↓+H2O
6.用NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.1mol过氧化氢完全分解转移的电子数为0.2NA
B.200mL 2mol·L-1蔗糖溶液中所含分子数为0.4NA
C.在常温常压下,17g硫化氢所含质子数为8NA
D.在标准状况下,4.48L二氧化硫与氧气的混合气体中所含氧原子数为0.4NA
5.溶质为11.2g的KOH稀溶液与0.11L 1.0mol/L的硫酸溶液反应可放出11.44kJ的热量。下列能表示中和热的热化学方程式为 ( )
A.KOH(aq)+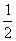 H2SO4(aq)===
H2SO4(aq)===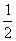 K2SO4(aq)+H2O(l);△H=+57.3kJ/mol
K2SO4(aq)+H2O(l);△H=+57.3kJ/mol
B.2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l);△H=-114.6kJ/mol
C.2KOH(aq)+H2SO4(aq) === K2SO4(aq)+2H2O(l);△H=-57.3kJ/mol
D.KOH(aq)+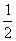 H2SO4(aq)===
H2SO4(aq)===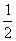 K2SO4(aq)+H2O(l);△H=-57.3kJ/mol
K2SO4(aq)+H2O(l);△H=-57.3kJ/mol
4. 已知:CO(g)+2H2(g) CH3OH(g);△H<0,为了增加甲醇的产量,工业生产采取的正确措施是 ( )
已知:CO(g)+2H2(g) CH3OH(g);△H<0,为了增加甲醇的产量,工业生产采取的正确措施是 ( )
A.高温、高压 B.适当的温度、高压、催化剂
C.低温、低压 D.低温、高压、催化剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com