
9.在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如下图所示,由此确定原溶液中含有的阳离子是
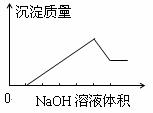
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
8.在下列反应类型中,能体现绿色化学中的“原子经济”原则的是
(1)置换反应;(2)化合反应;(3)分解反应;(4)取代反应;(5)加成反应;(6)复分解反应;(7)酯化反应。
A.(2)(5)(7) B.(1)(2)(3)(4) C.(2)(5) D.(1)(2)(5)(6)
7.下列说法正确的是
A.铜、石墨均导电,所以它们均是电解质
B.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
C.液态HCl、固体NaCl均不导电,所以HCl、NaCl均是非电解质
D.蔗糖、酒精在水溶液或熔融状态下均不导电,所以它们均是非电解质
6.以NA 表示阿伏加德罗常数,下列说法正确的是
A.T℃时,1 L pH=6纯水中,含10–6NA个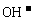
B.15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA
C.1 mol SiO2中含有2 mol Si–O单键
D.如果5.6 L N2含有n个氮分子,则阿伏加德罗常数一定约为4n
5.HF的酸性比HCN的酸性强,现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,前者溶液中的离子总数为n1,后者溶液中的离子总数为n2 ;另有物质的量浓度和体积均相同的Na2A ( pH=10 )和Na2B ( pH=9 ) 两种溶液,前者溶液中的离子总数为n3,后者溶液中的离子总数为n4;下列关系正确的是
A.n1<n2,n3>n4 B.n1<n2,n3<n4 C.n1>n2,n3<n4 D.n1>n2,n3>n4
4.欲配制100 ml 1.0 mol/L Na2SO4溶液,正确的方法是
①将14.2 g Na2SO4 溶于100 ml水中;②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml;③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml。
A.②③ B.①② C.①③ D.①②③
3.下列有关叙述:① 非金属单质M能从N的化合物中置换出非金属单质N;② M原子比N原子容易得到电子;③单质M跟H2反应比N跟H2反应容易得多;④气态氢化物水溶液的酸性HmM>HnN;⑤氧化物水化物的酸性HmMOx>HnNOy;⑥熔点M>N。能说明非金属元素M比N的非金属性强的是
A.②⑤ B.①②③ C.①②③⑤ D.全部
2.合成氨工业中用铁触媒来催化N2和H2合成NH3 。若将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),则该b L气体中的NH3体积分数是
A.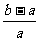 B.
B.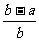 C.
C.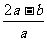 D.
D.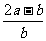
1.将甲和乙气体同时通入过量丙溶液中,可能产生沉淀的组合是
|
序号 |
甲 |
乙 |
丙 |
|
① |
CO2 |
SO2 |
Ca(OH)2 |
|
② |
HCl |
CO2 |
Ca(OH)2 |
|
③ |
CO2 |
SO2 |
Ba(NO3)2 |
|
④ |
NO2 |
SO2 |
CaCl2 |
|
⑤ |
CO2 |
NH3 |
CaCl2 |
|
⑥ |
O2 |
NH3 |
AlCl3 |
A.全部 B.①③④⑤⑥ C.①②③④⑤ D.①③⑤⑥
21.(10分)2.80 g铁与100 mL稀硝酸混合后充分反应,产生气体为NO,反应后铁、硝酸均无剩余。向反应后的溶液中加入100 ml 0.2mol/L的碘化钾溶液,恰好将溶液中的Fe3+全部还原。求原硝酸溶液的物质的量浓度(要求有计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com