
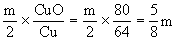

答案:(1)方程式从略。
CuO+CO
 Cu+CO2
Cu+CO2
那么,溶液Y中含FeCl2和CuCl2,粉末Z中含Fe和Cu:
Fe+Cu2+=Fe2++Cu
Fe+2H+=Fe2+H2↑
由于反应后溶液强酸性,且不会有Cu2+说明Z中Fe完全溶解了。不溶物W全部是金属铜,应是两份试样中的CuO转化生成的Cu。则每份试样中CuO的质量为:
FeO+CO  Fe+CO2
Fe+CO2
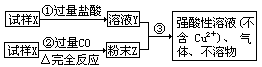
(1)请写出步骤③中所发生的全部反应的离子方程式______。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量为m,则每份试样X中氧化铜的质量为______(用m表示)。
思路引导A:根据试样X在
①和②的反应以确定出溶液Y和粉末Z的成分。
思路引导B:溶液Y和Z发生的反应③,只能是Fe和CuCl2和过量盐酸之间的置换反应,进而引导分析试样中CuO的质量关系。
学生审题,并进行如下的分析:
在反应①中,会发生如下反应:
FeO+2HCl=FeCl2+H2O
CuO+2HCl=CuCl2+H2O
在反应②中,会发生的反应有:
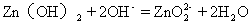


规律:只有两性氢氧化物才能与强碱溶液反应。
(4)与氨水作用
AgOH+2NH3?H2O=Ag(NH3)2OH+2H2O
*Cu(OH)2+4NH3?H2O=Cu(NH3)4(OH)2+4H2O
* Zn(OH)2+4NH3?H2O=Zn(NH3)4(OH)2+4H2O
规律:易形成氨络合物的金属氢氧化物能与氨水反应。
(5)与氧化剂反应
4Fe(OH)2+O2+2H2O=4Fe(OH)3
规律:低价金属氧化物具有还原性。
【小结】金属氢氧化物所发生的反应,总结起来,主要有:
①热稳定性
②酸性(H+)
③碱性(OH-)
④络合剂
⑤还原性
【投影】右图试样X由氧化亚铁和氧化铜组成,取质量相等的两
份试样如右图所示进行实验:试回答在题右的两个问题。
(指导学生读题、审题并形成解题的思路)。
2Fe(OH)3  Fe2O3+3H2O
Fe2O3+3H2O
规律:①金属活动顺序“Mg”以前的金属氢氧化物稳定性好,难分解。
②“AgOH”常温下易分解。
③“Mg―Hg”的氢氧化物常温下难分解,受热或灼烧易分解。
(2)与强酸(H+)的反应
Mg(OH)2+2H+=Mg2++2H2O
Al(OH)3+3H+=Al3++3H2O
(3)与强碱(OH-)反应
Al(OH)3+OH-=AlO2-+2H2O
Cu(OH)2  CuO+H2O
CuO+H2O
2AgOH
 Ag2O+H2O
Ag2O+H2O
其它的都是难溶性的,如Mg(OH)2、Fe(OH)3、Cu(OH)2
【提问】请同学分析总结这些氢氧化物的化学性质规律是什么。
可从下面几点去思考,回答。
(1)加热是否分解
(2)与强酸(H+)反应
(3)与强碱(OH-)反应
(4)与氨水反应
(5)是否容易被氧化
(6)是否能被还原
(指导学生分析,回答)
学生讨论,分析,整理笔记。
(1)热稳定性
Zn(OH)2、Fe(OH)2、AgOH
红褐色:Fe(OH)3
蓝色:Cu(OH)2
【提问】这些金属氢氧化物对水的溶解性规律是什么?请总结之。
(指导学生分析、回答)
ⅠA和部分ⅡA金属氢氧化物都易溶于水,如NaOH,KOH,Ba(OH)2。Ca(OH)2是微溶性的。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com