
A.70% B.30% C.47.6% D.52.4%
例2.有一块Al-Fe合金,溶于足量的盐酸中,再用过量的NaOH溶液处理,将产生的沉淀过滤、洗涤、干燥、灼烧完全变成红色粉末后,经称量,红色粉末的质量恰好与合金的质量相等,则合金中铝的质量分数为 ( )
若要由反应方程式分别求出镁、铝的物质的量,繁而难解,可运用“终态法”,沉淀为最大量时,即镁、铝全部以=Mg(OH)2 、Al(OH)3存在,而此时溶液中只存在NaCl,则根据原子守恒,有:n(NaOH)=n(HCl)=0.5L×4mol?L?1=2mol,V(NaOH)=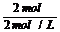 =1L=1000mL,选C。
=1L=1000mL,选C。
例1.有镁、铝的混合粉末10.2g,将它溶于500mL,4mol?L?1的盐酸中,若要得到沉淀量为最大值,则需加入2mol?L?1的NaOH溶液的体积为 ( )
A.300mL B.500mL C.1000mL D.1500mL
[解析]:有关反应为:Mg+2HCl = MgCl2+H2↑ 2Al+6HCl = 2AlCl3+3H2↑
HCl+NaOH=NaCl +H2O(可能) MgCl2+2NaOH =Mg(OH)2↓ +2NaCl
AlCl3+3NaOH = Al(OH)3↓+3NaCl
(3)

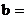

四川省南充市08-09学年高二教学质量监测
D.断裂 氮氮三键同时断裂
氮氮三键同时断裂 氮氢键
氮氢键
(1)容器甲 内用
内用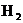 表示的平均反应速率
表示的平均反应速率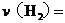
 。
。
(2)下列哪些情况表明容器乙已达到平衡状态 。
A.容器乙的气体密度不再变化
B.氢元素的质量不再变化
C.氮气的生成速率等于氨气的消耗速率
 已知甲乙达到平衡时,温度、压强以及相同组分的体积分数均相同。
已知甲乙达到平衡时,温度、压强以及相同组分的体积分数均相同。
Ⅱ.容器乙起始投入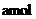
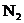 ,
,
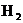 ,维持恒温恒压到平衡,测得平衡时
,维持恒温恒压到平衡,测得平衡时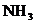 的物质的量为
的物质的量为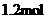 ;
;
 I.体积为
I.体积为
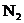 ,
,
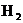 ,经过
,经过 达到平衡,测得平衡时
达到平衡,测得平衡时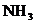 的物质的量为
的物质的量为 ;
;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com