
12ЃЎвбжЊXЁЂYЪЧжїзхдЊЫиЃЌIЮЊЕчРыФмЃЌЕЅЮЛЪЧKJЃЏmolЁЃИљОнЯТБэЫљСаЪ§ОнХаЖЯДэЮѓЕФ
ЁЁ ЪЧ
|
дЊЫи |
I1 |
I2 |
I3 |
I4 |
|
X |
500 |
4 600 |
6 900 |
9 500 |
|
Y |
580 |
l 800 |
2 700 |
11 600 |
ЁЁЁЁ AЃЎдЊЫиXЕФГЃМћЛЏКЯМлЪЧ+lМл
ЁЁЁЁ BЃЎдЊЫиYЪЧЂѓAзхЕФдЊЫи
ЁЁЁЁ CЃЎдЊЫиXгыТШаЮГЩЛЏКЯЮяЪБЃЌЛЏбЇЪНПЩФмЪЧXCl
ЁЁЁЁ DЃЎШєдЊЫиYДІгкЕк3жмЦкЃЌЫќПЩгыРфЫЎОчСвЗДгІ
11ЃЎШ§ТШЛЏЕЊ(NCl3)ГЃЮТЪЧвЛжжЕЛЦЩЋвКЬхЃЌЦфЗжзгНсЙЙГЪШ§НЧзЖаЮЃЌвдЯТЙигкNCl3ЕФЫЕЗЈжае§ШЗЕФЪЧЃК
ЁЁЁЁ AЃЎЫќЪЧвЛжжЗЧМЋадЗжзг
ЁЁЁЁ BЃЎЫќФмвдХфЮЛМќгыC1-НсКЯЃЌЩњГЩNCl4вЛ
ЁЁЁЁ CЃЎЦфЛгЗЂадБШPCl3аЁ ЁЁ
ЁЁЁЁ DЃЎвбжЊNCl3жаNдЊЫиЮЊвЛ3МлЃЌЫљвдNCl3ЫЎНтВњЮяЮЊNH3КЭHClO
10ЃЎ1999Фъ1дТЃЌЖэУРПЦбЇМвСЊКЯаЁзщаћВМКЯГЩГі114КХдЊЫиЕФвЛжжЭЌЮЛЫиЃЌИУЭЌЮЛЫидзгЕФжЪСПЪ§ЮЊ298ЁЃвдЯТа№ЪіВЛе§ШЗЕФЪЧ
ЁЁЁЁ AЃЎИУдЊЫиЪєгкЕкЦпжмЦкЁЁ ЁЁ
ЁЁЁЁ BЃЎИУдЊЫиЮЛгкЂѓAзх
ЁЁЁЁ CЃЎИУдЊЫиЮЊН№ЪєдЊЫиЃЌаджЪгы82PbЯрЫЦ
ЁЁЁЁ DЃЎИУЭЌЮЛЫидзгКЌга114ИіЕчзгЃЌ184ИіжазгЁЁ ЁЁ
9ЃЎNH3ЁЂH2SЕШЪЧМЋадЗжзгЃЌC02ЁЂBF3ЁЂCCl4ЕШЪЧКЌМЋадМќЕФЗЧМЋадЗжзгЁЃИљОнЩЯЪіЪЕР§ПЩЭЦГіABnаЭЗжзгЪЧЗЧМЋадЗжзгЕФОбщЙцТЩЪЧ
ЁЁЁЁ AЃЎЗжзгжаВЛФмКЌгаЧтдзг
ЁЁЁЁ BЃЎдкABnЗжзгжаAЕФЯрЖддзгжЪзюгІаЁгкBЕФЯрЖддзгжЪСП
ЁЁЁЁ CЃЎдкABnЗжзгНкAдзгУЛгаЙТЖдЕчзг
ЁЁЁЁ DЃЎЗжзгжаУПИіЙВМлМќЕФМќГЄгІЯрЕШЁЁ ЁЁ
8ЃЎРћгУЕчИКадЪ§жЕПЩвддЄВт
ЁЁЁЁ AЃЎЗжзгЕФМЋадЁЁЁЁ BЃЎЗжзгЕФЖдГЦадЁЁЁЁ CЃЎЛЏбЇМќЕФМЋадЁЁЁЁ DЃЎЗжзгЕФПеЮЪЙЙаЭ
7ЃЎЙЬЬхБљжаВЛДцдкЕФзїгУСІЪЧ ЁЁ
ЁЁЁЁ AЃЎРызгМќ ЁЁЁЁBЃЎМЋадМќЁЁЁЁ ЁЁCЃЎЧтМќЁЁЁЁ ЁЁDЃЎЗЖЕТЛЊСІ
6ЃЎЯТСаЙ§ГЬжаЃЌЙВМлМќБЛЦЦЛЕЕФЪЧ
ЁЁЁЁ AЃЎЕтЩ§ЛЊЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЃЎфхеєЦћБЛФОЬПЮќИН
ЁЁЁЁ CЃЎNaClШмгкЫЎЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁDЃЎHClЦјЬхШмгкЫЎ
5ЃЎЯТСаИїзщдЊЫиАДЕчИКадгЩДѓЕНаЁХХСае§ШЗЕФЪЧ
ЁЁ ЁЁAЃЎCl>S>As ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЃЎO>Cl>F
CЃЎAs>P>HЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁDЃЎF>N>OЁЁ ЁЁ
4ЃЎЯТСаЙьЕРБэЪОЪНЫљБэЪОЕФдЊЫидзгжаЃЌЦфФмСПДІгкзюЕЭзДЬЌЕФЪЧ
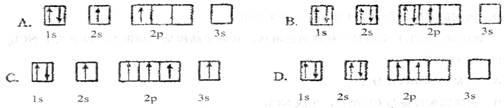
3ЃЎвдЯТФмМЖЗћКХВЛе§ШЗЕФЪЧ
ЁЁЁЁ AЃЎ5SЁЁ ЁЁBЃЎ3fЁЁ ЁЁCЃЎ6p ЁЁЁЁЁЁDЃЎ 4d
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com