
21.(5分)某同学想通过比较两种最高价氧化物对应水化物的酸性强弱来验证硫与碳的非金属性的强弱,他采用了如图所示的装置。请回答:
(1)仪器a的名称是 ,应盛放下列药品中的 。
A.稀硫酸 B.亚硫酸
C.氢硫酸 D.盐酸
(2)仪器b的名称是 ,应盛放下列药品中的 。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)如果观察到C中的现象为 ,
即可证明硫与碳的非金属性的强 弱。
弱。
20.难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:
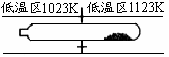


 TaS2 (s)+2I2 (g)
TaI4 (g)+S2 (g) ;△H
TaS2 (s)+2I2 (g)
TaI4 (g)+S2 (g) ;△H
下列说法正确的是
A.在不同温度区域,TaI4 的量保持不变
B. 利用上述原理提纯TaS2需要消耗大量的I2
C.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区
D.在1023-1123K范围內,该反应的△H<0
非选择题(共50分)
19.某同学按右图所示的装置进行试验。A、B 为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析错误的是
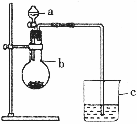
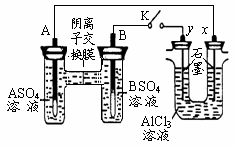 A.金属活动性A强于B
A.金属活动性A强于B
B.B 的电极反应: B-2e一= B2+
C.x电极上有 H2 产生,发生还原反应
D.反应初期, x 电极周围出现白色沉淀,
不久沉淀溶解
18.X、Y、Z、W四种元素的质子数之和是35,X、Y是相邻周期的同主族元素,Z、W 是相同周期的非金属元素,化合物ZW的相对分子质量是30,化合物YX的式量是40,则下列说法不正确的是
是相同周期的非金属元素,化合物ZW的相对分子质量是30,化合物YX的式量是40,则下列说法不正确的是
A.X的最简单氢化物的稳定性比Y的强
B.X的最高价氧化物的水化物的酸性比Z的强
C.ZW是一种气体,不用排空气法收集,原因是ZW在空气中易被氧化
D.YX构成的物质是一种硬度很高的新型材料
17.如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
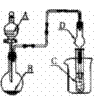 A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B.若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊
C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生
白色沉淀后沉淀又溶解
D.实验仪器D对防止溶液倒吸无作用
16.某化学科研小组研究在其他条件不变时,改变其一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量):
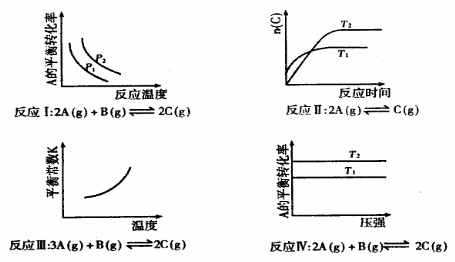
根据以上规律判断,下列结论正确的是 ( )
A.反应Ⅰ:△H>0,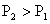 B.反应Ⅱ:△H>0,
B.反应Ⅱ:△H>0,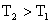 [
[
C.反应Ⅲ:△H>0
D.反应Ⅳ:△H<0,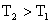
15.在稀硫酸中加入铜粉,铜粉不溶,再加入下列物质 ①FeCl3 ②Fe2O3 ③Cu(NO3)2 ④KNO3, 铜粉溶解的是
A.只有①或② B. 只有②或④
C.只有①或②或③ D. 上述四种物质中任意一种
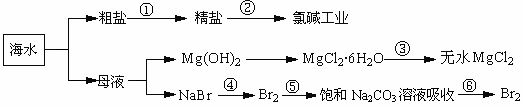
14.如下图所示,利用海洋可提取很多重要的化工原料。
 下列有关说法
下列有关说法 正确的是
正确的是
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸。
B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置
C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解 制无水MgCl2。
制无水MgCl2。
D.在第④步中溴元素被氧化,第⑤⑥步中既有溴元素被氧化也有溴元素被还原。
13.下列离子或化学方程式与所述事实相符且正确的是
A.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
 B.用K37ClO3 与浓盐酸反应制氯气: K37ClO3 + 6HCl (浓) K37Cl
+ 3Cl2↑+ 3H2O
B.用K37ClO3 与浓盐酸反应制氯气: K37ClO3 + 6HCl (浓) K37Cl
+ 3Cl2↑+ 3H2O
C.向硅酸钠溶液中通入少量的CO2: SiO32- + 2CO2 + 2H2O =H2SiO3↓+ 2HCO3-
D.向AlCl3溶液中滴加过量的氨水:Al3++4OH-=AlO2-+ 2H2O
12. 向含有1mol的FeCl2溶液中通入0.2molCl2,再加入含0.1molX2O72-的酸性溶液,使溶液中Fe2+全部恰好氧化,并使X2O72-还原为 Xn+,则n值为(
Xn+,则n值为( )
)
A、2 B、3 C、4 D、5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com