
3.(1)不可能 (2)有 O2 (3)没有
19.常温下,两种常见无色无味的气体A和B组成的混合气体(A的相对分子质量小于B的相对分子质量)。经分析混合气体中总共只含氧和碳两种元素,但不论A和B以何种比例混合,氧和碳的质量比总是大于4/3。
(1)在下表中填写A和B可能的分子式(不一定填满)。
|
|
(1) |
(2) |
(3) |
(4) |
|
A的分子式 |
|
|
|
|
|
B的分子式 |
|
|
|
|
(2)当氧和碳的质量比等于2时,试确定A和B的可能组成以及A与B的物质的量之比___________________________________。
第40讲
典例解析
[例1]根据同主族元素原子结构和性质的递变规律可知,114号元素最外层有4个电
子,其常见化合价有+2、+4 ;由于它在铅的下方,则其金属性>铅>铜。故本题答案选B、D。
[例2]稳定性: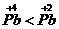 ,
,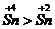 ;氧化性:
;氧化性: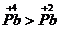 ,
,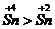 ,
,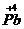 (PbO2)>Cl2>
(PbO2)>Cl2>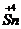 ;还原性:Fe2+<Sn2+
。根据氧化还原反应规律可写出有关反应方程式。
;还原性:Fe2+<Sn2+
。根据氧化还原反应规律可写出有关反应方程式。
△ △
本题答案:(1)还原性;氧化性。 (2)①Sn + 2Cl2 = SnCl4 ;②Pb + Cl2 = PbCl2 ;
△
③PbO2 + 4HCl = PbCl2 + Cl2↑ + 2H2O ;④PbO2 + H2SO3 = PbSO4↓ + H2O
当堂反馈:1.AC 2.CD
18.(200年全国春季,32)第Ⅳ主族元素R,在它的化合物R(OH)n中,其质量分数为0.778,在它的另一种化合物R(OH)m中,其质量分数为0.636。
(1)试求n和m的值:n= ,m= ;
(2)试求R的相对原子质量a:a= 。
17.Fe3O4若看作“混合氧化物”时可以写成FeO 。Fe2O3 ,若看作一种盐时又可写成
Fe (FeO2)2 。根据化合价规则和这种书写方法,Pb3O4可以分别写成______和_______。等物质的量的Fe3O4和Pb3O4分别和浓盐酸反应量,所消耗的HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气。试写出Fe3O4和Pb3O4分别和浓盐酸反应的化学方程式:____________________________、___________________________________。
16.锗(Ge)可以从燃烧的烟道灰中提取,其过程如下,试写出①、②、③、④各步反应的化学方程式。





烟道灰中所含的 锗的 锗 纯净的锗



 锗的高价氧化物 盐酸 氯化物 水解 酸 分解 的氧化物 氢气 锗
锗的高价氧化物 盐酸 氯化物 水解 酸 分解 的氧化物 氢气 锗
① ② △③ △④
①________________________________,②_____________________________;
③________________________________,④_____________________________。
15.我国古代炼丹中经常使用到红丹,俗称铅丹。在一定条件下,铅丹(用X表示)与硝酸能发生如下反应:X+4HNO3 = PbO2+2Pb (NO3)2+2H2O 。
(1)铅丹的化学式为___________,此铅丹中铅的化合价为______。
(2)由此反应可推测PbO是_______性氧化物,PbO2是_______性氧化物。
14.铅的氧化物较多,其中Pb3O4是铅的最高价氧化物和最低价氧化物形成的复杂氧化物,
在Pb3O4中铅的最高价氧化物与最低价氧化物的物质的量之比为
A.1:1 B.1:2 C.2:1 D.无法确定
13.将4.14 g Pb充分氧化,得到氧化物的质量为4.46 g ,则生成的氧化物的化学式为
A.PbO2 B.Pb3O4 C.PbO D.Pb2O5
12.根据碳族元素的相似性能和递变性、一般性和特殊性的知识,判断下列说法中正确的是
A. CO2为弱氧化剂而PbO2为强氧化剂
B.CO2和PbO2都是弱氧化剂,CO和PbO都是还原剂
C.Sn (OH)4可与NaOH反应但不与盐酸反应
D. Ge单质的熔点介于Si与Pb之间,是半导体材料
11.大多数碳的化合物都是共价化合物,其原因是
A.碳原子最外层电子数为4 B.碳元素是非金属元素
C.碳有多种同素异形体 D.碳元素有三种同位素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com