
(五)、电解质溶液的导电性问题
1. 导电的原因:溶液中有自由移动的离子
2. 导电性强弱:取决于溶液中自由移动离子的浓度。与电解质的强弱和溶解度皆无关。
(四)、电离方程式的书写
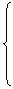 ①强用“=”,弱用“
”
①强用“=”,弱用“
”
②多元弱酸分步写,多元弱碱一步写
③强酸酸式盐(NaHSO4)完全电离(产生H+),弱酸酸式盐完全电离产生两种离子。
④复盐完全电离出多种离子
⑤注意配平(电荷守恒和质量守恒)
常见的强电解质和弱电解质
强电解质:强酸、强碱和大部分盐,如:
弱电解质:HF、HClO、H2CO3、H2SO3、H2S、H3PO4、NH3·H2O、CH3COOH、 Fe(OH)3、Cu(OH)2、Al(OH)3、Pb(Ac)2等。
[练习]1、写出下列物质的电离方程式
H2SO4 ,Ca(OH)2
CaCO3 ,NaHSO4
HF ,HClO
H2S ,H2SO3
H3PO4 ,NaHCO3
NH3·H2O ,Al(OH)3
[练习]2、下列物质中哪些是电解质?哪些是非电解质?
明矾,NO2,Cl2,Fe,乙醇,HF,HClO4,NH4NO3,NaHCO3,Al(OH)3,NH3·CO2,Al2O3,AgCl,BaSO4,氯水。
[练习]3、下列叙述是否正确?为什么?
(1)无水硫酸铜不导电,而胆矾中含结晶水,所以胆矾可以导电。
(2)强电解质由于完全电离,溶液的导电性一定强。
[练习]4、下列说法是否正确?
1. 强电解质的导电能力一定强?弱电解质的导电能力一定弱?
2. 溶解度小的物质导电能力一定弱,溶解度大的物质导电能力一定强?
(三)、强弱电解质
1、强电解质:
2、弱电解质:
3、各类化合物的电离情况:
(1)离子化合物:
(2)共价化合物:
[结论]强酸、强碱和大部分盐是完全电离的,属于强电解质。
(二)、电解质和非电解质
1、电解质:
2、非电解质:
注意:(1)描述的对象:
(2)条件:
(3)化合物本身电离
(一)、什么是电离?
举例:
5、 简单电离方程式的书写;
教学重点。难点:离子方程式的书写,离子共存;
教学过程
4、 离子方程式的书写,离子反应发生的条件;
3、 理解电解质、非电解质的概念,简单判断离子共存问题;
4、日常生活中应用(净水原理)
教学目标
3、土壤化学应用;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com