
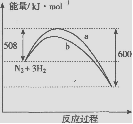
12.右图是298K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
A.该反应的热化学方程式为:N2+3H2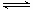 2NH3
△H=-92kJ/mol
2NH3
△H=-92kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热增大
D.在温度体积一定的条件下,通入1mol N2和3 mol H2反应后放出的 热量为Q1kJ,若通入2 mol N2和6mol H2反应后放出的热量为Q2kJ,则184>Q2>2Q1
11.有关热化学方程式的书写与对应表述均正确的是:
A.密闭容器中,1molSO2与0.5mol O2混合加热生成0.5mol SO3时,放出19.12
kJ热量。则O2(g)+2SO2(g)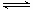 2SO3(g) ; △H= -76.48KJ
2SO3(g) ; △H= -76.48KJ
B.在101 kPa时,2g H2完全燃烧生成液态水,放出285.8
kJ热量,则电解水的热化学方程式表示为2H2O(l)=2H2(g)+O2(g);ΔH=571.6 kJ/mol
C.在稀溶液中:H+(aq)+OH-(aq)= H2O(l);ΔH=-57.3 kJ/mol。若将含0.5mol H2SO4的溶液与含1 mol
NaOH的溶液混合,放出的热量大于57.3
kJ
 D.已知2C(s)+O2(g)=2CO(g); △H= -221 kJ/mol,则可知C的燃烧热为110.5 kJ/mol
D.已知2C(s)+O2(g)=2CO(g); △H= -221 kJ/mol,则可知C的燃烧热为110.5 kJ/mol
10.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:
Cd + 2NiOOH + 2H2O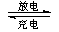 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是:
A.放电时负极附近溶液的碱性不变
B.充电过程中Cd被氧化
C.充电时阳极反应:Ni(OH)2-e-+OH-== NiOOH + H2O
D.放电时电解质溶液中的OH-向正极移动
9.下列离子方程式正确的是:
A.硫酸亚铁在空气中氧化:4Fe2++3O2+6H2O=4Fe(OH)3
B.向次氯酸钠溶液中通入少量SO2:4ClO-+SO2+H2O=
2Cl-+2HClO+SO42-
C.向Na2SO3、NaI的混合溶液中滴加少量氯水:2I-+C12==2Cl-+I2

D.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:
2AlO2-+5H+ =Al(OH)3↓+Al3++H2O
8.下列各组离子在指定条件下一定能够大量共存的是:
A.含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+
B.由水电离出的c ( H十)=
l×l0-12 mol / L 的溶液中: K+、Na+、Cl一、SO32-
C.能使 pH 试纸变深蓝色的溶液中: S2一、AlO2-、S2O32-、Na +
D.遇Al能放出H2的溶液:NO3-、K+、Ca2+、Cl-
7.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:
3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
则关于该反应的说法:①氧化剂是H3AsO3;②还原性:Cl->As;③每生成1molAs,反应中转移电子的物质的量为3mol;④M为OH-;⑤ SnCl62-是氧化产物。正确的是:
A.①③⑤
B.①②④⑤ C.①②③④ D.只有①③
6.下列有关物质性质、结构的表述均正确,且存在因果关系的是:
|
|
表述Ⅰ |
表述Ⅱ |
|
A |
在水中,NaCl的溶解度比I2的溶解度大 |
NaCl晶体中C1-与Na+间的作用力大于碘晶体中分子间的作用力 |
|
B |
通常条件下,CH4分子比SiH4分子稳定性高 |
Si的原子半径比C的大,Si与H之间的键能比C与H间的小 |
|
C |
在形成化合物时,同一主族元素的化合价都相同 |
同一主族元素原子的最外层电子数相同 |
|
D |
乙醇、C6H12O6溶于水后均不导电 |
乙醇、C6H12O6均属于共价化合物 |
5.NA代表阿伏加德罗常数的值,以下说法正确的是:
A.32gCu将浓、稀硝酸分别氧化为NO2和NO,浓、稀硝酸得到的电子数均为NA
B.将1mol MnO2固体与含4mol HCl的浓盐酸共热产生的气体体积在标准状况下为22.4L
C.将1.4mol金属钠和5.4g金属铝同时投入到足量水中产生的气体所含原子数目为2NA
D.物质的量浓度均为1mol/L的NaCl和MgCl2混合溶液中,含有Cl-的数目为3NA
4.
 某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为140.0,原子核外的电子数为58。则下列叙述中错误的是:
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为140.0,原子核外的电子数为58。则下列叙述中错误的是:

 A.它是副族元素
B.它是第六周期元素
A.它是副族元素
B.它是第六周期元素

 C.它的原子核内有58个质子
D.它的一种同位素的核内有82个中子
C.它的原子核内有58个质子
D.它的一种同位素的核内有82个中子
3.等物质的量浓度的下列溶液混合后,所得溶液呈中性的是:
A.20mL NH3·H2O与20mL H2SO4 B.10mL Ca(HCO3)2与10mL NaOH
C.20mL NaHCO3与10mL Ca(OH)2 D.20mL NaHSO4与10mL Ba(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com