
15.对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸。
对于下列物质不能确认其在溶液中是否存在的是 ( )
A. Br- B. SO42- C. H2SO3 D. NH4+
13.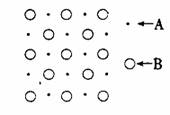 某物质的晶体内部一个截面上原子的排布情况如右图
某物质的晶体内部一个截面上原子的排布情况如右图
所示,则该晶体的化学式可表示为 ( )
A.A2B B.AB
C.AB2 D.A3B
 14.如图是元素周期表前六周期的一部分,关于元素X、Y、Z
14.如图是元素周期表前六周期的一部分,关于元素X、Y、Z
的叙述正确的是 ( )
①X的气态氢化物与Y最高价氧化物对应的水化
物能发生反应生成盐
②X、Y、Z的气态氢化物的水溶液的酸性X<Y<Z
③Z的单质常温下的是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素 A.只有③ B.只有①④ C.只有①②③④ D.①②③④⑤
12.六氧化四磷的分子结构中只含有单键,且每个原子的最外层都满足8电子结构,则该分
子中含有的共价键的数目是 ( )
A.10 B.12 C.24 D.28
11.下列几种情况都有白色沉淀物质生成,其中生成物的化学成分相同的是 ( )
(1)块状纯碱久置于空气中生成的白色粉末
(2)盛澄清石灰水的烧杯内壁附着的白色物质
(3)生石灰久置于空气中生成的白色物质
(4)Na2SiO3水溶液置于敞口容器中,溶液中出现的白色浑浊
A.(1)、(4) B.(2)、(3) C.(1)、(2) D.(3)、(4)
10.几种短周期元素的主要化合价及原子的原子半径数据见下表: (
|
元素代号 |
L |
M |
Q |
R |
T |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+7、-1 |
-2 |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.099 |
0.074 |
据表中信息判断,下列有关叙述中,正确的是 ( )
A.L、M的单质分别与同浓度的稀盐酸反应时,M的单质反应更剧烈 B.M与T形成的化合物能和强酸、强碱反应
C.Q、T两元素的氢化物热稳定性比较:Q的氢化物大于T的氢化物 D.L与R两元素形成的化合物中,含有共价键
9.下列有关化学键与晶体结构说法正确的是 ( )
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
8.镁橄榄石(2MgO·SiO2)中阴离子是 ( )
A. SiO32- B. SiO64- C. SiO44- D. SiO54-
7.要除去混在二氧化碳气体中的HCl、H2O、SO2等气体,混合气体依次通过的试剂是( )
A.碳酸钠溶液、浓硫酸、品红溶液 B.品红溶液、碳酸钠溶液、浓硫酸
C.饱和小苏打溶液、无水氯化钙 D.酸性高锰酸钾溶液、碱石灰
6.有甲、乙、丙三瓶等体积、等物质的量浓度的硫酸,若将甲用水稀释,在乙中加入少量BaCl2溶液,丙不变,然后分别与等浓度的NaOH溶液混合,至完全反应时,所消耗的NaOH溶液的体积是 ( )
A.甲=丙>乙 B.丙>乙>甲
C.乙>丙>甲 D.甲=丙=乙
5. 将SO2气体逐渐通入某溶液,溶液pH随通入的SO2气体
将SO2气体逐渐通入某溶液,溶液pH随通入的SO2气体
体积的变化如右图所示:该溶液可能是 ( )
A.氨水 B.氯水
C.石灰水 D.食盐水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com