
选择题是现代各种形式的考试中最为常用的一种题型.在高考物理试卷中选择题分数占试卷总分的32%.所以,选择题得分的高低直接影响着考试成绩.
从高考命题的趋势来看,选择题主要考查对物理概念、物理现象、物理过程和物理规律的认识、判断、辨析、理解和应用等,选择题中的计算量有逐年下降的趋势.
(二)比较:
1、同一反应生成物状态不同时:A(g)+B(g)=C(g) △H1<0;A(g)+B(g)=C(l) △H2<0。因为C(g)=C(l) △H3<0,则△H3=△H2-△H1,所以△H2<△H1。
2、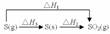 同一反应反应物状态不同时:S(g)+O2(g)=SO2(g) △H1<0;S(s)+O2(g)=SO2(g) △H2<0。
,△H2+△H3=△H1,△H3=△H1-△H2,又因为△H3<0,所以△H1<△H2。
同一反应反应物状态不同时:S(g)+O2(g)=SO2(g) △H1<0;S(s)+O2(g)=SO2(g) △H2<0。
,△H2+△H3=△H1,△H3=△H1-△H2,又因为△H3<0,所以△H1<△H2。
3、两个有联系的不同反应相比:C(s)+O2(g)=CO2(g) △H1<0,C(s)+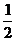 O2(g)=CO(g) △H2<0。C(s)
O2(g)=CO(g) △H2<0。C(s)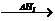 CO2(g),C(s)
CO2(g),C(s)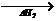 CO(g)
CO(g)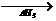 CO2(g),△H2+△H3=△H1。已知△H3<0,所以△H2>△H1。
CO2(g),△H2+△H3=△H1。已知△H3<0,所以△H2>△H1。
[基础训练]
1、在测定中和反应反应热的实验中,下列叙述错误的是( D )
A、向量热计中加入盐酸,搅拌后的温度为初始温度
B、实验中可使酸或碱略过量
C、向量热计中加入碱液时,碱液的温度应与酸的温度相同
D、可以用KOH代替NaOH,浓硫酸代替盐酸
2、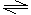 已知298K时,2SO2(g)+O2(g) 2SO3(g) △H=-197kJ·mol-1,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出的热量Q1,向另一体积相同的密闭容器中通入1molSO2和1molO2,达到平衡时放出热量Q2,则下列关系正确的是( C )
已知298K时,2SO2(g)+O2(g) 2SO3(g) △H=-197kJ·mol-1,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出的热量Q1,向另一体积相同的密闭容器中通入1molSO2和1molO2,达到平衡时放出热量Q2,则下列关系正确的是( C )
A、2Q2=Q1 B、2Q2<Q1 C、Q2<Q1<197kJ D、Q2=Q1<197kJ
3、已知298K时,2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1,
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2200kJ·mol-1。设有H2和C3H8的混合气体5mol,完全燃烧时共放出热量3847kJ,则混合气体中H2与C3H8的体积比是( B )
A、1︰3 B、3︰1 C、1︰4 D、1︰1
[高考模拟]
4、(2007海南高考)已知:(1)Zn(s)+1/2O2(g)=ZnO(s),△H=-348.3kJ·mol-1,
(2)2Ag(s)+1/2 O2(g)=Ag2O(s),△H=-31.0kJ·mol-1。
则Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s)的△H等于( A )
A、-317.3kJ·mol-1 B、-379.3kJ·mol-1 C、-332.8kJ·mol-1 D、317.3kJ·mol-1
5、(2008宁夏理综13)已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、
-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( A )
A、-44.2kJ·mol-1 B、+44.2kJ·mol-1 C、-330kJ·mol-1 D、+330kJ·mol-1
(一)计算:
1、用键能数据进行计算:这种计算方法的依据是:反应热等于破坏旧化学键吸收的能量与新化学键所放出的能量之差。△H=E(反应物的总键能)-E(生成物的总键能)。
2、利用盖斯定律进行计算:这是最常见也是考查最多的计算方式。其方法为:若一个化学方程式可由另外几个化学方程式相加减而得到,则该化学反应的焓变即为相关化学反应的焓变的代数和。
(一)内容:一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。
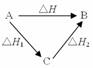 (二)图示:如图:由A到B可设计两个途径:途径一:A→B;途径二:A→C→B。则焓变△H、△H1、△H2的关系可以表示为:△H=△H1+△H2。
(二)图示:如图:由A到B可设计两个途径:途径一:A→B;途径二:A→C→B。则焓变△H、△H1、△H2的关系可以表示为:△H=△H1+△H2。
(四)能源的充分利用
1、化石燃料主要包括:煤、石油、天然气等。
2、可燃物燃烧的条件:与氧气接触、温度达到着火点。
3、燃料不充分燃烧的危害:产热少,浪费资源,污染环境。
(三)燃烧热
1、概念:在101kPa下,1mol物质完全燃烧的反应热。
2、热值:在101kPa下,1g物质完全燃烧的反应热。
3、完全燃烧:指物质中含有的氮元素转化为N2(g),氢元素转化为H2O(l),碳元素转化为CO2(g)。
(二)吸热反应和放热反应
|
|
吸热反应 |
放热反应 |
|
概念 |
吸收热量的反应 |
放出热量的反应 |
|
反应物与生成物能量关系 |
反应物的总能量比生成物的总能量要小 |
反应物的总能量比生成物的总能量要大 |
|
表示方法 |
△H>0 |
△H<0 |
|
实例 |
多数分解反应等 |
中和反应、燃烧反应等 |
(一)反应热与焓变的关系
|
|
反应热 |
焓变 |
|
概念 |
化学反应过程中,当反应物和生成物具有相同 的温度时,所吸收或放出的热量。 |
在恒温、恒压的条件下,化学反应过程中 吸收或释放的热量 |
|
实质 |
在化学反应过程中,旧化学键断裂吸收的能量与新化学键形成时放出的能量的差。 |
|
|
表示符号 |
Q |
△H |
|
单位 |
kJ·mol-1 |
|
|
测定装置 |
量热计 |
|
|
二者关系 |
恒温、恒压下的反应热即为焓变 |
20. A man is being questioned in relation to the ________ murder last night.
A. advised B. attended C. attempted D. admitted
19. Most film adaptation are _______ than the books they’re based on.
A. very well-known B. far better-known
C. fairly well-known D. quite better- known
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com