
6.(2009·南京调研)如图是某一动物物种迁入一个适宜环境后的增长曲线图,下列说法不正确的是
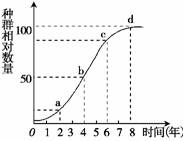 A.图中的增长曲线呈“S”型,d点对应的是K值
A.图中的增长曲线呈“S”型,d点对应的是K值
B.图中表示种群增长速度最快的点是c
C.图中种群数量的增长在迁入第2年后明显加快
D.图中第8年后,种群数量趋于稳定
解析 本题考查对“S”型增长曲线的识图分析能力。种群增长速度最快的点应是b点,即K/2处。
答案 B
5.(2009·临沂质检)如图表示某物种迁入新环境后,种群数量增长速率(平均值)随时间(单位:年)的变化关系。经调查在第5年时该种群的种群数量为200只。下列有关叙述正确的是
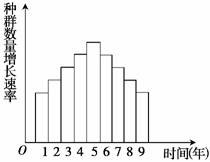
A.由图可知,该物种迁入新环境后,其种群数量一直呈“J”型增长
B.理论上该种群在此环境中的环境容纳量约为400只
C.导致第5年到第9年这段时间内种群数量增长速率下降、种群数量减少的原因主要包括天敌、生活空间和资源等
D.如果该种群为东方田鼠,则将其数量控制在200只左右可有效防治鼠患
解析 本题中的柱状图表示的是种群数量增长速率与时间的关系。第1-5年种群数量增长速率不断增大,种群数量增加得越来越快;第5年时种群数量增长速率最大,此时种群数量增加最快;第5-9年种群数量增长速率虽然逐渐减小,种群数量增加得越来越慢,但依然在增多。由此可判断,图示时间内种群数量呈“S”型增长(但未达到K值);由于第5年时该种群数量为200只,等于K/2,故理论上K值(环境容纳量)为400只;防治鼠患时,若将其数量控制在K/2左右,则鼠种群具有最大的增长速率,很快就会恢复到较大的数量,应将其数量控制在200只以下。
答案 B
4.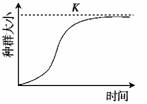 (2010·江苏南京高三学情分析)如右图所示为有限环境中某一种群增长的曲线。下列有关叙述错误的是
(2010·江苏南京高三学情分析)如右图所示为有限环境中某一种群增长的曲线。下列有关叙述错误的是
A.K值是环境条件所允许达到的种群数量最大值
B.在K值之前,种群的数量逐渐增大
C.如果不考虑迁入迁出等其他因素,在K值时出生率=死亡率
D.假设这是鱼的种群,当种群达到K值时才能开始捕捞
解析 一般将种群数量控制在环境容纳量的一半,即K/2左右,此时种群增长率最快,可提供的资源数量也最多,而且又不影响资源的再生,所以当鱼的种群数量大于K/2值时即可开始捕捞。
答案 D
3.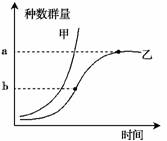 (2010·江苏泰兴调研)如右图为两种生物种群的生长曲线,以下说法错误的是
(2010·江苏泰兴调研)如右图为两种生物种群的生长曲线,以下说法错误的是
A.按甲曲线增长的种群无K值,无种内斗争,增长率始终不变
B.按乙曲线增长的种群,到a点后种内斗争最为激烈,且增长率为零
C.按乙曲线增长的不同种群在同一环境下,b点时的增长速率不同,但均为最大值
D.甲曲线的数学模型为Nt=N0λt,其中λ代表增长率
解析 λ代表该种群数量是一年前种群数量的倍数。
答案 D
2.(2009·深圳调研)下列有关调查种群密度的说法错误的是
A.五点取样和等距离取样是样方法取样的常用方式,遵循了随机取样的原则
B.调查古树木、蝗虫的幼虫、某种蛇的种群密度,通常采用样方法
C.标志重捕法调查得到的种群密度一般不是最精确的现实反映
D.将M只鹿标记,在捕获的n只鹿中有m只被标记,则该鹿群约有(M×n)÷m只
解析 由于蛇的行动范围较广,故调查其种群密度不宜采用样方法,而是标志重捕法。
答案 B
1.(2009·广州综合测试)如图表示野兔进入某草原后的种群数量增长情况,对该图的叙述不正确的是
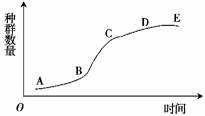
A.AB段兔群数量较少的原因是性别比例失调
B.BC段兔群的年龄组成为增长型
C.CD段兔群的生存斗争在进一步加剧
D.DE段兔群数量的增长率几乎为0
解析 AB段显示兔群逐步适应新环境,种群数量逐渐增多,而非性别比例失调,性别比例失调的结果是种群数量减少;DE段显示兔群处于动态的平衡中,此时期兔群数量的增长率在极小的范围内波动,即几乎为零。
答案 A
21.(12分)某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为____________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中所含固体物质的成分有: 种(填1种.2种.1种或2种),具体情况是 ,若溶液未变红色则说明硬质试管中固体物质的成分有: 种(填1种.2种.1种或2种),具体情况是 。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是: (用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按右图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式:
。
20.(12分) A.B.C.D.E.X.Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
(1)若A为金属单质,B为氢气,X为盐酸,Y为强碱溶。则A物质的名称是 ;D与Y反应的离子方程式为 ;
(2)若A.C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则A→C的反应类型是 ;将X通入A的溶液中,可观察到的现象是 ;C→D的化学反应方程式为 。
(3)若A、C为为短周期不同主族元素组成的单质,通常状况下,A.C均为固体,X.Y为气体。则A→C的反应方程式是 ;该反应发生时盛有X的装置 (填是.否)需要做什么处理中,如需要怎么处理 (如不需要此问不需作答)。为什么: 。
19.(14分)X.Y.Z.L.M五种元素的原子序数依次增大。X.Y.Z.L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:⑴ L的元素符号为________ ; M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。⑵ Z.X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。⑶硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,原子结构示意图为: 其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。a.+99.7 mol·L-1 b.+29.7 mol·L- 1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1⑷用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:____________________;
由R生成Q的化学方程式:__________________________;
18.(10分)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+.NH4+.Mg2+.Ba2+.Cl-.SO42-.CO32-。将该混合物溶于水后得澄清溶液.现取3份l00mL该溶液分别进行如下实验:
|
试验序号 |
试验内容 |
试验结果 |
|
1 |
加AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体 1.12L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤.干燥.称量;再向沉淀中加足量稀盐酸,然后干燥.称量 |
第一次称量读数为 6.27g,第二次称量读数为 2.33g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是 (填“一定存在”.“一定不存在”或“不能确定”);根据实验l-3判断混合物中一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
|
阴离子符号 |
物质的量浓度(mo1·L-) |
|
|
|
|
|
|
(3)试确定K+是否存在? ,判断的理由是 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com